Főszerkesztő: C. Michael Gibson, M.S., M.D. ; Associate Editor(s)-in-Chief: Aparna Vuppala, M.B.B.B.S.
Disclaimer
AWikiDoc NEM TÁMOGATJA AZ ÉRVÉNYESSÉGET. A WikiDoc nem hivatásos egészségügyi szolgáltató, és nem is alkalmas helyettesítője az engedéllyel rendelkező egészségügyi szolgáltatónak. A WikiDoc oktatási eszköznek szánják, nem pedig az egészségügyi ellátás bármely formájának eszközeként. A WikiDoc gyógyszeroldalak oktatási tartalma az FDA betegtájékoztatóján, a National Library of Medicine tartalmán és gyakorlati útmutatókon / konszenzusos nyilatkozatokon alapul. A WikiDoc nem támogatja olyan gyógyszerek vagy eszközök alkalmazását, amelyek nem felelnek meg a címkézésüknek. Kérjük, olvassa el a teljes jogi nyilatkozatunkat itt.
Áttekintés
A butalbital egy kombinált készítmény, amelyet az FDA engedélyezett a tenziós (vagy izomösszehúzódásos) fejfájás tünetegyüttesének enyhítésére. Gyakori mellékhatások közé tartozik a szédülés és a gyomor-bélrendszeri zavarok, beleértve a hányingert, hányást és puffadást, a toxikus epidermális nekrolízis és az erythema multiforme.
Felnőttek javallatai és adagolása
FDA-jelölt javallatok és adagolás (felnőttek)
Főfájás
- A butalbit, aszpirin és koffein tabletta a tenziós (vagy izomösszehúzódásos) fejfájás tünetegyüttesének enyhítésére javallt.
- A butalbital, az aszpirin és a koffein hatékonyságát és biztonságosságát alátámasztó bizonyítékok nem állnak rendelkezésre a többszörösen visszatérő fejfájás kezelésében. Ebben a tekintetben óvatosságra van szükség, mivel a butalbital szokásképző és potenciálisan visszaélhető.
Off-Label alkalmazás és adagolás (felnőtt)
Az irányelvekkel támogatott alkalmazás
A butalbital felnőtt betegeknél történő, irányelvekkel támogatott off-label alkalmazásával kapcsolatban korlátozott információ áll rendelkezésre.
Nem irányvonallal támogatott alkalmazás
A Butalbital felnőtt betegeknél történő, nem irányvonallal támogatott alkalmazásával kapcsolatban korlátozott információ áll rendelkezésre.
GYermekgyógyászati javallatok és adagolás
FDA által megjelölt javallatok és adagolás (gyermekgyógyászat)
A Butalbital gyermekgyógyászati betegeknél történő FDA által megjelölt alkalmazásával kapcsolatban korlátozott információ áll rendelkezésre.
Off-Label alkalmazás és adagolás (gyermekgyógyászat)
Az irányelvek által támogatott alkalmazás
A Butalbital irányelvek által nem támogatott alkalmazásáról gyermekgyógyászati betegeknél korlátozott információ áll rendelkezésre.
Nem irányvonallal támogatott alkalmazás
A Butalbital nem irányvonalon kívüli, nem irányvonallal támogatott alkalmazásáról gyermekbetegeknél korlátozott információ áll rendelkezésre.
Ellenjavallatok
- Aszpirinnel, koffeinnel vagy barbiturátokkal szembeni túlérzékenység. Porfíriás betegek.
Figyelmeztetések
Drogfüggőség:
- A barbiturátok tartós alkalmazása gyógyszerfüggőséget okozhat, amelyet pszichés függőség, ritkábban fizikai függőség és tolerancia jellemez. A butalbital, az aszpirin és a koffein visszaélési érzékenysége hasonló a többi barbiturát tartalmú gyógyszerkombinációéhoz. Óvatosan kell eljárni, amikor olyan betegek számára írnak fel gyógyszert, akiknél ismert a túlzott mennyiségű gyógyszerbevitelre való hajlam, ami nem ritka a krónikus tenziós fejfájásban szenvedő betegeknél.
Az ambuláns betegeknél történő alkalmazás:
- A butalbitál, az aszpirin és a koffein károsíthatja a potenciálisan veszélyes feladatok, például a gépjárművezetés vagy a gépek kezelése során szükséges szellemi és/vagy fizikai képességeket. A beteget ennek megfelelően figyelmeztetni kell. A butalbital központi idegrendszeri depresszív hatása additív lehet más CNS depresszánsokéval. Más nyugtató-hipnotizáló szerekkel vagy alkohollal való egyidejű alkalmazása kerülendő. Ha ilyen kombinált kezelésre van szükség, egy vagy több szer adagját esetleg csökkenteni kell.
Figyelmeztetések
- A szalicilátokat gyomorfekély vagy véralvadási rendellenességek esetén különös óvatossággal kell alkalmazni.
Mellékhatások
Klinikai vizsgálatok tapasztalatai
- A leggyakoribb mellékhatások az álmosság és a szédülés. Ritkább mellékhatások a szédülés és a gyomor-bélrendszeri zavarok, beleértve a hányingert, hányást és puffadást. Butalbital, aszpirin és koffein alkalmazásával kapcsolatban csontvelő-szuppresszió egyszeri előfordulását jelentették. Számos esetben számoltak be bőrgyógyászati reakciókról, beleértve a toxikus epidermális nekrolízist és az erythema multiforme-t.
Marketing utáni tapasztalatok
A butalbitál forgalomba hozatal utáni tapasztalatokkal kapcsolatban korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Kölcsönhatások
A Butalbital gyógyszerkölcsönhatásaival kapcsolatban korlátozott mennyiségű információ áll rendelkezésre a gyógyszer címkéjén.
Egyedi populációkban történő alkalmazás
Terhesség
Terhességi kategória (FDA): C
- Nem végeztek megfelelő vizsgálatokat állatokon annak megállapítására, hogy ez a gyógyszer befolyásolja-e a hímek vagy nőstények termékenységét, teratogén potenciállal rendelkezik-e, vagy van-e egyéb káros hatása a magzatra. Bár terhes nőkön nem készültek jól kontrollált vizsgálatok, a több mint húszéves forgalmazási és klinikai tapasztalatok nem tartalmaznak pozitív bizonyítékot a magzatra gyakorolt káros hatásokra vonatkozóan. Bár nincs egyértelműen meghatározott kockázat, az ilyen tapasztalatok nem zárhatják ki az emberi magzatot érintő ritka vagy finom károsodás lehetőségét. A butalbital, az aszpirin és a koffein csak akkor alkalmazható terhes nőknél, ha egyértelműen szükséges.
Várandóssági kategória (AUS): Nincs az Ausztrál Gyógyszerértékelő Bizottság (ADEC) iránymutatása a Butalbital terhes nőknél történő alkalmazására vonatkozóan.
Vajúdás és szülés
A Butalbital vajúdás és szülés alatti alkalmazására vonatkozóan nincs FDA útmutató.
Szoptató anyák
- A butalbital, az aszpirin és a koffein hatása a szoptató anyák csecsemőire nem ismert. A szalicilátok és a barbiturátok kiválasztódnak a szoptató anyák anyatejébe. A csecsemők szérumszintje a terápiás dózisok esetén feltételezhetően jelentéktelen.
GYermekeknél történő alkalmazás
- A biztonságosságot és a hatékonyságot 12 évesnél fiatalabb gyermekbetegeknél nem állapították meg.
Geriátriai alkalmazás
A Butalbital geriátriai betegek tekintetében történő alkalmazására vonatkozóan nincs FDA-iránymutatás.
Gender
A Butalbital meghatározott nemű populációk tekintetében történő alkalmazására vonatkozóan nincs FDA-iránymutatás.
Rasszus
Nincs FDA-iránymutatás a Butalbital alkalmazására vonatkozóan meghatározott faji populációk tekintetében.
Veseelégtelenség
Nincs FDA-iránymutatás a Butalbital alkalmazására vonatkozóan vesekárosodott betegeknél.
Májelégtelenség
Nincs FDA útmutató a Butalbital májkárosodásban szenvedő betegeknél történő alkalmazására vonatkozóan.
Reproduktív potenciállal rendelkező nők és férfiak
Nincs FDA útmutató a Butalbital reproduktív potenciállal rendelkező nőknél és férfiaknál történő alkalmazására vonatkozóan.
Immunkompromittált betegek
Nincs FDA útmutató a Butalbitalnak immunkompromittált betegeknél történő alkalmazására vonatkozóan.
Alkalmazás és megfigyelés
Alkalmazás
- Orálisan
Monitorozás
A Butalbital megfigyelésére vonatkozóan korlátozott információ áll rendelkezésre a gyógyszer címkéjében.
Intravénás kompatibilitás
A Butalbital intravénás kompatibilitására vonatkozóan korlátozott mennyiségű információ áll rendelkezésre a gyógyszer címkéjén.
Túladagolás
- A butalbital, az aszpirin és a koffein akut túladagolásának toxikus hatásai elsősorban a barbiturát komponensnek, és kisebb mértékben az aszpirinnek tulajdoníthatók. Mivel a koffein toxikus hatásai csak nagyon nagy dózisokban jelentkeznek, a butalbital, az aszpirin és a koffein túladagolásából származó jelentős koffeintoxicitás lehetősége valószínűtlen. Az akut barbiturátmérgezésre visszavezethető tünetek közé tartozik az álmosság, zavartság és kóma; légzésdepresszió; hipotenzió; sokk. Az akut aszpirin-mérgezésre visszavezethető tünetek közé tartozik a hiperpnoe; sav-bázis zavarok metabolikus acidózis kialakulásával; hányás és hasi fájdalom; fülzúgás; hipertermia; hipotrombinémia; nyugtalanság; delírium; görcsök. Akut koffeinmérgezés álmatlanságot, nyugtalanságot, remegést és delíriumot okozhat; tachycardia és extrasystolák. A kezelés elsősorban a barbiturátmérgezés kezeléséből és a szalicilizmus okozta sav-bázis egyensúlyhiány korrekciójából áll. Az eszméleténél lévő betegnél a hányást mechanikusan vagy hánytatókkal kell előidézni. Gyomormosást lehet alkalmazni, ha a garat- és gégereflexek jelen vannak, és ha a lenyelés óta kevesebb mint 4 óra telt el. Az eszméletlen beteg gyomormosása előtt és szükség esetén az asszisztált lélegeztetés biztosítása érdekében mandzsettás endotracheális csövet kell bevezetni. A diurézist, a vizelet lúgosítását és az elektrolit-zavarok korrekcióját intravénás folyadékok, például 1%-os nátrium-bikarbonát 5%-os vízben lévő dextrózban történő adagolásával kell elvégezni. Aprólékos figyelmet kell fordítani a megfelelő tüdőszellőzés fenntartására. A hipotenzió korrekciója szükségessé teheti levartherenol-bitartarát vagy fenilefrin-hidroklorid intravénás infúzióval történő beadását. Súlyos mérgezés esetén peritoneális dialízis, hemodialízis vagy csereátömlesztés életmentő lehet. A hipotrombinémiát intravénásan K-vitaminnal kell kezelni.
A Butalbital krónikus túladagolása tekintetében korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Farmakológia
A Butalbital farmakológiája tekintetében korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Hatásmechanizmus
- Farmakológiai szempontból a butalbital, az aszpirin és a koffein egyesíti az aszpirin fájdalomcsillapító tulajdonságait a butalbital anxiolitikus és izomlazító tulajdonságaival.
A butalbital, az aszpirin és a koffein klinikai hatékonyságát a tenziós fejfájásban kettős vak, placebokontrollos, több klinikán végzett vizsgálatokban igazolták. Egy faktoriális felépítésű vizsgálatban a butalbitált, az aszpirint és a koffeint hasonlították össze az egyes fő összetevőkkel. Ez a vizsgálat kimutatta, hogy az egyes komponensek hozzájárulnak a butalbital, az aszpirin és a koffein hatékonyságához a tenziós fejfájás céltüneteinek (fejfájás, pszichés feszültség és izomösszehúzódás a fej, a nyak és a váll területén) kezelésében. Az egyes tünetek és a tünetegyüttes egésze esetében a butalbital, az aszpirin és a koffein szignifikánsan jobb klinikai hatást mutatott, mint bármelyik komponens önmagában.
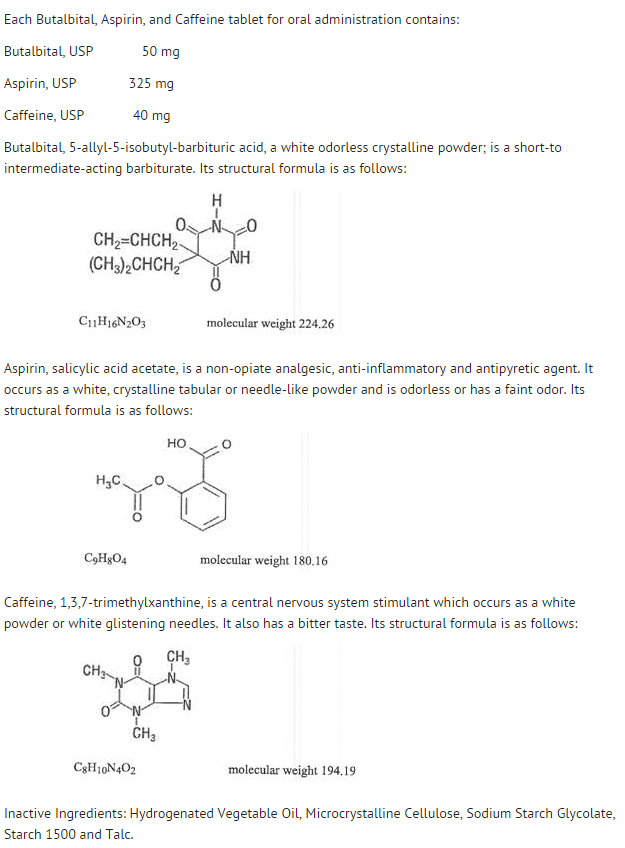
Szerkezet
- Az egyes összetevők viselkedését az alábbiakban ismertetjük.
- Az aszpirin szisztémás hozzáférhetősége orális adagolás után nagymértékben függ az adagolási formától, az étel jelenlététől, a gyomorürülési időtől, a gyomor pH-jától, az antacidoktól, a pufferanyagoktól és a részecskemérettől. Ezek a tényezők nem feltétlenül az összes szalicilát felszívódásának mértékét, hanem inkább az aszpirin felszívódást megelőző stabilitását befolyásolják.
- A felszívódás során és a felszívódást követően az aszpirin főként szalicilsavvá hidrolizálódik és eloszlik a szervezet valamennyi szövetében és folyadékában, beleértve a magzati szöveteket, az anyatejet és a központi idegrendszert (CNS). A legmagasabb koncentráció a plazmában, a májban, a vesekéregben, a szívben és a tüdőben található. A plazmában a szalicilsav és metabolitjainak mintegy 50-80%-a lazán kötődik a plazmafehérjékhez.
- A teljes szalicilátok kiürülése telítődési kinetikának van kitéve; az elsőrendű eliminációs kinetika azonban 650 mg-os dózisokig még mindig jó közelítést jelent. Az aszpirin plazma felezési ideje körülbelül 12 perc, a szalicilsav és/vagy az összes szalicilátoké pedig körülbelül 3,0 óra.
- A terápiás dózisok eliminációja a vesén keresztül történik, vagy szalicilsav vagy más biotranszformációs termékek formájában. A renális clearance-t nagymértékben fokozza a lúgos vizelet, ahogyan azt nátrium-bikarbonát vagy kálium-citrát egyidejű adagolása eredményezi.
- Az aszpirin biotranszformációja elsősorban a hepatocitákban történik. A fő metabolitok a szalicilsav (75%), a szalicilát fenol- és acilglükuronidjai (15%), valamint a gentisic- és gentisurinsav (1%). Az aszpirinkomponens butalbital, aszpirin és koffein biológiai hozzáférhetősége megegyezik az oldatéval, kivéve a lassabb felszívódási sebességet. A 650 mg-os adag után 40 perccel 8,80 mcg/ml csúcskoncentrációt értek el.
- A butalbital jól felszívódik a gyomor-bél traktusból és várhatóan eloszlik a szervezet legtöbb szövetében. A barbiturátok általában megjelenhetnek az anyatejben és könnyen átjutnak a placentáris gáton. A plazma- és szövetfehérjékhez különböző mértékben kötődnek, és a kötődés a lipidoldékonyság függvényében közvetlenül növekszik.
- A butalbitál kiürülése elsősorban a vesén keresztül történik (az adag 59%-88%-a) változatlan hatóanyag vagy metabolitok formájában. A plazma felezési ideje körülbelül 35 óra. A vizelettel történő kiválasztódás termékei közé tartozott az alapdrog (az adag kb. 3,6%-a), 5-izobutil-5-(2,3-dihidroxipropil)barbitursav (az adag kb. 24%-a), 5-allyl-5(3-hidroxi-2-metil-1-propil)barbitursav (az adag kb. 4,8%-a), a karbamid kiválasztásával hidrolizált barbitursavgyűrűvel rendelkező termékek (az adag kb. 14%-a), valamint azonosítatlan anyagok. A vizelettel ürített anyag 32%-a konjugált volt.
- A butalbital, az aszpirin és a koffein butalbital komponensének biológiai hozzáférhetősége megegyezik az oldatéval, kivéve a felszívódás sebességének csökkenését. A 2020 ng/ml csúcskoncentráció körülbelül 1,5 órával 100 mg-os adag beadása után érhető el.
- A butalbitál in vitro plazmafehérje kötődése 45% a 0,5-20 mcg/ml koncentrációtartományban. Ez a plazmafehérje-kötődésnek abba a tartományába esik (20-45%), amelyet más barbiturátok, például fenobarbitál, pentobarbitál és szekobarbitál-nátrium esetében jelentettek. A plazma-vér koncentráció aránya majdnem egység volt, ami azt jelzi, hogy a butalbitálnak nincs preferenciális eloszlása sem a plazmába, sem a vérsejtekbe. (a toxicitásra vonatkozó információkat lásd a Túladagolás című fejezetben).
- A legtöbb xantinhoz hasonlóan a koffein is gyorsan felszívódik és eloszlik a szervezet valamennyi szövetében és folyadékában, beleértve a központi idegrendszert, a magzati szöveteket és az anyatejet is.
- A koffein gyorsan kiürül az anyagcsere és a vizelettel történő kiválasztás révén. A plazma felezési ideje körülbelül 3,0 óra. A kiválasztást megelőző hepatikus biotranszformáció körülbelül azonos mennyiségű 1-metil-xantint és 1-metilurinsavat eredményez. A vizelettel visszanyert dózis 70%-ának csak 3%-a volt változatlan hatóanyag.
- A butalbital, az aszpirin és a koffein koffein komponensének biológiai hozzáférhetősége megegyezik az oldatéval, kivéve a kissé hosszabb csúcsérték elérési időt. A 80 mg-os adag esetében kevesebb mint egy óra alatt 1660 ng/ml csúcskoncentrációt értek el
- Butalbital, aszpirin és koffein tabletta, USP 50 mg/325 mg/40 mg fehér, kerek, pontozatlan, tömörített tabletta “West-ward 785” felirattal.
- 20-25oC-on (68-77oF) tárolható . Fénytől és nedvességtől védje.
- Az USP-ben meghatározottak szerint gyermekbiztos zárószerkezettel ellátott, tömör, fényálló tartályban adagolja.
- Az alkohol és a butalbitál kölcsönhatását nem állapították meg. Beszéljen kezelőorvosával az alkohol és a gyógyszer együttes szedésének hatásairól.
Farmakodinamika
A butalbitál farmakodinamikájával kapcsolatban korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Farmakokinetika
Aszpirin:
Butalbital:
Koffein:
Nonklinikai toxikológia
A butalbitál nem klinikai toxikológiájára vonatkozóan korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Klinikai vizsgálatok
A butalbitál klinikai vizsgálataira vonatkozóan korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Hogyan kerül forgalomba
30 tablettás palackok50 tablettás palackok100 tablettás palackok500 tablettás palackok1000 tablettás palackok100 tablettás egységdózisú dobozok
Tárolás
A gyógyszer címkéjén korlátozott mennyiségű információ található a butalbital tárolására vonatkozóan.
Képek
Képek
A gyógyszer neve: Összetevő(k): Butalbital, acetaminofen és koffein
Az összetevő(k): Butalbital, acetaminofen és koffein: BUTALBITÁL, ACETAMINOPHEN, KAFFEIN
Impresszum: West;ward;787
Adagolás: 50 mg
Szín(ek): Szín(ek): Kék
Festék(ek): Kék
Állat: Kék
Alak: Kerek
Méret (mm): 11
Méret: 1
NDC:01431787
Gyógyszercímke Szerző: A gyógyszer címkéje: West-Ward Pharmaceutical Corp
Ez a tablettakép a National Library of Medicine’s PillBox.

A gyógyszer neve: Butalbital, aszpirin és koffein
Az összetevő(k): Butalbital, aszpirin és koffein: BUTALBITÁL, ASZPIRIN, KAFFEIN
Impresszum: BUTALBITÁL, ASZPIRIN, KAFFEIN
Imp: Nyugati;785
Adagolás: Butalinnal, baktalinnal, baktalinnal, baktalinnal, baktalinnal, baktalinnal, baktalinnal és baktalinnal: 50 mg
Szín(ek): Fehér
Állat: West-ward Pharmaceutical Corp
Ez a tablettakép a National Library of Medicine’s PillBox.

A gyógyszer neve: Butalbital, aszpirin és koffein
Az összetevő(k): Butalbital, aszpirin és koffein: BUTALBITÁL, ASZPIRIN, KAFFEIN
Impresszum: BUTALBITÁL, ASZPIRIN, KAFFEIN
Imp: WATSON;3219
Dosage: 50 mg
Szín(ek): Kapszula
Méret (mm): 22
Méret: 1
NDC:05913219
Gyógyszerkészítmény címkéjének szerzője: Watson Laboratories, Inc.
Ezt a tablettaképet a National Library of Medicine’s PillBox szolgáltatta.
A gyógyszer neve: Butalbital, aszpirin és koffein tabletta
összetevő(k): Aszpirin, butalbitál, koffein
Impresszum: West;ward;785
Adagolás: Aszpirin, bazalint, tablettát, tablettát, tablettát, tablettát, tablettát és tablettát: 50 mg
Szín(ek): Fehér
Állat: Qualitest
Ezt a tablettaképet a National Library of Medicine’s PillBox.
Package and Label Display Panel
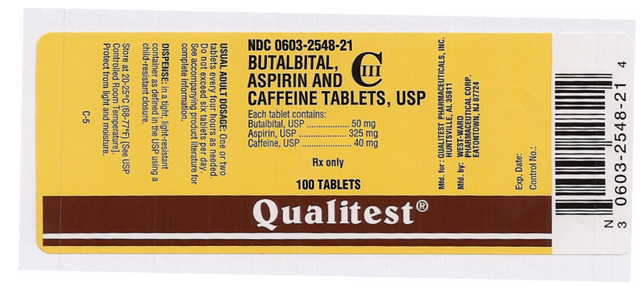
Az FDA címke képét a National Library of Medicine bocsátotta rendelkezésre.

Az FDA címke képét a National Library of Medicine bocsátotta rendelkezésre.
Betegtájékoztató információ
A butalbitálra vonatkozó betegtájékoztató információval kapcsolatban korlátozott információ áll rendelkezésre a gyógyszer címkéjén.
Vigyázat az alkohollal
Márkanevek
A gyógyszer címkéjén a Butalbital márkanevére vonatkozóan korlátozott számú információ áll rendelkezésre.
Look-Alike gyógyszernevek
A gyógyszer címkéjén a Butalbital Look-Alike gyógyszernevekre vonatkozóan korlátozott számú információ áll rendelkezésre.
A gyógyszerhiányos állapot
.