Editor-In-Chief: C. Michael Gibson, M.S., M.D. ; Associate Editor(s) -in-Chief: Aparna Vuppala, M.B.B.S.
Disclaimer
WikiDoc NON GARANTISCE LA VALIDITÀ. WikiDoc non è un fornitore di assistenza sanitaria professionale, né è un sostituto adatto per un fornitore di assistenza sanitaria autorizzato. WikiDoc è destinato ad essere uno strumento educativo, non uno strumento per qualsiasi forma di fornitura di assistenza sanitaria. Il contenuto educativo sulle pagine dei farmaci di WikiDoc è basato sul foglietto illustrativo della FDA, sui contenuti della National Library of Medicine e sulle linee guida pratiche / dichiarazioni di consenso. WikiDoc non promuove la somministrazione di alcun farmaco o dispositivo che non sia coerente con la sua etichettatura. Si prega di leggere il nostro disclaimer completo qui.
Panoramica
Butalbital è una combinazione approvata dalla FDA per il trattamento del sollievo del complesso dei sintomi della cefalea tensiva (o da contrazione muscolare). Le reazioni avverse comuni includono stordimento e disturbi gastrointestinali tra cui nausea, vomito e flatulenza, necrolisi epidermica tossica ed eritema multiforme.
Indicazioni e dosaggio per adulti
Indicazioni e dosaggio FDA-Labeled (Adulti)
Mal di testa
- Le compresse di butalbital, aspirina e caffeina sono indicate per il sollievo del complesso di sintomi della cefalea da tensione (o contrazione muscolare).
- Non sono disponibili prove a sostegno dell’efficacia e della sicurezza di butalbital, aspirina e caffeina nel trattamento delle cefalee multiple ricorrenti. E’ richiesta cautela a questo proposito perché il butalbital forma l’abitudine ed è potenzialmente abusabile.
Uso e Dosaggio Off-Label (Adulti)
Uso supportato dalla linea guida
Ci sono informazioni limitate riguardo all’Uso Off-Label supportato dalla linea guida del butalbital in pazienti adulti.
Uso non supportato dalla linea guida
Ci sono informazioni limitate riguardo all’uso non supportato dalla linea guida di Butalbital in pazienti adulti.
Indicazioni e dosaggio pediatrici
Indicazioni e dosaggio etichettati dalla FDA (pediatrici)
Ci sono informazioni limitate riguardo all’uso di Butalbital in pazienti pediatrici.
Uso Off-Label e Dosaggio (Pediatrico)
Uso supportato dalla linea guida
Ci sono informazioni limitate riguardo all’Uso Off-Label supportato dalla linea guida di Butalbital in pazienti pediatrici.
Uso non supportato dalla linea guida
Ci sono informazioni limitate riguardo all’uso non supportato dalla linea guida di Butalbital in pazienti pediatrici.
Contraindicazioni
- Ipersensibilità ad aspirina, caffeina o barbiturici. Pazienti con porfiria.
Avvertenze
Dipendenza:
- L’uso prolungato di barbiturici può produrre dipendenza, caratterizzata da dipendenza psichica, e meno frequentemente, dipendenza fisica e tolleranza. La responsabilità di abuso di butalbital, aspirina e caffeina è simile a quella di altre combinazioni di farmaci contenenti barbiturici. La cautela deve essere esercitata quando si prescrivono farmaci per pazienti con una nota propensione ad assumere quantità eccessive di farmaci, che non è rara nei pazienti con cefalea tensiva cronica.
Uso in pazienti ambulatoriali:
- Butalbital, aspirina e caffeina possono compromettere le capacità mentali e/o fisiche richieste per lo svolgimento di compiti potenzialmente pericolosi, come guidare un’auto o azionare macchinari. Il paziente deve essere avvertito di conseguenza. Gli effetti depressivi del sistema nervoso centrale del butalbital possono essere additivi a quelli di altri depressivi del SNC. L’uso concomitante con altri sedativi-ipnotici o alcol dovrebbe essere evitato. Quando tale terapia combinata è necessaria, la dose di uno o più agenti può dover essere ridotta.
Precauzioni
- I salicilati devono essere usati con estrema cautela in presenza di ulcera peptica o anomalie di coagulazione.
Reazioni avverse
esperienza negli studi clinici
- Le reazioni avverse più frequenti sono sonnolenza e vertigini. Reazioni avverse meno frequenti sono stordimento e disturbi gastrointestinali inclusi nausea, vomito e flatulenza. Una singola incidenza di soppressione del midollo osseo è stata riportata con l’uso di butalbital, aspirina e caffeina. Sono stati riportati diversi casi di reazioni dermatologiche tra cui necrolisi epidermica tossica ed eritema multiforme.
Esperienza post-marketing
Ci sono informazioni limitate riguardanti l’esperienza post-marketing di Butalbital nell’etichetta del farmaco.
Interazioni farmacologiche
Ci sono informazioni limitate riguardo alle interazioni farmacologiche di Butalbital nell’etichetta del farmaco.
Uso in popolazioni specifiche
Gravidanza
Categoria di gravidanza (FDA): C
- Non sono stati effettuati studi adeguati negli animali per determinare se questo farmaco influisce sulla fertilità nei maschi o nelle femmine, ha un potenziale teratogeno o ha altri effetti avversi sul feto. Mentre non ci sono studi ben controllati in donne incinte, oltre venti anni di marketing e di esperienza clinica non includono alcuna prova positiva di effetti avversi sul feto. Anche se non esiste un rischio chiaramente definito, tale esperienza non può escludere la possibilità di danni infrequenti o sottili al feto umano. Il butalbital, l’aspirina e la caffeina devono essere usati nelle donne in gravidanza solo in caso di chiara necessità.
Categoria gravidanza (AUS): Non c’è una guida dell’Australian Drug Evaluation Committee (ADEC) sull’uso del Butalbital in donne che sono incinte.
Lavoro e parto
Non c’è una guida della FDA sull’uso del Butalbital durante il lavoro e il parto.
Madri che allattano
- Gli effetti del butalbital, dell’aspirina e della caffeina sui bambini delle madri che allattano non sono noti. Salicilati e barbiturici sono escreti nel latte materno delle madri che allattano. I livelli sierici nei neonati sono ritenuti insignificanti con dosi terapeutiche.
Uso pediatrico
- Sicurezza ed efficacia in pazienti pediatrici di età inferiore ai 12 anni non sono state stabilite.
Uso geriatrico
Non esiste una guida della FDA sull’uso di Butalbital rispetto ai pazienti geriatrici.
Gender
Non esiste una guida della FDA sull’uso di Butalbital rispetto a specifiche popolazioni di genere.
Race
Non ci sono indicazioni della FDA sull’uso del Butalbital rispetto a specifiche popolazioni razziali.
Improbabilità renale
Non ci sono indicazioni della FDA sull’uso del Butalbital in pazienti con insufficienza renale.
Malattia epatica
Non ci sono indicazioni della FDA sull’uso del Butalbital in pazienti con insufficienza epatica.
Femmine di potenziale riproduttivo e maschi
Non ci sono indicazioni della FDA sull’uso di Butalbital in donne di potenziale riproduttivo e maschi.
Pazienti immunocompromessi
Non ci sono indicazioni della FDA sull’uso di Butalbital in pazienti che sono immunocompromessi.
Somministrazione e Monitoraggio
Somministrazione
- Orale
Monitoraggio
Ci sono informazioni limitate riguardo al Monitoraggio di Butalbital nell’etichetta del farmaco.
Compatibilità IV
Ci sono informazioni limitate riguardo alla compatibilità IV di Butalbital nell’etichetta del farmaco.
Sovradosaggio
- Gli effetti tossici del sovradosaggio acuto di butalbital, aspirina e caffeina sono attribuibili principalmente alla sua componente barbiturica e, in misura minore, all’aspirina. Poiché gli effetti tossici della caffeina si verificano solo a dosaggi molto alti, la possibilità di una significativa tossicità della caffeina dal sovradosaggio di butalbital, aspirina e caffeina è improbabile. I sintomi attribuibili all’avvelenamento acuto da barbiturici includono sonnolenza, confusione e coma; depressione respiratoria; ipotensione; shock. I sintomi attribuibili all’avvelenamento acuto da aspirina includono iperpnea; disturbi acido-base con sviluppo di acidosi metabolica; vomito e dolore addominale; tinnito; ipertermia; ipoprotrombinemia; irrequietezza; delirio; convulsioni. L’avvelenamento acuto da caffeina può causare insonnia, irrequietezza, tremore e delirio; tachicardia ed extrasistoli. Il trattamento consiste principalmente nella gestione dell’intossicazione da barbiturici e nella correzione dello squilibrio acido-base dovuto al salicilismo. Il vomito dovrebbe essere indotto meccanicamente o con emetici nel paziente cosciente. La lavanda gastrica può essere usata se sono presenti i riflessi faringei e laringei e se sono passate meno di 4 ore dall’ingestione. Un tubo endotracheale ammanettato dovrebbe essere inserito prima della lavanda gastrica del paziente non cosciente e quando necessario per fornire la respirazione assistita. La diuresi, l’alcalinizzazione delle urine e la correzione dei disturbi elettrolitici devono essere realizzate attraverso la somministrazione di fluidi endovenosi come il bicarbonato di sodio all’1% in destrosio al 5% in acqua. Un’attenzione meticolosa deve essere data al mantenimento di un’adeguata ventilazione polmonare. La correzione dell’ipotensione può richiedere la somministrazione di levartherenol bitartrato o fenilefrina cloridrato per infusione endovenosa. In casi gravi di intossicazione, la dialisi peritoneale, l’emodialisi o la trasfusione di scambio possono essere salvavita. L’ipoprotrombinemia deve essere trattata con Vitamina K, per via endovenosa.
C’è un’informazione limitata riguardante Overdose cronica di Butalbital nell’etichetta del farmaco.
Farmacologia
C’è un’informazione limitata riguardante Butalbital Pharmacology nell’etichetta del farmaco.
Meccanismo d’azione
- Farmacologicamente, butalbital, aspirina e caffeina combina le proprietà analgesiche dell’aspirina con le proprietà ansiolitiche e miorilassanti del butalbital.
L’efficacia clinica di butalbital, aspirina e caffeina nella cefalea da tensione è stata stabilita in studi in doppio cieco, controllati con placebo, multi-clinica. Uno studio con disegno fattoriale ha confrontato il butalbital, l’aspirina e la caffeina con ciascuno dei suoi componenti principali. Questo studio ha dimostrato che ogni componente contribuisce all’efficacia di butalbital, aspirina e caffeina nel trattamento dei sintomi target della cefalea tensiva (dolore alla testa, tensione psichica e contrazione muscolare nella regione della testa, del collo e delle spalle). Per ogni sintomo e per il complesso dei sintomi nel suo insieme, il butalbital, l’aspirina e la caffeina hanno dimostrato di avere effetti clinici significativamente superiori a quelli di entrambi i componenti da soli.
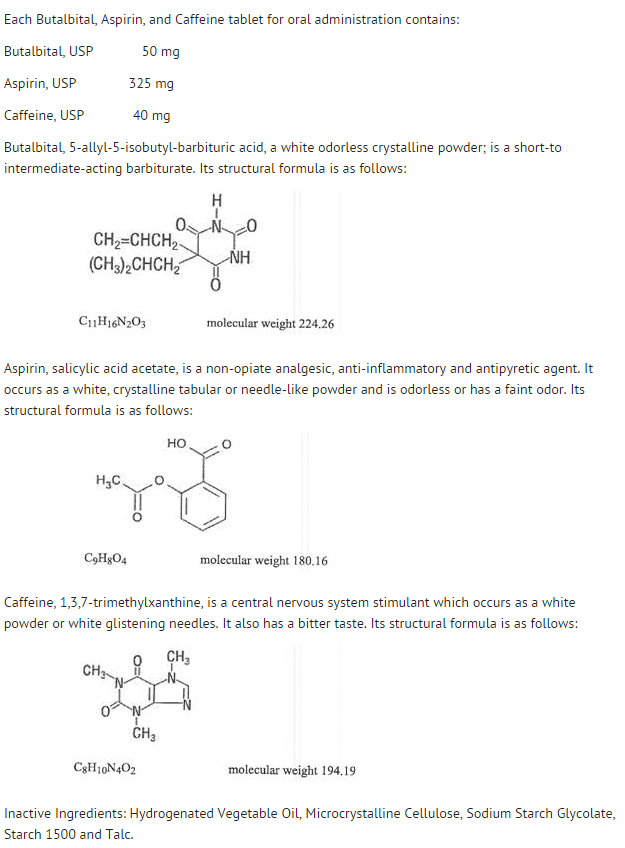
Struttura
- Il comportamento dei singoli componenti è descritto di seguito.
- La disponibilità sistemica dell’aspirina dopo una dose orale dipende fortemente dalla forma di dosaggio, dalla presenza di cibo, dal tempo di svuotamento gastrico, dal pH gastrico, dagli antiacidi, dagli agenti tampone e dalla dimensione delle particelle. Questi fattori influenzano non necessariamente il grado di assorbimento dei salicilati totali ma più la stabilità dell’aspirina prima dell’assorbimento.
- Durante il processo di assorbimento e dopo l’assorbimento, l’aspirina si idrolizza principalmente in acido salicilico e si distribuisce in tutti i tessuti e fluidi corporei, compresi i tessuti fetali, il latte materno e il sistema nervoso centrale (SNC). Le concentrazioni più alte si trovano nel plasma, nel fegato, nella corteccia renale, nel cuore e nei polmoni. Nel plasma, circa il 50%-80% dell’acido salicilico e dei suoi metaboliti sono vagamente legati alle proteine plasmatiche.
- La clearance dei salicilati totali è soggetta a cinetica saturabile; tuttavia, la cinetica di eliminazione di primo ordine è ancora una buona approssimazione per dosi fino a 650 mg. L’emivita plasmatica per l’aspirina è di circa 12 minuti e per l’acido salicilico e/o i salicilati totali è di circa 3,0 ore.
- L’eliminazione delle dosi terapeutiche avviene attraverso i reni o come acido salicilico o altri prodotti di biotrasformazione. La clearance renale è notevolmente aumentata da un’urina alcalina come viene prodotta dalla somministrazione concomitante di bicarbonato di sodio o citrato di potassio.
- La biotrasformazione dell’aspirina avviene principalmente negli epatociti. I principali metaboliti sono l’acido salicilurico (75%), i glucuronidi fenolici e acilici del salicilato (15%), e l’acido gentisico e gentisurico (1%). La biodisponibilità del componente dell’aspirina maalbital, dell’aspirina e della caffeina è equivalente a quella di una soluzione, tranne che per un tasso di assorbimento più lento. Una concentrazione di picco di 8,80 mcg/mL è stata ottenuta a 40 minuti dopo una dose di 650 mg.
- Butalbital è ben assorbito dal tratto gastrointestinale e si prevede che si distribuisca alla maggior parte dei tessuti del corpo. I barbiturici, in generale, possono comparire nel latte materno e attraversano facilmente la barriera placentare. Sono legati alle proteine del plasma e dei tessuti in misura variabile e il legame aumenta direttamente in funzione della solubilità dei lipidi.
- L’eliminazione del butalbital avviene principalmente attraverso il rene (59%-88% della dose) come farmaco invariato o metaboliti. L’emivita plasmatica è di circa 35 ore. I prodotti di escrezione urinaria hanno incluso la droga madre (circa 3,6% della dose), 5-isobutyl-5-(2,3-dihydroxypropyl) acido barbiturico (circa 24% della dose), 5-allyl-5(3-hydroxy-2-methyl-1-propyl) acido barbiturico (circa 4,8% della dose), prodotti con l’anello di acido barbiturico idrolizzato con escrezione di urea (circa 14% della dose), così come materiali non identificati. Del materiale escreto nelle urine, il 32% era coniugato.
- La biodisponibilità del componente butalbital di butalbital, aspirina e caffeina è equivalente a quella di una soluzione tranne che per una diminuzione del tasso di assorbimento. Una concentrazione di picco di 2020 ng/mL si ottiene a circa 1,5 ore dopo una dose di 100 mg.
- Il legame in vitro delle proteine plasmatiche del butalbital è del 45% nell’intervallo di concentrazione da 0,5 a 20 mcg/mL. Questo rientra nell’intervallo di legame alle proteine plasmatiche (dal 20% al 45%) riportato con altri barbiturici come il fenobarbital, il pentobarbital e il secobarbital sodico. Il rapporto di concentrazione plasma-sangue era quasi unito indicando che non c’è distribuzione preferenziale del butalbital nel plasma o nelle cellule del sangue. (vedi OVERDOSAGE per informazioni sulla tossicità).
- Come la maggior parte delle xantine, la caffeina è rapidamente assorbita e distribuita in tutti i tessuti e fluidi del corpo, compreso il SNC, i tessuti fetali e il latte materno.
- La caffeina viene eliminata rapidamente attraverso il metabolismo e l’escrezione nelle urine. L’emivita del plasma è di circa 3,0 ore. La biotrasformazione epatica prima dell’escrezione risulta in quantità circa uguali di 1-metil-xantina e acido 1-metilurico. Del 70% della dose che è stata recuperata nelle urine, solo il 3% era droga invariata.
- La biodisponibilità del componente caffeina per il butalbital, l’aspirina e la caffeina è equivalente a quella di una soluzione, tranne che per un tempo leggermente più lungo al picco. Una concentrazione di picco di 1660 ng/mL è stata ottenuta in meno di un’ora per una dose di 80 mg
- Butalbital, Aspirina e Caffeina compresse, USP 50 mg/325 mg/40 mg sono compresse compresse compresse compresse bianche, rotonde, non graduate, con impresso “West-ward 785”.
- Conservare a 20-25oC (68-77oF). Proteggere dalla luce e dall’umidità.
- Dispensare in un contenitore stretto e resistente alla luce come definito nella USP utilizzando una chiusura a prova di bambino.
- L’interazione alcol-Butalbital non è stata stabilita. Parlate con il vostro medico degli effetti dell’assunzione di alcol con questo farmaco.
Farmacodinamica
Ci sono informazioni limitate riguardanti la Farmacodinamica di Butalbital nell’etichetta del farmaco.
Farmacocinetica
Aspirina:
Butalbital:
Caffeina:
Tossicologia non clinica
Ci sono informazioni limitate riguardo alla Tossicologia non clinica del Butalbital nell’etichetta del farmaco.
Studi clinici
Ci sono informazioni limitate riguardo agli studi clinici del Butalbital nell’etichetta del farmaco.
Come viene fornito
Bottiglie da 30 compresseBottiglie da 50 compresseBottiglie da 100 compresseBottiglie da 500 compresseBottiglie da 1000 compresseUnit Dose Box da 100 compresse
Conservazione
Ci sono informazioni limitate riguardo alla conservazione del Butalbital nell’etichetta del farmaco.
Immagini
Immagini del farmaco
Nome del farmaco: Butalbital, Acetaminofene e Caffeina
Ingrediente(i): BUTALBITAL, ACETAMINOPHEN, CAFFEINA
Impronta: West;ward;787
Dosaggio: 50 mg
Colore(i): Blu
Forma: Rotondo
Dimensione (mm): 11
Score: 1
NDC:01431787
Etichetta del farmaco Autore: West-Ward Pharmaceutical Corp
Questa immagine pillola è fornita da PillBox della National Library of Medicine.

Nome del farmaco: Butalbital, Aspirina e Caffeina
Ingrediente(i): BUTALBITAL, ASPIRINA, CAFFEINA
Impronta: Westward;785
Dosaggio: 50 mg
Colore(i): Bianco
Forma: Rotondo
Dimensione (mm): 11
Score: 1
NDC:01431785
Etichetta del farmaco Autore: West-ward Pharmaceutical Corp
Questa immagine pillola è fornita dalla National Library of Medicine’s PillBox.

Nome farmaco: Butalbital, Aspirina e Caffeina
Ingrediente(i): BUTALBITAL, ASPIRINA, CAFFEINA
Impronta: WATSON;3219
Dosage: 50 mg
Colore(i): Verde, Giallo
Forma: Capsula
Dimensione (mm): 22
Score: 1
NDC:05913219
Etichetta del farmaco Autore: Watson Laboratories, Inc.
Questa immagine della pillola è fornita dalla National Library of Medicine’s PillBox.
Nome del farmaco: Butalbital, Aspirina e Caffeina compresse
Ingrediente(i): ASPIRINA, BUTALBITAL, CAFFEINA
Impronta: West;ward;785
Dosaggio: 50 mg
Colore(i): Bianco
Forma: Rotondo
Dimensione (mm): 7
Score: 1
NDC:06032548
Autore dell’etichetta del farmaco: Qualitest
Questa immagine della pillola è fornita da PillBox della National Library of Medicine.
Pannello di visualizzazione della confezione e dell’etichetta
Questa immagine dell’etichetta FDA è fornita dalla National Library of Medicine.

Questa immagine dell’etichetta FDA è fornita dalla National Library of Medicine.
Informazioni per il paziente
C’è un’informazione limitata riguardante le Informazioni per il paziente di Butalbital nell’etichetta del farmaco.
Precauzioni con l’alcol
Nomi di marca
Ci sono informazioni limitate riguardo ai nomi di marca di Butalbital nell’etichetta del farmaco.
Nomi di farmaci simili
Ci sono informazioni limitate riguardo ai nomi di farmaci simili a Butalbital nell’etichetta del farmaco.