Exeleadでは、希少疾患や小規模またはサービスが行き届いていない人々のためのリポソームおよびPEG化製剤に焦点を当てた専門知識により、受託製造に取り組んでいます。
リポソームとは何ですか、そしてドラッグデリバリーでどのように使用されますか?
リポソームは、活性医薬品成分(API)の能力を高めるために複数の役割を果たす特殊な送達手段です。 まず、生体膜を模倣することで体内の免疫系による検出を防ぎ、薬物が目的地に到達するまでの時間をより長くすることができます。
リポソームはユニークな小胞構造を有しています。 この小胞は、水相を包む中空球の形状をした脂質二重層で構成されています。 そのため、水性区画(水溶性/親水性の場合)または脂質二重層(脂溶性/親油性の場合)のいずれかにあるリポソーム内に、関心のあるあらゆる積荷を封入することができる。 この2つのカテゴリーの脂質は、親水性/水を好む頭部基と親水性/水を嫌う尾部基を持つという点でユニークである。 これらの分子は両親媒性であるため、水溶液に添加すると自発的に自己集合し、リポソームなどのユニークな3次元構造を形成する。 3次元構造の形状や形態は、脂質組成、温度、pH、水中の他の緩衝剤、塩、糖の存在など、さまざまな異なる要因に左右される。

Image Source: Chem Libre Texts
薬物がリポソーム製剤として処方された場合、どのように身体と相互作用し、使用可能になるのか?
近年、リポソームは薬物送達媒体の信頼できるクラスとして大きく注目されている。 その自己閉鎖型構造は、一度に複数の薬物をカプセル化することができ、封入された貨物を加水分解や破壊から保護します。 さらに、脂質二重層の外殻にタンパク質や表面機能性リガンドをターゲティングすることで、抗体や受容体ターゲティングリガンドを介して、リポソームの細胞内への標的侵入を可能にする新しい機能を付加することができる。 これらのリガンドは、特定の疾患細胞で過剰発現している細胞受容体に付着し、細胞膜を通して薬剤の侵入を可能にします。
「リポソームは、装填した薬剤分子を外部劣化から保護し、生物膜との類似性により、薬剤分子を細胞または細胞内区画に送達する独自の機会を提供します……」。 さらに、リポソームのサイズ、電荷、表面機能リガンドなど様々な物理化学的特性を変えることができ、特定の薬物送達タスクに適した機能性を得ることが可能である。 これらの利点により、リポソームは、臨床において幅広い用途を持つ主要な薬物送達プラットフォームとなっています」
– Liposome-like nanostructures for drug delivery|Gao W, Hu C-MJ, Fang RH, Zhang L 1
一般に、リポソームは血流に送達する無菌注射薬として製造されており、脂質包が壊れると薬剤が放出されます(細胞外環境または細胞内環境で発生しうる)が、このリポソームもまた、血流に送達するために無毒化された注射器です。
従来のリポソームを設計するためにさまざまな戦略が採用されており、刺激反応に基づいてカプセル化されたAPIまたは「カーゴ」をリポソームが放出することによって治療効果を高めるトリガーリリース機能を備えている。 この放出は、リポソームの従来の分解によって引き起こされるか、または熱エネルギー、pH勾配およびシアストレスを含む活性刺激および環境の合図によって引き起こされます1
細胞内環境での放出を目的とした製剤は、リポソーム構造を変更するか酸性区画内で分解してカプセル化薬剤の放出を可能にするpH感受性の脂質を含むことができます。 あるいは、温度変化や特定の波長の光への反応による分解や構造変化を可能にする感温性成分や感光性成分が含まれることもある。
リポソーム様薬物キャリアは多くの異なる種類があり、広範囲の生化学的および生物物理学的特性を示すことができる。 これは有利であり、これらの脂質ベースの粒子が何百もの異なる環境で有用なアプリケーションを想定することを可能にしますが、潜在的なバリエーションの数が、厳格な製造管理を必須にしています2
Exelead は、Abelcet で始まった 1990年代初期から脂質ベースの薬剤を製造しています。 アベルセットの有効成分であるアムホテリシンBは、脂質複合体に保持され、真菌膜と選択的に融合して疾患細胞を標的にします。
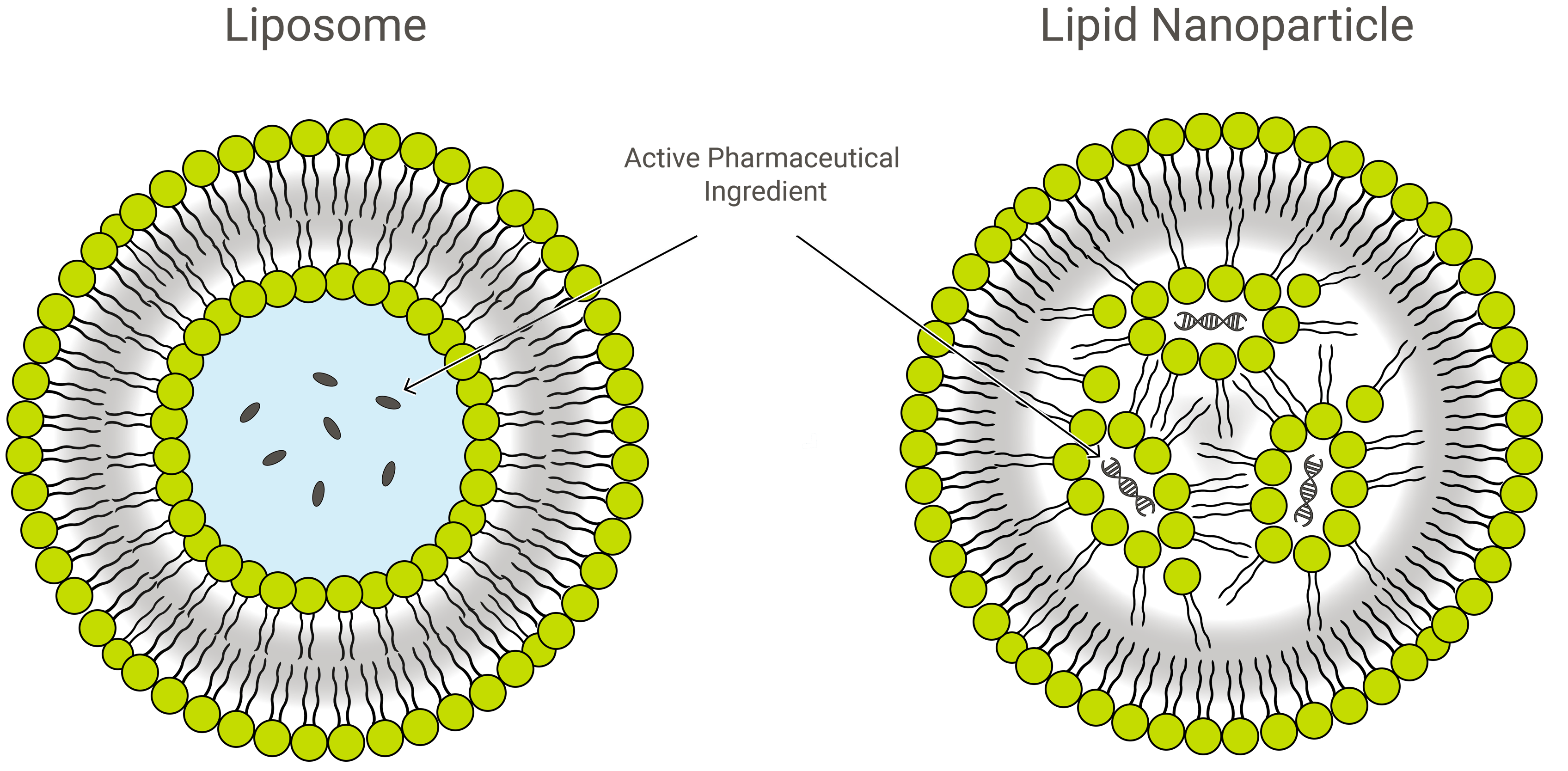
リポソームと脂質ナノ粒子
リポソームと脂質ナノ粒子 (LNP) は設計上似ていますが、組成と機能がわずかに異なっています。 どちらも脂質ナノ製剤であり、優れたドラッグデリバリービークルとして、目的の積荷を脂質の保護外層内で輸送する。 しかし、応用においては、LNPは様々な形態をとることができる。
LNPはリポソーム状の構造で、特に幅広い種類の核酸(RNAおよびDNA)のカプセル化に適しており、そのため、最も人気のある非ウイルス遺伝子送達システムとなっています。 Exeleadは、siRNA、mRNA、saRNAなど、さまざまな種類の遺伝子ペイロードをカプセル化するLNPを開発・製造しています。
従来のリポソームは、水性ポケットを囲む1つまたは複数のリング状の脂質二重層を含みますが、すべてのLNPが脂質小粒子またはリポソームとして認められる連続した二重層を持つわけではありません。 いくつかのLNPはミセル様構造をとり、非水性コアに薬物分子を封入する。
PEGylation of LNPs and liposome-like drug delivery structures
LNP は他の脂質成分と共に主に陽イオン脂質(下記の遺伝子治療を参照)から構成される。 これらは通常、ホスファチジルコリン(PC)クラスに属する中性リン脂質分子や、コレステロールなどのステロールを含む。

PEG化リン脂質は多くの脂質ベースの薬剤キャリアで使用されていますが、その理由は主に、体内で循環する薬剤にステルス効果として知られるものを提供するためです。 人間の免疫システムは、あらゆる異物から体を守ろうとするものであり、薬用ナノ粒子も例外ではない。 送達効率を助け、積荷分子が目的の疾患部位に到達するための循環時間を長くするために、PEG を添加して、血漿タンパク質がリポソーム表面に吸収されるのを防ぐことによってこれらのナノ粒子を保護し、血流循環寿命を長くします1
PEG 化による 2 つ目の利点は、リポソーム様ナノ構造の安定性が向上することです。 従来のリポソーム、特に200 nm以下のサイズのリポソームは、それ自体では不安定であり、表面張力を下げるために互いに融合する傾向がある。 その結果、封入された薬剤が失われたり、異なるベシクルの荷物が不利に混合されたりすることがある。
これらのステルス機能を備えたナノ粒子により、新世代のリポソーム製剤が生まれ、複数の臨床承認製品が生まれました。 PEG化リポソームとLNPは現在、ほとんどのがん治療薬の新しいパラダイムとなっています。
LNPs in gene therapy
長い間、遺伝子ベースの治療薬をヒト細胞に送達する最も効果的な方法は、自己複製する有害遺伝子ではなく、薬用成分を運ぶように改造されたウイルスを使用することでした。 この方法は、現在でも時々使われており、ウイルス遺伝子導入と呼ばれている。 しかし、非ウイルス性遺伝子導入は、安全性が高く、免疫原性副作用の発生率が低く、製造が容易であることから、ここ20年ほどの間に一般的になってきている。 この動きの主な原動力の1つは、脂質およびポリマーベースのキャリアの開発であり、その中でもLNPが最も普及している。
遺伝子を送達するために使用されるLNPは、主に、アニオン、つまり負電荷の核酸と会合するカチオン、つまり正電荷の脂質を使用して合成される。 他の脂質ベースの成分はまた、遺伝子の貨物の送達効率と場所の放出を調整するために追加することができます。 1
無機材料、有機材料、およびハイドロゲルはそれぞれ、殻を形成するさまざまな数の脂質層内にカプセル化されたリポソームナノ粒子のコアとして研究されてきました。 これらのハイブリッドナノ粒子の最も成功したバリエーションの1つは、脂質単層内にPLAまたはPGLAポリマーを組み込んだものである。 これら2つのコアバイオポリマーは、薬物放出の制御を容易にするため、薬物送達に特に有用である1。

上に示したナノ粒子製剤は、疎水性のPGLAコアと親水性の脂質-PEGシェルとの脂質-高分子複合体である。
拡大する分野
「リポソームは、有効な薬物キャリアのクラスとなるまで長い道のりを歩んできました…リポソーム様のナノ構造はますます多様化しており、それぞれが特定の薬物送達タスクに適した独自の強度を備えています」(同)。 一方、これらのナノ構造体と生体システムとの相互作用の理解も急速に進んでいる。 循環時間、組織への蓄積、潜在的な毒性に関する相当量の情報が得られている。 リポソーム様ナノキャリアは、近い将来、ドラッグデリバリーにより大きな役割を果たすことは間違いありません」
– ドラッグデリバリーのためのリポソーム様ナノ構造|Gao W, Hu C-MJ, Fang RH, Zhang L 1
放出制御、ナノ区画化薬物の開発において大きな研究が行われていますが、リポソームとLNPは特に有望なオプションといえます。 これらの構造は、ナノ医薬品のためのユニークな、自然に安定した、細胞のような形態を提供し、より高度な治療戦略に向けて進歩する態勢を整えています。
1960年代後半にリポソームが薬物送達システムとして最初に提案されて以来、構造と機能のバリエーションが生まれ、疾患ターゲティングの面で貴重な進歩をもたらしています。 LNP医薬品は、抗がん剤、抗生物質、遺伝子治療薬、麻酔薬、抗炎症薬などを送達するために設計された治療法として、製薬業界全体に現れている3。
「臨床応用において、リポソーム薬剤は、その平均直径が超濾過可能範囲(直径<200 nm)である場合に、血管透過性が増大する部位に「受動的に」集積する能力、およびカプセル化した薬剤の副作用を遊離薬剤に比べて低減する能力が最も有用であると証明されている。 その結果、毒性よりも有効性を評価するTherapeutic Indexが全体的に向上しています。「
– Liposomal drug delivery systems: from concept to clinical applications|アレン TM、カリス PR 3
Applications in personalized medicine-a new era in therapeutic strategies
病気の治療に対する従来の大手製薬会社のアプローチとは異なり、個別医療では患者の遺伝学を含むライフスタイル、環境、生物学における個人差を考慮に入れて治療します。 4
個別化遺伝子治療の出現により、医師や科学者は、医薬品の有効成分(多くの場合、RNAやDNA)を特定の患者や患者グループの特定の疾患プロファイルに合わせて効果的に調整することができるようになりました。
LNPs as delivery vehicles for oligonucleotides
個別化医療の成長分野の多くが遺伝子治療に焦点を当てているため、LNPは薬剤送達プラットフォームとして特に有用になってきています。 理論的には、どんなオリゴヌクレオチドもリポソームやLNPの中に封入することができますが、siRNAは現在、この種の薬物製品で最も一般的なカーゴとなっています。 残念ながら、カプセル化されていない無料のRNAをヒトの細胞に送達することは困難であり、それらは大きく、血清中で不安定であり、ヌクレアーゼ分解を受けやすいからです5
研究者はホスホロチオエート結合を加えることによって血清中のsiRNAを安定化する試みを行ってきましたが、ヒトで効果的に遺伝子を沈黙させるには高い用量が必要とされます。 LNPは、柔軟で容易なカプセル化の手段を提供し、意図した目的地に到達するまでsiRNAセグメントを保護し、標的細胞への送達を容易にすることによって、この問題に対する解決策を提供しました5
「イオン化可能なカチオン性脂質を含むLNPは、小さなサイズ、血清安定性、生理的pHでの低い表面ゼータ電位、酸性pH値(たとえば、エンドソーム)でのカチオン性荷電など、ポリ核酸の全身送達に必要な多くの特徴を持っている」(同)。 さらに、投与後のApoEとの結合による「内因性」ターゲティングプロセスを利用することで、i.v.投与後に高効率で肝細胞に取り込まれ、優れた遺伝子サイレンシング能力を発揮することが可能である。”
– Liipid nanoparticle delivery systems for siRNA-basedrapeutics|Wan C, Allen TM, Cullis PR 5
Smaller batch sizes
個人向け医薬品はしばしば単一患者または少人数向けに小さなバッチサイズで製造され、しばしば1リットル未満の製品になることがあります。 対照的に、主流の医薬品の従来の製造バッチでは、数千リットルの医薬品が大規模に生産されることがよくあります。
個別化医療が医薬品開発で注目されるようになるにつれ、医薬品製造業界の多くの企業が、従来の大規模な医薬品製造に加え、少人数の患者を対象とする少量バッチに対応するためにパイプラインを適応させています。 患者または抗原特異的な医薬品は、オリゴヌクレオチドが配列決定されてから、私たちのサイトで製品を調合する必要があるまで、それほど時間がかかりません。 このような短期間の予測、ときにはわずか6週間という課題は、既存のシステムを改良し、革新的な製剤技術を取り入れることによって克服することができました。
広範な応用
個別化医療はほとんどすべての疾患を治療できる可能性を秘めていますが、現在の研究は主に1)免疫療法、2)ゲノム薬理学によって強化された従来の療法、3)バイオマーカー関連のがん治療法に焦点を当てています。 リポソームとLNPは、これら各カテゴリーの薬剤の送達手段として応用されており、この新しい医薬品開発分野において不可欠な資産となっています。

参考文献
- Gao W, Hu C-MJ, Fang RH, Zhang L. L. Liposome-like Nanostructures for Drug Delivery. また、「震災復興に向けた取り組み」の一環として、「震災復興支援プロジェクト」を立ち上げました。 2013;1(48):10.1039/C3TB21238F. doi:10.1039/C3TB21238F.
- Kraft JC, Freeling JP, Wang Z, Ho RJY. リポソームと脂質ナノ粒子薬物送達システムの新たな研究・臨床開発動向. ジャーナル オブ ファーマシューティカル サイエンス. 2014;103(1):29-52. doi:10.1002/jps.23773.
- テレサ・M・アレン、ピーテル・R・カリス. リポソーム薬物送達システム。 コンセプトから臨床応用まで。 アドバンスト・ドラッグ・デリバリー・レビュー。 2013 Jan;65(1):36-48
- Esposito L. What Does Personalized Medicine Really Mean? USニュース ヘルスケア. 2018 Jan;
- Wan C, Allen TM, Cullis PR. siRNAベースの治療薬のための脂質ナノ粒子送達システム。 Drug Deliv Transl Res. 2014 Feb;4(1):74-83. doi: 10.1007/s13346-013-0161-z.
- Vogenberg FR, Isaacson Barash C, Pursel M. Personalized Medicine.の項参照。 第1部:セラノスティックスへの進化と発展. Pharmacy and Therapeutics. 2010;35(10):560-576.