Redactor șef: C. Michael Gibson, M.S., M.D. ; Editor(i)-șef asociat(i): C. Michael Gibson, M.S., M.D. ; Editor(i)-șef asociat(i): C. Michael Gibson, M.S., M.D: Aparna Vuppala, M.B.B.S.
Disclaimer
WikiDoc NU OFERĂ NICI O GARANȚIE DE VALIDITATE. WikiDoc nu este un furnizor profesionist de asistență medicală și nici nu este un înlocuitor adecvat pentru un furnizor de asistență medicală autorizat. WikiDoc se dorește a fi un instrument educațional, nu un instrument pentru orice formă de furnizare de asistență medicală. Conținutul educațional de pe paginile de medicamente WikiDoc se bazează pe prospectul FDA, pe conținutul Bibliotecii Naționale de Medicină și pe ghidurile de practică / declarațiile de consens. WikiDoc nu promovează administrarea niciunui medicament sau dispozitiv care nu este în concordanță cu etichetarea acestuia. Vă rugăm să citiți aici declarația noastră completă de declinare a responsabilității.
Vizualizare generală
Butalbitalul este o combinație care este aprobată de FDA pentru tratamentul pentru ameliorarea complexului de simptome al cefaleei de tensiune (sau de contracție musculară). Reacțiile adverse frecvente includ amețeală și tulburări gastrointestinale, inclusiv greață, vărsături și flatulență, necroliză epidermică toxică și eritem multiform.
Indicații și doze pentru adulți
Indicații și doze etichetate de FDA (adulți)
Durere de cap
- Comprimatele de butalbital, aspirină și cofeină sunt indicate pentru ameliorarea complexului simptomatic al cefaleei de tensiune (sau de contracție musculară).
- Nu sunt disponibile dovezi care să susțină eficacitatea și siguranța butalbitalului, aspirinei și cafeinei în tratamentul multiplelor cefalee recurente. Este necesară prudență în această privință deoarece butalbitalul creează dependență și este potențial abuzabil.
Utilizare și dozare off-Label (adulți)
Utilizare susținută de ghiduri
Există informații limitate privind utilizarea off-Label susținută de ghiduri a butalbitalului la pacienții adulți.
Utilizare neacoperită de ghid
Există informații limitate cu privire la utilizarea off-Label neacoperită de ghid a Butalbitalului la pacienții adulți.
Indicații și doze pediatrice
Indicații și doze (pediatrice)
Există informații limitate cu privire la utilizarea Butalbitalului la pacienții pediatrici.
Utilizare și dozare în afara indicațiilor de pe eticheta (pediatrică)
Utilizare susținută de ghid
Există informații limitate privind utilizarea în afara indicațiilor de pe eticheta susținută de ghid a Butalbitalului la pacienții pediatrici.
Utilizare neacoperită de ghid
Există informații limitate privind utilizarea off-Label neacoperită de ghid a Butalbitalului la pacienții pediatrici.
Contraindicații
- Hipersensibilitate la aspirină, cafeină sau barbiturice. Pacienți cu porfirie.
Atenționări
Droguri dependente:
- Utilizarea prelungită a barbituricelor poate produce dependență medicamentoasă, caracterizată prin dependență psihică și, mai puțin frecvent, dependență fizică și toleranță. Responsabilitatea de abuz a butalbitalului, aspirinei și cafeinei este similară cu cea a altor combinații de medicamente care conțin barbiturice. Trebuie să se manifeste prudență atunci când se prescriu medicamente pentru pacienții cu o înclinație cunoscută de a lua cantități excesive de medicamente, ceea ce nu este neobișnuit la pacienții cu cefalee tensională cronică.
Utilizarea la pacienții ambulatoriali:
- Butalbitalul, aspirina și cafeina pot afecta abilitățile mentale și/sau fizice necesare pentru îndeplinirea unor sarcini potențial periculoase, cum ar fi conducerea unui autovehicul sau operarea mașinilor. Pacientul trebuie avertizat în consecință. Efectele deprimante asupra sistemului nervos central ale butalbitalului pot fi aditive cu cele ale altor deprimante ale SNC. Trebuie evitată utilizarea concomitentă cu alte sedative-hipnotice sau cu alcool. Atunci când este necesară o astfel de terapie combinată, poate fi necesară reducerea dozei unuia sau mai multor agenți.
Precauții
- Salicilații trebuie utilizați cu extremă precauție în prezența ulcerului peptic sau a anomaliilor de coagulare.
Reacții adverse
Experiența studiilor clinice
- Cele mai frecvente reacții adverse sunt somnolența și amețelile. Reacțiile adverse mai puțin frecvente sunt amețeală și tulburări gastrointestinale, inclusiv greață, vărsături și flatulență. O singură incidență de suprimare a măduvei osoase a fost raportată la utilizarea de butalbital, aspirină și cafeină. Au fost raportate mai multe cazuri de reacții dermatologice, inclusiv necroliză epidermică toxică și eritem multiform.
Experiență după punerea pe piață
Există informații limitate cu privire la Experiența după punerea pe piață a butalbitalului în eticheta medicamentului.
Interacțiuni medicamentoase
Există informații limitate cu privire la Interacțiuni medicamentoase ale Butalbitalului în eticheta medicamentului.
Utilizare la populații specifice
Sarcina
Categoria de gravide (FDA): C
- Nu au fost efectuate studii adecvate la animale pentru a determina dacă acest medicament afectează fertilitatea la masculi sau femele, are potențial teratogen sau are alte efecte adverse asupra fătului. Deși nu există studii bine controlate la femeile gravide, cei peste douăzeci de ani de experiență clinică și de comercializare nu includ nicio dovadă pozitivă a efectelor adverse asupra fătului. Deși nu există un risc clar definit, această experiență nu poate exclude posibilitatea unor daune rare sau subtile asupra fătului uman. Butalbitalul, aspirina și cafeina trebuie utilizate la femeile gravide numai atunci când este în mod clar necesar.
Categoria de sarcină (AUS): Nu există un ghid al Comitetului Australian de Evaluare a Medicamentelor (Australian Drug Evaluation Committee – ADEC) privind utilizarea Butalbitalului la femeile însărcinate.
Lucru și naștere
Nu există un ghid al FDA privind utilizarea Butalbitalului în timpul travaliului și nașterii.
Mamele care alăptează
- Nu sunt cunoscute efectele Butalbitalului, aspirinei și cafeinei asupra sugarilor mamelor care alăptează. Salicilații și barbituricele sunt excretate în laptele matern al mamelor care alăptează. Se consideră că nivelurile serice la sugari sunt nesemnificative în cazul dozelor terapeutice.
Utilizare pediatrică
- Siguranța și eficacitatea la pacienții pediatrici cu vârsta sub 12 ani nu au fost stabilite.
Utilizare în geriatrie
Nu există niciun ghid al FDA privind utilizarea Butalbitalului în ceea ce privește pacienții geriatrici.
Gender
Nu există niciun ghid al FDA privind utilizarea Butalbitalului în ceea ce privește populațiile specifice de gen.
Rasă
Nu există niciun ghid al FDA privind utilizarea Butalbitalului în ceea ce privește populațiile rasiale specifice.
Insuficiență renală
Nu există niciun ghid al FDA privind utilizarea Butalbitalului la pacienții cu insuficiență renală.
Insuficiență hepatică
Nu există niciun ghid al FDA privind utilizarea Butalbitalului la pacienții cu insuficiență hepatică.
Femeile cu potențial reproductiv și bărbații
Nu există niciun ghid al FDA privind utilizarea Butalbitalului la femeile cu potențial reproductiv și la bărbați.
Pacienți imunocompromiși
Nu există niciun ghid al FDA privind utilizarea Butalbitalului la pacienții care sunt imunocompromiși.
Administrare și monitorizare
Administrare
- Orală
Monitorizare
Există informații limitate privind monitorizarea Butalbitalului în eticheta medicamentului.
Compatibilitate IV
Există informații limitate cu privire la Compatibilitatea IV a Butalbitalului în eticheta medicamentului.
Supradozaj
- Efectele toxice ale supradozajului acut de butalbital, aspirină și cafeină sunt atribuite în principal componentei sale barbiturice și, într-o măsură mai mică, aspirinei. Deoarece efectele toxice ale cafeinei apar numai în doze foarte mari, este puțin probabilă posibilitatea unei toxicități semnificative a cafeinei în urma supradozajului de butalbital, aspirină și cafeină. Simptomele atribuibile intoxicației acute cu barbiturice includ somnolență, confuzie și comă; depresie respiratorie; hipotensiune; șoc. Simptomele atribuibile intoxicației acute cu aspirină includ hiperpnee; tulburări acido-bazice cu dezvoltarea acidozei metabolice; vărsături și dureri abdominale; tinitus; hipertermie; hipoprotrombinemie; agitație; delir; convulsii. Intoxicația acută cu cafeină poate provoca insomnie, agitație, tremor și delir; tahicardie și extrasistole. Tratamentul constă în primul rând în gestionarea intoxicației cu barbiturice și în corectarea dezechilibrului acido-bazic datorat salicilismului. Vărsăturile trebuie să fie induse mecanic sau cu emetice la pacientul conștient. Se poate folosi lavajul gastric dacă reflexele faringiene și laringiene sunt prezente și dacă au trecut mai puțin de 4 ore de la ingestie. Trebuie introdus un tub endotraheal cu manșetă înainte de lavajul gastric al pacientului inconștient și atunci când este necesar pentru a asigura respirația asistată. Diureza, alcalinizarea urinei și corectarea tulburărilor electrolitice trebuie să se realizeze prin administrarea de lichide intravenoase, cum ar fi bicarbonat de sodiu 1% în dextroză 5% în apă. Trebuie acordată o atenție meticuloasă menținerii unei ventilații pulmonare adecvate. Corectarea hipotensiunii poate necesita administrarea de bitartrat de levartherenol sau clorhidrat de fenilefrină prin perfuzie intravenoasă . În cazurile severe de intoxicație, dializa peritoneală, hemodializa sau transfuzia de schimb pot fi salvatoare de vieți. Hipoprotrombinemia trebuie tratată cu vitamina K, pe cale intravenoasă.
Există informații limitate cu privire la Supradozaj cronic de Butalbital în eticheta medicamentului.
Farmacologie
Există informații limitate cu privire la Farmacologia Butalbitalului în eticheta medicamentului.
Mecanism de acțiune
- Farmacologic, butalbital, aspirină și cafeină combină proprietățile analgezice ale aspirinei cu proprietățile anxiolitice și de relaxare musculară ale butalbitalului.
Eficacitatea clinică a butalbitalului, aspirinei și cafeinei în cefaleea tensională a fost stabilită în studii dublu-orb, controlate cu placebo, multiclinice. Un studiu cu design factorial a comparat butalbitalul, aspirina și cafeina cu fiecare dintre componentele sale principale. Acest studiu a demonstrat că fiecare componentă contribuie la eficacitatea butalbitalului, aspirinei și cafeinei în tratamentul simptomelor țintă ale cefaleei tensionale (durere de cap, tensiune psihică și contracție musculară în regiunea capului, gâtului și umerilor). Pentru fiecare simptom și pentru complexul de simptome în ansamblu, s-a demonstrat că butalbitalul, aspirina și cofeina au avut efecte clinice semnificativ superioare față de oricare dintre componente luate separat.
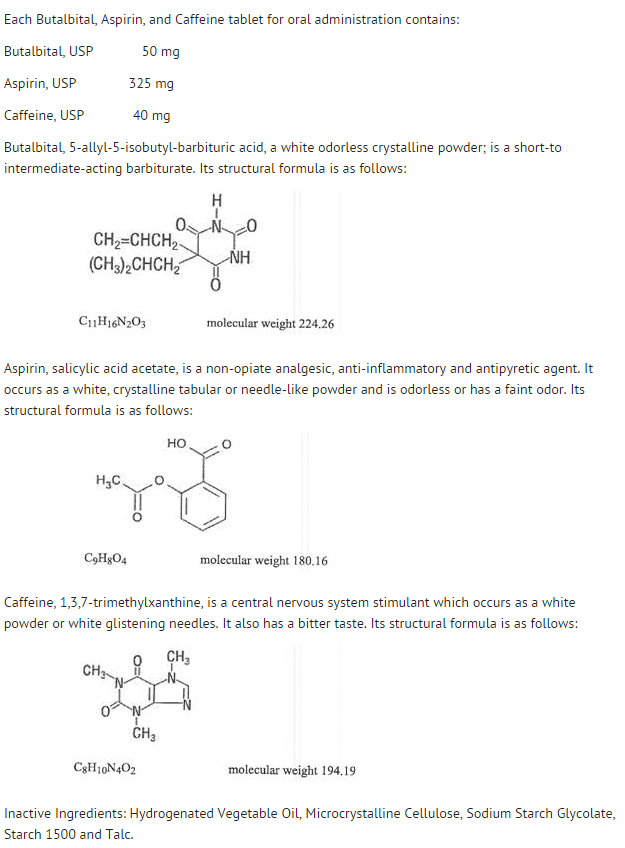
Structura
- Comportamentul componentelor individuale este descris mai jos.
- Disponibilitatea sistemică a aspirinei după o doză orală este foarte dependentă de forma de dozare, de prezența alimentelor, de timpul de golire gastrică, de pH-ul gastric, de antiacide, de agenții tampon și de mărimea particulelor. Acești factori afectează nu neapărat gradul de absorbție a salicilaților totali, ci mai mult stabilitatea aspirinei înainte de absorbție.
- În timpul procesului de absorbție și după absorbție, aspirina se hidrolizează în principal în acid salicilic și se distribuie în toate țesuturile și fluidele organismului, inclusiv în țesuturile fetale, laptele matern și sistemul nervos central (SNC). Cele mai mari concentrații se găsesc în plasmă, ficat, cortex renal, inimă și plămâni. În plasmă, aproximativ 50%-80% din acidul salicilic și metaboliții săi sunt slab legați de proteinele plasmatice.
- Limbajul salicilaților totali este supus unei cinetici saturabile; cu toate acestea, cinetica de eliminare de ordinul întâi este încă o bună aproximare pentru doze de până la 650 mg. Timpul de înjumătățire plasmatică pentru aspirină este de aproximativ 12 minute, iar pentru acidul salicilic și/sau salicilații totali este de aproximativ 3,0 ore.
- Eliminarea dozelor terapeutice se face prin rinichi, fie sub formă de acid salicilic, fie sub formă de alți produși de biotransformare. Clearance-ul renal este mult mărit de o urină alcalină așa cum este produsă de administrarea concomitentă de bicarbonat de sodiu sau citrat de potasiu.
- Biotransformarea aspirinei are loc în principal în hepatocite. Principalii metaboliți sunt acidul saliciluric (75%), fenolicele și glucuronidele de acil ale salicilatului (15%) și acidul gentisic și gentisuric (1%). Biodisponibilitatea componentei de aspirină butalbital, aspirină și cafeină este echivalentă cu cea a unei soluții, cu excepția unei viteze de absorbție mai lente. O concentrație maximă de 8,80 mcg/mL a fost obținută la 40 de minute după o doză de 650 mg.
- Butalbitalul este bine absorbit din tractul gastrointestinal și este de așteptat să se distribuie în majoritatea țesuturilor din organism. Barbituricele, în general, pot apărea în laptele matern și traversează cu ușurință bariera placentară. Ei sunt legați de proteinele plasmatice și tisulare într-un grad variabil, iar legarea crește direct în funcție de solubilitatea lipidică.
- Eliminarea butalbitalului se face în principal prin rinichi (59%-88% din doză) sub formă de medicament neschimbat sau metaboliți. Timpul de înjumătățire plasmatică este de aproximativ 35 de ore. Produsele de excreție urinară au inclus medicamentul de bază (aproximativ 3,6% din doză), acidul 5-izobutil-5-(2,3-dihidroxipropil) barbituric (aproximativ 24% din doză), acidul 5-allyl-5(3-hidroxi-2-metil-1-propil) barbituric (aproximativ 4,8% din doză), produse cu inelul acidului barbituric hidrolizat cu excreție de uree (aproximativ 14% din doză), precum și materiale neidentificate. Din materialul excretat în urină, 32% a fost conjugat.
- Biodisponibilitatea componentei butalbital din butalbital, aspirină și cafeină este echivalentă cu cea a unei soluții, cu excepția unei scăderi a vitezei de absorbție. O concentrație maximă de 2020 ng/mL este obținută la aproximativ 1,5 ore după o doză de 100 mg.
- Legătura in vitro a butalbitalului la proteinele plasmatice este de 45% în intervalul de concentrație de la 0,5 la 20 mcg/mL. Aceasta se încadrează în intervalul de legare a proteinelor plasmatice (20% până la 45%) raportat cu alte barbiturice, cum ar fi fenobarbitalul, pentobarbitalul și secobarbitalul de sodiu. Raportul dintre concentrația plasmatică și cea sanguină a fost aproape unitar, ceea ce indică faptul că nu există o distribuție preferențială a butalbitalului nici în plasmă, nici în celulele sanguine. (pentru informații privind toxicitatea, a se vedea secțiunea SUPradozaj).
- Cafeina, ca majoritatea xantinelor, este rapid absorbită și distribuită în toate țesuturile și fluidele corpului, inclusiv în SNC, țesuturile fetale și laptele matern.
- Cafeina este eliminată rapid prin metabolizare și excreție în urină. Timpul de înjumătățire plasmatică este de aproximativ 3,0 ore. Biotransformarea hepatică înainte de excreție are ca rezultat cantități aproximativ egale de 1-metil-xantină și acid 1-metiluric. Din cele 70% din doza care a fost recuperată în urină, doar 3% a fost medicament neschimbat.
- Biodisponibilitatea componentei cafeină pentru butalbital, aspirină și cafeină este echivalentă cu cea a unei soluții, cu excepția unui timp ușor mai lung până la vârf. O concentrație maximă de 1660 ng/mL a fost obținută în mai puțin de o oră pentru o doză de 80 mg
- Butalbital, Aspirină și Cafeină Tablete, USP 50 mg/325 mg/40 mg sunt comprimate albe, rotunde, nesubtitrate, imprimate „West-ward 785”.
- Să se păstreze la 20-25oC (68-77oF) . Protejați de lumină și umiditate.
- Dispuneți într-un recipient etanș, rezistent la lumină, așa cum este definit în USP, folosind un sistem de închidere de siguranță pentru copii.
- Interacțiunea alcool-Butalbital nu a fost stabilită. Discutați cu medicul dumneavoastră despre efectele administrării de alcool împreună cu acest medicament.
Farmacodinamică
Există informații limitate cu privire la Farmacodinamica Butalbitalului în eticheta medicamentului.
Farmacocinetică
Aspirină:
Butalbital:
Cafeina:
Toxicologie nonclinică
Există informații limitate cu privire la Toxicologia nonclinică a butalbitalului în eticheta medicamentului.
Studii clinice
Există informații limitate cu privire la Studiile clinice ale butalbitalului în eticheta medicamentului.
Cum se eliberează
Foarte de 30 comprimateFoarte de 50 comprimateFoarte de 100 comprimateFoarte de 500 comprimateFoarte de 1000 comprimateCăsuțe cu doze unitare de 100 comprimate
Stocare
Există informații limitate cu privire la Stocarea Butalbitalului în eticheta medicamentului.
Imagini
Imagini de medicamente
Denumirea medicamentului: Butalbital, paracetamol și cafeină
Ingredient(e): BUTALBITAL, ACETAMINOPHEN, CAFEINĂ
Imprimare: West;ward;787
Dosare: 50 mg
Culoare(e): Albastru
Forma: Rotundă
Dimensiuni (mm): 11
Scotare: 1
NDC:01431787
Autorul etichetei medicamentului: West-Ward Pharmaceutical Corp
Această imagine de pastilă este furnizată de PillBox al Bibliotecii Naționale de Medicină.
Denumire medicament: Butalbital, Aspirină și Cofeină
Ingredient(e): BUTALBITAL, ASPIRINĂ, CAFEINĂ
Imprimare: Westward;785
Dosare: 50 mg
Culoare(e): Alb
Forma: Rotundă
Dimensiuni (mm): 11
Scotare: 1
NDC:01431785
Autorul etichetei medicamentului: West-ward Pharmaceutical Corp
Această imagine de pastilă este furnizată de PillBox al Bibliotecii Naționale de Medicină.

Denumirea medicamentului: Butalbital, Aspirină și Cofeină
Ingredient(e): BUTALBITAL, ASPIRINĂ, CAFEINĂ
Imprimare: WATSON;3219
Dosage: 50 mg
Culoare(e): Verde, Galben
Forma: Capsulă
Dimensiune (mm): 22
Scotare: 1
NDC:05913219
Etichetă medicament Autor: AICI: Watson Laboratories, Inc.
Această imagine de pastilă este furnizată de PillBox al Bibliotecii Naționale de Medicină.
Denumirea medicamentului: Tablete de butalbital, aspirină și cafeină
Ingredient(e): ASPIRIN, BUTALBITAL, CAFEINĂ
Imprimare: Vest;Ward;785
Dosare: 50 mg
Culoare(e): Alb
Forma: Rotundă
Dimensiuni (mm): 7
Scotare: 1
NDC:06032548
Autorul etichetei medicamentului: Qualitest
Această imagine a pilulei este furnizată de PillBox al Bibliotecii Naționale de Medicină.
Panou de afișare a ambalajelor și etichetelor
Această imagine a etichetei FDA este furnizată de Biblioteca Națională de Medicină.

Această imagine a etichetei FDA este furnizată de National Library of Medicine.
Informații privind consilierea pacienților
Există informații limitate cu privire la informațiile privind consilierea pacienților despre Butalbital în eticheta medicamentului.
Precauții cu alcoolul
Nume de marcă
Există informații limitate privind numele de marcă ale Butalbitalului în eticheta medicamentului.
Nume de medicamente asemănătoare
Există informații limitate privind numele de medicamente asemănătoare ale Butalbitalului în eticheta medicamentului.
Starea de penurie a medicamentului
.