Spațiul interpalpebral al conjunctivei dezvoltă frecvent modificări tisulare neregulate care sunt, de cele mai multe ori, minim patologice sau deloc patologice. Această localizare este expusă la radiațiile ultraviolete (UV) și la iritanții atmosferici și este susceptibilă la uscăciune; astfel, leziuni precum pingueculae și pterigia sunt neregularități ale suprafeței oculare frecvent întâlnite și, în general, atrag o atenție minimă la examinare.
Boala neoplazică scuamoasă, totuși, este ocazional întâlnită. Carcinomul scuamos conjunctival invaziv cu celule scuamoase este adesea precedat histologic de neoplasmul intraepitelial conjunctival (CIN), care reprezintă cea mai frecvent întâlnită creștere neoplazică conjunctivală. Aceste leziuni – adesea diagnosticate greșit ca fiind creșteri mai tipice ale suprafeței oculare – sunt lent progresive, invazive la nivel local și nu au potențial metastatic. Cu toate acestea, ele pot provoca ocazional leziuni locale semnificative ale suprafeței oculare și pot evolua spre carcinomul cu celule scuamoase, mai invaziv. Atât diagnosticul, cât și tratamentul CIN pot fi o provocare. Acest articol oferă informații pentru medicii oftalmologi care s-ar putea să nu se întâlnească prea des cu CIN și care ar dori o privire de ansamblu clinică.
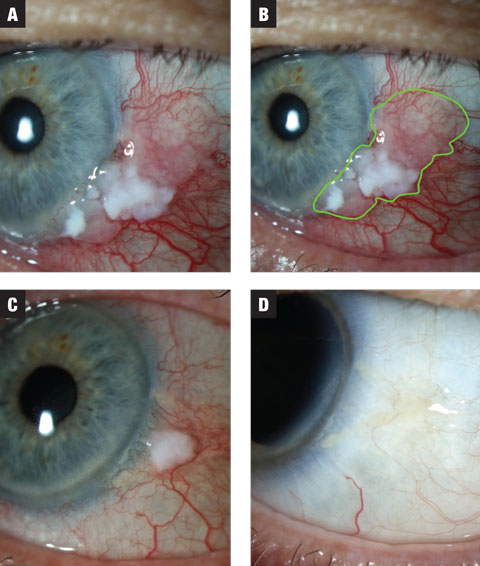
Fig. 1a. În cazul 1, leziunea prezintă atât zone leucoplacice, cât și zone gelatinoase. Tratamentul a fost inițiat cu MMC 0,02% QID. Fig. 1b. Întinderea estimată a leziunii evidențiate. Fig. 1c. După primul tratament de trei săptămâni, leziunea prezintă o reducere dramatică a dimensiunii. Pacientul a fost plasat într-o perioadă de spălare de două săptămâni și a fost instruit să anticipeze o a doua cură de MMC. Fig. 1d. Leziunea a prezentat o rezoluție completă după spălare. Faceți clic pe imagine pentru a o mări.
Dezvoltarea CIN
Geneza unei populații de celule canceroase epiteliale, sau carcinom, necesită o serie de modificări ale comportamentului celulelor. Celulele care prezintă această displazie prezintă o creștere și o maturare dezorganizată, rezultând o supraabundență de celule imature care este contrastată de o sărăcie relativă concomitentă de celule mature din această linie. În timp ce displazia este un proces reversibil, celulele displazice pot suferi apoi mutații suplimentare, ceea ce duce la o transformare neoplazică, prin care celulele devin insensibile la inhibitorii de creștere și devin invazive.
Carcinoamele neoplazice pot fi limitate local de membrana bazală – cunoscut sub numele de carcinom in situ – sau pot fi invazive, caracterizate prin faptul că leziunea străpunge membrana bazală respectivă și se răspândește local. Cu toate acestea, această stadializare nu se referă la două entități separate; mai degrabă, carcinomul in situ reprezintă o etapă preliminară de-a lungul aceluiași continuum al neoplaziei. Dacă este lăsat singur, carcinomul in situ poate deveni în cele din urmă invaziv.
În timp ce este posibil ca carcinomul scuamos să sară peste etapa de CIN, aceasta reprezintă frecvent punctul intermediar în etiologia bolii. CIN este o linie anormală de celule epiteliale conjunctivale (și, eventual, corneene) și reprezintă fie o displazie simplă (grosime parțială a țesutului epitelial), fie un carcinom in situ atunci când leziunea este de grosime totală.1-4 CIN face parte din spectrul de afecțiuni neoplazice ale conjunctivei și corneei cunoscute colectiv sub denumirea de neoplazie scuamoasă de suprafață oculară (OSSN). Dacă CIN devine invazivă prin străpungerea membranei bazale, aceasta este reclasificată ca carcinom cu celule scuamoase invaziv (SCC).
Deși neobișnuită, CIN este cel mai frecvent întâlnit neoplasm conjunctival în Statele Unite ale Americii.4 Factorii de risc pentru dezvoltarea CIN și a tuturor formelor de OSSN sunt expunerea la UV (în special UV-B), sexul masculin, expunerea la produse petroliere, fumul de tutun intens, virusul imunodeficienței umane (HIV) și virusul papiloma uman (HPV) tip 16, deși acest ultim risc rămâne controversat.1,3-5 Prognosticul CIN este de obicei bun, cu excepția cazurilor în care creșterea este neobișnuit de mare. Odată ce leziunea rupe membrana bazală și devine invazivă, prognosticul este mai rău și necesită adesea un tratament agresiv, cum ar fi enuclearea sau extenuarea. Chiar și în aceste cazuri, riscul de metastaze la distanță este scăzut.
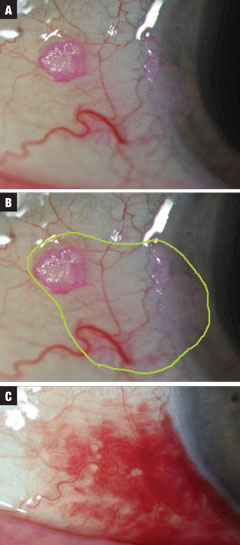
Fig. 2a-c (de sus în jos). Cazul 2 a implicat o mică leziune suspectă de CIN descoperită întâmplător la examinare. Tratamentul a fost inițiat cu INF-a2b QID până când flaconul de 10 ml a fost golit. Întinderea totală estimată a marginilor neoplazice este evidențiată cu verde. În cele din urmă, s-a observat o rezoluție, cu SCH concomitent legată de valsalva (nu indusă de medicamente). Tratamentul a necesitat o lună la un milion de UI QID și apoi 10 zile QID la trei milioane de UI de INF-a2b. Faceți clic pe imagine pentru a o mări.
Prezentare clinică
Aspectul clinic al CIN este acela al unei mase cărnoase anormale, ușor ridicate, localizate de obicei în zona limbală interpalpebrală (95% din toate leziunile).6 Predilecția pentru această zonă se datorează probabil caracteristicilor sale. Expunerea la UV-B este cea mai mare în zona interpalpebrală, iar zona celulelor stem din limbus este un spațiu de tranziție între epiteliul cornean și cel conjunctival. Această zonă de tranziție conferă probabil un risc special pentru țesut de a suferi displazie.
Leziunile conjunctivale pot fi gelatinoase, papilare sau, mai rar, leucoplacice, care apar ca urmare a hiperkeratozei. Aceste leziuni sunt, de obicei, bine definite și vor prezenta un anumit grad de vascularizație feeder.3,7,8 Nouăzeci și cinci la sută din cazuri vor implica limbul.6 Manifestările corneene prezintă o albire similară și pot prezenta proiecții epiteliale gri, fimbriate (adică asemănătoare unor degete) dinspre limbus. În mod clasic, leziunile vor prezenta colorație pozitivă sau punctiformă cu roz bengal, care poate fi utilă în diferențierea clinică a CIN de alte leziuni conjunctivale.8,9
În ciuda constatărilor relativ proeminente pe hârtie, leziunile CIN și SCC pot fi dificil de diferențiat de creșterile mai normale ale conjunctivei, cum ar fi pingueculae, pterygia și nevi. Acest lucru poate duce la un diagnostic greșit în până la 60% din cazuri, chiar și atunci când sunt evaluate de clinicieni experimentați – ceea ce face ca biopsia cu evaluare histologică să fie potențial valoroasă.3
Testări de diagnosticare
În mod istoric, testarea a inclus biopsia excizională efectuată în momentul îndepărtării chirurgicale. Cu toate acestea, medicii folosesc în prezent chimioterapia ca modalitate principală de tratament, ceea ce poate limita accesul pentru biopsie.
Un instrument de diagnostic mai nou este citologia de amprentă, care se realizează prin aplicarea unei hârtii de filtru pe leziune, îndepărtând epiteliul superficial și permițând studii histologice minim invazive. Aceasta este sensibilă în proporție de aproximativ 80%, deși falsurile negative rămân punctul său slab, deoarece hârtia colectoare poate fi împiedicată de keratoza excesivă a leziunii; încercările repetate sunt, în general, mai reușite.8 Un studiu arată că OCT de rezoluție ultra-înaltă, deși nu este disponibil în prezent, este foarte sensibil în diferențierea OSSN și a pterigionului pe baza grosimii epiteliale a leziunii.10
Tratament
Tratamentul tradițional al CIN este excizia cu margini de 1 mm până la 5 mm, în funcție de amploarea și istoricul leziunilor primare și recurente. Afectarea corneei este debridată cu o lamă chirurgicală, iar crioterapia este aplicată pe pat și pe marginile conjunctivale. Sclera este lăsată goală. De obicei, acest procedeu are succes, dar recidivele sunt raportate între 10% și 52%, în funcție de rata de margini chirurgicale clare, așa cum este determinată de histologia postoperatorie.6-11 Rata scade la 5% dacă se obțin margini clare; din păcate, studiile arată că este dificil de garantat existența unor margini clare.8,9 Aceste cifre par să susțină utilizarea unor margini cât mai largi posibil; cu toate acestea, există consecințe ale exciziei conjunctivale extinse: modificări cicatriciale, deficit de celule stem limbale, topire sclerală, perturbări semnificative ale filmului lacrimal și modificări neregulate ale astigmatismului cornean.
Opțiuni topice
Mai recent, chimioterapicele topice au devenit populare pentru a gestiona CIN, deoarece au avantajul de a trata întreaga suprafață oculară și, atunci când sunt utilizate judicios, par a fi bine tolerate.
Mitomicina. Descoperite în anii 1950, mitomicinele sunt produse secundare de fermentare ale Streptomyces caespitosus. Mitomicina-C (MMC), ultima dintre aceste molecule descoperite, este un antimetabolit utilizat în afara îngrijirii oftalmologice ca agent de chimioterapie antitumorală.12,13 MMC acționează ca un agent alchilant care previne scindarea ADN-ului în timpul mitozei celulare, o alterare extrem de toxică.1 Chiar și una dintre aceste legături încrucișate poate fi fatală pentru o celulă.13 În plus, MMC poate genera specii reactive de oxigen și poate crește sinteza factorului de necroză tumorală (TNF).
Deși își are rădăcinile în oncologie, utilizarea MMC a devenit mai răspândită, în special în cadrul îngrijirii oftalmologice, în încercarea de a limita formarea excesivă de cicatrici postoperatorii. Optometriștii care comanagementul pacienților cu intervenții chirurgicale pot fi familiarizați cu utilizarea sa intraoperatorie pentru a preveni cicatrizarea la pacienții care au fost supuși unei proceduri de filtrare a glaucomului și cu utilizarea sa în PRK pentru a preveni apariția ceții corneene. De la prima sa utilizare asociată OSSN la mijlocul anilor 1990, MMC s-a dovedit a fi eficient, cu rate de succes între 82% și 100%. Dozajul este de obicei o concentrație de 0,04% administrată QID în cicluri de o săptămână, o săptămână de pauză, sau o concentrație de 0,02% este administrată în mod continuu în tratamente de patru săptămâni.4 Toxicitatea medicamentului este mai mare în cazul tratamentelor prelungite sau al concentrațiilor mai mari
Deoarece MMC este un medicament deosebit de puternic, potențial periculos, efectele sale secundare-deficiența celulelor stem limbale și topirea sclerală, de exemplu-poate fi severe. Efectele secundare mai frecvent întâlnite, cum ar fi epiteliopatia corneană și conjunctivală și injecția conjunctivală, sunt tranzitorii.4,14 Atunci când se utilizează, MMC necesită o urmărire atentă și întreruperea medicației atunci când se suspectează orice efect secundar semnificativ.
5-Fluorouracil (5-FU). Acesta este un alt antimetabolit utilizat în tratamentul tumorilor dermatologice și, de asemenea, de către chirurgii specializați în glaucom. Mecanismul său blochează sinteza ADN prin interferarea cu enzima timidilat sintetază. În tratamentul OSSN, 5-FU este, în general, dozat la o concentrație de 1% QID o lună da, o lună nu, până la rezoluție. Majoritatea cazurilor se rezolvă cu unul sau două cicluri, deși în unele cazuri este nevoie de până la cinci cicluri. Toxicitatea epitelială, care duce la eroziune sau descuamare, este frecventă. Într-un studiu, durata tratamentului a fost stabilită în funcție de timpul până la apariția descuamării, iar timpul de întrerupere a tratamentului a durat până la reepitelizare. În ciuda acestei complicații dureroase, efectele secundare ale 5-FU nu par a fi la fel de severe ca cele ale MMC, iar ratele de recurență sunt în general raportate ca fiind echivalente.4,14
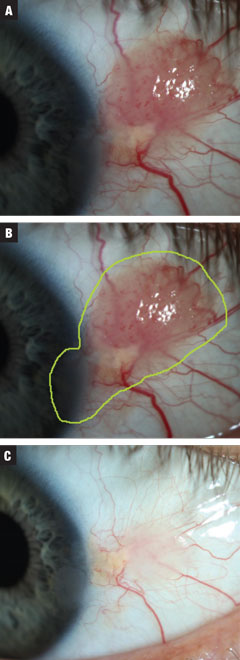
Fig. 3a. Cazul 3 a implicat o CIN papilomatoasă prezumată de dimensiuni moderate. Pacientul a fost inițiat pe tratament INF-a2b trei milioane UI timp de 10 zile. Fig. 3b. Dimensiunea totală estimată a leziunii. Fig. 3c. Post-tratament. Rezolvarea aproape completă a creșterii cu un epiteliu cornean neregulat în continuare. Împotriva sfaturilor, pacientul a optat pentru observație în acest moment. Faceți clic pe imagine pentru a o mări.
Interferon alfa 2b (INF-a2b). Interferonii sunt un subgrup de proteine inflamatorii naturale cunoscute sub numele de citokine. Aceștia sunt produși de celulele imune activate și au efecte antineoplazice, antivirale și antimicrobiene variabile. Prima utilizare raportată a INF-a2b în 1994 a dus la rezolvarea cu succes a unei leziuni CIN cu ajutorul utilizării sale topice.5 De atunci, INF-a2b a fost utilizat atât topic, cât și subconjunctival, cu un efect bun, în tratamentul OSSN.
Dosarea perilesională are cea mai mare eficacitate, cu o rezoluție de 87% până la 100% pe o perioadă de cinci săptămâni (cu injecții administrate de până la trei ori pe săptămână).4,14,15 Sunt necesare mai multe injecții pentru a obține acest nivel de eficacitate, ceea ce determină ca până la 100% dintre pacienți să dezvolte mialgii sistemice și febră.5,14 Dozarea topică este aproximativ echivalentă cu MMC în ceea ce privește eficacitatea.14,15 Se administrează la o concentrație de un milion de unități internaționale (UI) pe milimetru și se administrează QID timp de o lună dincolo de rezoluția clinică. În cazul în care nu apare rezoluția, concentrația poate fi crescută până la trei milioane UI, tot QID. În general, indiferent de concentrația de tratament, farmaciile de compoziție vor pregăti flaconul dintr-un singur preparat de un milion de UI. Acest preparat de un milion UI poate fi concentrat și mai mult prin reducerea cantității de suport din flacon. Efectele secundare ale INF-a2b topic sunt ușoare, hiperemia și conjunctivita foliculară fiind raportate frecvent; cheratita este raportată mai rar.4
Topic vs. Chirurgie
Deși biopsia și excizia chirurgicală au fost tratamentul istoric de elecție, chimioterapicele topice, care au unele beneficii teoretice față de chirurgie, au câștigat o oarecare acceptare ca terapie de primă linie. În cazul chirurgiei, este imposibil să se garanteze marje clare – o caracteristică necesară pentru cel mai bun prognostic. Cu cât este mai mare cantitatea de țesut îndepărtată pentru a asigura marje clare, cu atât mai mare este potențialul de perturbare pe termen lung a suprafeței oculare. Agenții topici tratează întreaga suprafață oculară, eliminând necesitatea de a identifica marginile și permițând un tratament eficient al populațiilor celulare neoplazice care nu ar putea fi identificate în mod clar cu ajutorul analizei microscopice – un beneficiu care ar putea duce la asocierea agenților topici cu excizia chirurgicală ca un protocol de tratament total pentru leziunile mari. Dezavantajul terapiei topice este, bineînțeles, că, deoarece întreaga suprafață oculară este expusă la medicament – din punct de vedere tehnic, un tratament excesiv – pot apărea complicații și, în cazul MMC în special, aceste complicații, deși rare, pot fi severe.
În ceea ce privește eficacitatea, toți agenții de chimioterapie topică pentru managementul OSSN se comportă rezonabil de bine. INF-a2b a fost supus unor studii de eficacitate față de rezecția chirurgicală și s-a demonstrat că elimină leziunea la rate comparabile, iar ratele de recurență pot fi de fapt mai mici pentru INF-a2b în raport cu rezecția.4 Studiile de urmărire raportează că utilizarea sa este mai adecvată în cazul leziunilor simple sau mici, în timp ce intervenția chirurgicală este preferabilă în cazul leziunilor mai avansate, deși terapia topică poate fi preferabilă în cazul leziunilor recurente.4,15
MMC are, în general, cea mai scurtă durată de tratament, dar este cea mai toxică și prezintă cel mai mare risc de complicații. 5-FU are un profil de efecte secundare și o durată de tratament medii; este, de asemenea, cel mai puțin costisitor din grup. INF-a2b are o tolerabilitate superioară, dar este adesea asociat cu un tratament mai îndelungat și un cost mai mare.4,13-16
Costul poate fi cu siguranță un aspect de luat în considerare atunci când se decide utilizarea chimioterapiei topice. Companiile de asigurări vor refuza uneori să acopere aceste medicamente, raportând utilizarea lor ca fiind experimentală. În cadrul unor cure scurte de tratament și comparând doar cheltuielile totale cu asistența medicală, chimioterapicele topice sunt mai puțin costisitoare decât intervenția chirurgicală; cu toate acestea, ele pot depăși cheltuielile cu intervenția chirurgicală după mai multe cure.
Lăsând la o parte acest posibil obstacol, având în vedere eficacitatea, capacitatea de a evita intervenția chirurgicală și tolerabilitatea generală, atunci când sunt utilizate într-un mod monitorizat, chimioterapicele topice par a fi o opțiune bună pentru tratamentul leziunilor de neoplasm intraepitelial conjunctival.
Dr. Bronner este optometrist al personalului de la Pacific Cataract and Laser Institute din Kennewick, Wash.
1. Kiire CA, Dhillon B. Etiologia și asociațiile neoplaziei intraepiteliale conjunctivale. Br J Ophthalmol. 2006:90(1);109-13.
2. Birkholz ES et al. Treatment of ocular surface squamous cell intraepithelial neoplasia with and without mitomycin C. Cornee. 2011;30:37-41.
3. Lee GA, Hirst LW. Neoplazia scuamoasă de suprafață oculară. Survey of Ophthalmology. 1995; 39:429-50.
4. Nelson KD, McSoley JJ. Constatări clinice și managementul neoplaziei intraepiteliale conjunctivale. Optometrie. 2011; 82:15-21.
5. Nanji AA, Sayyad FE, Karp CL. Chimioterapia topică pentru neoplazia scuamoasă a suprafeței oculare. Opinie curentă în oftalmologie. 2013; 24:336-42.
6. Warner M, Jakobiec F. Squamous Neoplasms of the Conjunctiva. În: The Humanity: Krachmer JH, Mannis MJ, Holland EJ eds. Cornea. 2nd ed. St Louis: Mosby; 2004:557-70.
7. Rapuono CJ, Luchs JI, Kim T. Conjunctival and External Disease. Segmentul anterior: cerințele. Ed. Krachmer, JH. Mosby. 2000;33-6.
8. Huerva V și Ascaso FJ. Conjunctival Intraepithelial Neoplasia – Prezentare clinică, diagnostic și posibilități de tratament. Srivstava S (Ed.) ISBN: 978-953-307-987-5, InTech.
9. Nelson KD, McSoley JJ. Constatări clinice și managementul neoplaziei intraepiteliale conjunctivale. Optometrie. 2011;82:15-21.
10. Kieval JZ1, Karp CL, Abou Shousha M, et al. Ultra-high resolution optical coherence tomography for differentiation of ocular surface squamous neoplasia and pterigia. Invest Ophthalmol and Vis Sci. 2011; 52:1741.
11. Peksayar G, Soyturk MK, Demiryont M: Rezultatele pe termen lung ale crioterapiei asupra tumorilor epiteliale maligne ale conjunctivei. Amer J of Ophthalmol. 1989;107: 337.
12. Santhiago MR, Netto MV, Wilson SE. Mitomicina C: Efecte biologice și utilizare în chirurgia refractivă. Cornea. 2012; 31:311-21.
13. Tomaz M. Mitomicina C: mică, rapidă și mortală (dar foarte selectivă). Chem and Biol. 1995; 2:575-9.
14. Majmudar PA, Epstein RJ. Antimetaboliți în neoplazia suprafeței oculare. Curr Opin in Ophthalmol. 1998; 9:35-9.
15. Besley J, Pappalardo J, Lee GA. Factori de risc de recidivă a neoplaziei scuamoase de suprafață oculară după tratamentul cu mitomicină C topică și interferon alfa 2b. Amer J of Ophthalmol 2014; 157:287-93.
16. Boehm M și Huang AJW. Tratamentul neoplaziei intraepiteliale corneene și conjunctivale recurente cu interferon alfa-2b topic. Ophthalmol. 2004; 111:1755-61.