Eliberarea de hormoniEdit
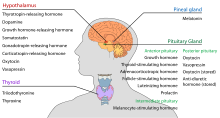
Ipotalamusul are o funcție neuroendocrină centrală, mai ales prin controlul hipofizei anterioare, care la rândul ei reglează diverse glande și organe endocrine. Hormonii de eliberare (numiți și factori de eliberare) sunt produși în nucleii hipotalamici, apoi sunt transportați de-a lungul axonilor fie la eminența mediană, fie la hipofiza posterioară, unde sunt depozitați și eliberați în funcție de necesități.
Hipofiza anterioară
În cadrul axei hipotalamo-adenohipofizare, hormonii de eliberare, cunoscuți și sub numele de hormoni hipofizotropi sau hipotalamici, sunt eliberați din eminența mediană, o prelungire a hipotalamusului, în sistemul portal hipofizar, care îi transportă la hipofiza anterioară, unde își exercită funcțiile de reglare a secreției de hormoni adenohipofizari. Acești hormoni hipofizotropici sunt stimulați de celulele neurosecretoare parvocelulare situate în zona periventriculară a hipotalamusului. După ce sunt eliberați în capilarele celui de-al treilea ventricul, hormonii hipofizotropici călătoresc prin ceea ce se numește circulația portal hipotalamo-hipofizar. Odată ajunși la destinație în hipofiza anterioară, acești hormoni se leagă de receptorii specifici situați pe suprafața celulelor hipofizare. În funcție de celulele care sunt activate prin această legare, hipofiza va începe să secrete sau va înceta să mai secrete hormoni în restul fluxului sanguin.
| Hormon secretat | Abbreviație | Produs de | Efect | |
|---|---|---|---|---|
| Hormonul eliberator de tirotropină (Hormonul eliberator de prolactină) |
TRH, TRF, sau PRH | Celule neurosecretoare parvocelulare ale nucleului paraventricular | Stimulează eliberarea hormonului de stimulare a tiroidei (TSH) de către hipofiza anterioară (în principal) Stimulează eliberarea prolactinei de către hipofiza anterioară |
|
| Corticotropina-releasing hormone | CRH sau CRF | Celule neurosecretoare parvocelulare ale nucleului paraventricular | Stimulează eliberarea hormonului adrenocorticotropic (ACTH) de către hipofiza anterioară | |
| Dopamina (Prolactina-inhibitor al hormonului) |
DA sau PIH | Neuronii dopaminergici din nucleul arcuat | Inhibă eliberarea de prolactină de către hipofiza anterioară | |
| Growth-hormon de eliberare a hormonului de creștere | GHRH | Neuronii neuroendocrini din nucleul arcuat | Stimulează creșterea-hormonului de creștere (GH) eliberat de hipofiza anterioară | |
| Hormonul de eliberare a gonadotropinei | GnRH sau LHRH | Celulele neuroendocrine din zona preoptică | Stimulează eliberarea de foliculul-stimularea hormonului (FSH) din hipofiza anterioară Stimulează eliberarea hormonului luteinizant (LH) din hipofiza anterioară | |
| Somatostatină (hormon inhibitor al hormonului de creștere) |
SS, GHIH, sau SRIF | Celule neuroendocrine ale nucleului periventricular | Inhibă eliberarea hormonului de creștere (GH) de către hipofiza anterioară Inhibă (moderat) eliberarea hormonului de stimulare a tiroidei (TSH) de către hipofiza anterioară |
Alți hormoni secretați de către eminența mediană includ vasopresina, oxitocina și neurotensina.
Hipofiza posterioară
În cadrul axei hipotalamo-neurohipofizare, hormonii neurohipofizari sunt eliberați din hipofiza posterioară, care este de fapt o prelungire a hipotalamusului, în circulație.
| Hormonul secretat | Abbreviație | Produs de | Efect |
|---|---|---|---|
| Oxitocină | OXY sau OXT | Celule neurosecretoare magnocelulare ale nucleului paraventricular și supraoptic. nucleul | Contracția uterină Lactația (reflexul de scădere) |
| Vasopresină (hormonul antidiuretic) |
ADH sau AVP | Celule neurosecretoare magnocelulare și parvocelulare ale nucleului paraventricular, celulele magnocelulare din nucleul supraoptic | Creșterea permeabilității la apă a celulelor tubului distal și a canalului colector din rinichi și permite astfel reabsorbția apei și excreția de urină concentrată |
Se știe, de asemenea, că hormonii axei hipotalamo-hipofizo-suprarenale (HPA) sunt legați de anumite boli de piele și de homeostazia pielii. Există dovezi care leagă hiperactivitatea hormonilor HPA de bolile cutanate legate de stres și de tumorile cutanate.
StimulareEdit
Ipotalamusul coordonează numeroase ritmuri circadiene hormonale și comportamentale, modele complexe de ieșiri neuroendocrine, mecanisme homeostatice complexe și comportamente importante. Prin urmare, hipotalamusul trebuie să răspundă la multe semnale diferite, dintre care unele sunt generate din exterior și altele din interior. Semnalizarea undei delta care apare fie în talamus, fie în cortex influențează secreția de hormoni eliberatori; GHRH și prolactina sunt stimulate, în timp ce TRH este inhibată.
Ipotalamusul este sensibil la:
- Lumină: Lungimea zilei și fotoperioada pentru reglarea ritmurilor circadiene și sezoniere
- Stimuli olfactivi, inclusiv feromoni
- Steroizi, inclusiv steroizi gonadici și corticosteroizi
- Informații transmise pe cale nervoasă care provin în special de la inimă, sistemul nervos enteric (al tractului gastrointestinal) și tractul reproducător.
- Intrări autonome
- Stimuli transmiși prin sânge, inclusiv leptină, grelină, angiotensină, insulină, hormoni hipofizari, citokine, concentrații plasmatice de glucoză și osmolaritate etc.
- Stresul
- Invadarea microorganismelor prin creșterea temperaturii corpului, resetarea în sus a termostatului organismului.
Stimuli olfactiviEdit
Stimulii olfactivi sunt importanți pentru reproducerea sexuală și funcția neuroendocrină la multe specii. De exemplu, dacă un șoarece gestant este expus la urina unui mascul „ciudat” în timpul unei perioade critice după coitus, atunci sarcina eșuează (efectul Bruce). Astfel, în timpul coitului, o femelă de șoarece își formează o „memorie olfactivă” precisă a partenerului său, care persistă timp de câteva zile. Indicii feromonali ajută la sincronizarea estrului la multe specii; la femei, menstruația sincronizată poate apărea, de asemenea, din indicii feromonali, deși rolul feromonilor la om este contestat.
Stimuli transmiși prin sângeEdit
Hormonii peptidici au influențe importante asupra hipotalamusului și, pentru a face acest lucru, trebuie să treacă prin bariera hemato-encefalică. Hipotalamusul este delimitat în parte de regiuni cerebrale specializate care nu au o barieră hemato-encefalică eficientă; endoteliul capilar din aceste locuri este fenestrat pentru a permite trecerea liberă chiar și a proteinelor mari și a altor molecule. Unele dintre aceste locuri sunt locurile de neurosecreție – neurohipofiza și eminența mediană. Cu toate acestea, altele sunt locuri în care creierul prelevează compoziția sângelui. Două dintre aceste situri, SFO (organul subfornical) și OVLT (organum vasculosum of the lamina terminalis) sunt așa-numitele organe circumventriculare, unde neuronii sunt în contact intim atât cu sângele, cât și cu LCR. Aceste structuri sunt dens vascularizate și conțin neuroni osmoreceptivi și receptori de sodiu care controlează băutul, eliberarea de vasopresină, excreția de sodiu și apetitul pentru sodiu. Acestea conțin, de asemenea, neuroni cu receptori pentru angiotensină, factor natriuretic atrial, endotelină și relaxină, fiecare dintre aceștia fiind importanți în reglarea echilibrului hidric și electrolitic. Neuronii din OVLT și SFO se proiectează către nucleul supraoptic și nucleul paraventricular, precum și către zonele hipotalamice preoptice. Organele circumventriculare pot fi, de asemenea, locul de acțiune al interleukinelor pentru a declanșa atât febra, cât și secreția de ACTH, prin efecte asupra neuronilor paraventriculari.
Nu este clar cum obțin accesul necesar toate peptidele care influențează activitatea hipotalamică. În cazul prolactinei și leptinei, există dovezi de absorbție activă la nivelul plexului coroidian din sânge în lichidul cefalorahidian (LCR). Unii hormoni hipofizari au o influență de feedback negativ asupra secreției hipotalamice; de exemplu, hormonul de creștere se alimentează înapoi la nivelul hipotalamusului, dar nu este clar cum intră în creier. Există, de asemenea, dovezi privind acțiunile centrale ale prolactinei.
Cerințele au sugerat că hormonul tiroidian (T4) este preluat de celulele gliale hipotalamice din nucleul infundibular/ eminența mediană și că aici este transformat în T3 de către deiodinaza de tip 2 (D2). Ulterior, T3 este transportată în neuronii producători de hormon eliberator de tirotropină (TRH) din nucleul paraventricular. În acești neuroni au fost găsiți receptori ai hormonului tiroidian, ceea ce indică faptul că aceștia sunt într-adevăr sensibili la stimulii T3. În plus, acești neuroni au exprimat MCT8, un transportor de hormoni tiroidieni, susținând teoria conform căreia T3 este transportat în ei. T3 ar putea apoi să se lege de receptorul hormonului tiroidian din acești neuroni și să afecteze producția de hormon eliberator de tirotropină, reglând astfel producția de hormoni tiroidieni.
Ipotalamusul funcționează ca un fel de termostat pentru organism. Acesta stabilește o temperatură corporală dorită și stimulează fie producția și retenția de căldură pentru a ridica temperatura sângelui la un nivel mai ridicat, fie transpirația și vasodilatația pentru a răci sângele la o temperatură mai scăzută. Toate febrele sunt rezultatul unui reglaj ridicat în hipotalamus; temperaturile corporale ridicate din orice altă cauză sunt clasificate ca hipertermie. Rareori, afectarea directă a hipotalamusului, cum ar fi în urma unui accident vascular cerebral, va provoca febră; aceasta se numește uneori febră hipotalamică. Cu toate acestea, este mai frecvent ca astfel de leziuni să provoace temperaturi corporale anormal de scăzute.
SteroiziEdit
Ipotalamusul conține neuroni care reacționează puternic la steroizi și glucocorticoizi – (hormonii steroizi ai glandei suprarenale, eliberați ca răspuns la ACTH). De asemenea, conține neuroni specializați sensibili la glucoză (în nucleul arcuat și în hipotalamusul ventromedial), care sunt importanți pentru apetit. Zona preoptică conține neuroni termosensibili; aceștia sunt importanți pentru secreția de TRH.
NeuralEdit
Secreția de oxitocină ca răspuns la supt sau la stimularea vagino-cervicală este mediată de unele dintre aceste căi; secreția de vasopresină ca răspuns la stimuli cardiovasculari proveniți de la chemoreceptorii din corpul carotidian și arcul aortic și de la receptorii volumului atrial de joasă presiune, este mediată de altele. La șobolan, stimularea vaginului determină, de asemenea, secreția de prolactină, iar acest lucru are ca rezultat o pseudo-graviditate în urma unei împerecheri infertile. La iepure, coitul provoacă ovulația reflexă. La oaie, stimularea cervicală în prezența unor niveluri ridicate de estrogen poate induce un comportament matern la o oaie virgină. Toate aceste efecte sunt mediate de hipotalamus, iar informația este transportată în principal prin căile spinale care se transmit în trunchiul cerebral. Stimularea mameloanelor stimulează eliberarea de oxitocină și prolactină și suprimă eliberarea de LH și FSH.
Stimulii cardiovasculari sunt transportați de nervul vag. De asemenea, vagul transmite o varietate de informații viscerale, inclusiv, de exemplu, semnale provenite din distensia sau golirea gastrică, pentru a suprima sau promova alimentația, prin semnalizarea eliberării de leptină, respectiv gastrină. Din nou, aceste informații ajung la hipotalamus prin intermediul unor relee din trunchiul cerebral.
În plus, funcția hipotalamică răspunde la – și este reglată de – nivelurile tuturor celor trei neurotransmițători monoaminici clasici, noradrenalina, dopamina și serotonina (5-hidroxitriptamina), în acele traiecte din care primește inervație. De exemplu, intrările noradrenergice care provin din locus coeruleus au efecte reglatoare importante asupra nivelurilor hormonului eliberator de corticotropină (CRH).
Controlul aportului alimentarEdit
| Peptide care cresc alimentația comportamentul de hrănire |
Peptide care scad comportamentul de hrănire |
|
|---|---|---|
| Ghrelina | Leptina | |
| Neuropeptida Y | (α,β,γ)-Hormoni de stimulare a melanocitelor | |
| Peptidă legată de Agouti | Peptide de transcriere reglate de cocaină și amfetamină | |
| Orexine (A,B) | Hormonul de eliberare a corticotropinei | |
| Hormonul de concentrare a melaninei | Cholecistochinina | |
| Galanina | Insulina | |
| Glucagon-like peptide 1 |
Partea extremă laterală a nucleului ventromedial al hipotalamusului este responsabilă de controlul aportului alimentar. Stimularea acestei zone determină creșterea aportului alimentar. Lezarea bilaterală a acestei zone determină încetarea completă a aportului alimentar. Părțile mediale ale nucleului au un efect de control asupra părții laterale. Lezarea bilaterală a părții mediale a nucleului ventromedial determină hiperfagia și obezitatea animalului. Lezarea ulterioară a părții laterale a nucleului ventromedial la același animal produce încetarea completă a aportului alimentar.
Există diferite ipoteze legate de această reglare:
- Ipoteza lipostatică: Această ipoteză susține că țesutul adipos produce un semnal umoral care este proporțional cu cantitatea de grăsime și acționează asupra hipotalamusului pentru a diminua aportul alimentar și a crește producția de energie. S-a evidențiat faptul că un hormon, leptina, acționează asupra hipotalamusului pentru a diminua aportul alimentar și a crește producția de energie.
- Ipoteza gastro-intestinală: hormoni gastro-intestinali precum Grp, glucagoni, CCK și alții susțin că inhibă aportul alimentar. Alimentele care intră în tractul gastrointestinal declanșează eliberarea acestor hormoni, care acționează asupra creierului pentru a produce sațietate. Creierul conține atât receptori CCK-A, cât și CCK-B.
- Ipoteza glucostatică: Activitatea centrului de sațietate din nucleii ventromediali este probabil guvernată de utilizarea glucozei la nivelul neuronilor. S-a emis ipoteza că atunci când utilizarea glucozei de către aceștia este scăzută și, în consecință, când diferența de glucoză din sângele arteriovenos prin aceștia este scăzută, activitatea prin neuroni scade. În aceste condiții, activitatea centrului de hrănire este necontrolată, iar individul are senzația de foame. Ingestia de alimente este rapid crescută prin administrarea intraventriculară de 2-deoxiglucoză, scăzând astfel utilizarea glucozei în celule.
- Ipoteza termostatică: Conform acestei ipoteze, o scădere a temperaturii corporale sub un anumit punct de referință stimulează pofta de mâncare, în timp ce o creștere peste punctul de referință inhibă pofta de mâncare.
Procesarea friciiEdit
Zona medială a hipotalamusului face parte dintr-un circuit care controlează comportamentele motivate, cum ar fi comportamentele defensive. Analizele de marcare Fos au arătat că o serie de nuclei din „coloana de control comportamental” este importantă în reglarea expresiei comportamentelor defensive înnăscute și condiționate.
Comportamentul defensiv antipredator
Expunerea la un prădător (cum ar fi o pisică) provoacă comportamente defensive la rozătoarele de laborator, chiar și atunci când animalul nu a fost niciodată expus la o pisică. În hipotalamus, această expunere determină o creștere a celulelor marcate cu Fos în nucleul hipotalamic anterior, în partea dorsomedială a nucleului ventromedial și în partea ventrolaterală a nucleului premamilar (PMDvl). Nucleul premamilar are un rol important în exprimarea comportamentelor defensive față de un prădător, deoarece leziunile în acest nucleu abolesc comportamentele defensive, precum înghețarea și fuga. PMD nu modulează comportamentul defensiv în alte situații, deoarece leziunile acestui nucleu au avut efecte minime asupra scorurilor de înghețare după șoc. PMD are conexiuni importante cu cenușiul periacueductal dorsal, o structură importantă în exprimarea fricii. În plus, animalele manifestă comportamente de evaluare a riscului față de mediul asociat anterior cu pisica. Analiza celulelor marcate cu Fos a arătat că PMDvl este cea mai activată structură din hipotalamus, iar inactivarea cu muscimol înainte de expunerea la context abolește comportamentul defensiv. Prin urmare, hipotalamusul, în principal PMDvl, are un rol important în exprimarea comportamentelor defensive înnăscute și condiționate față de un prădător.
Înfrângerea socială
La fel, hipotalamusul are un rol în înfrângerea socială: Nuclee din zona mediană sunt, de asemenea, mobilizate în timpul unei întâlniri cu un conspecific agresiv. Animalul învins are o creștere a nivelurilor Fos în structurile cu dimorfism sexual, cum ar fi nucleul preoptic medial, partea ventrolaterală a nucleului ventromedial și nucleul premamilar ventral. Astfel de structuri sunt importante în alte comportamente sociale, cum ar fi comportamentele sexuale și agresive. Mai mult, nucleul premamilar este, de asemenea, mobilizat, partea dorsomedială, dar nu și partea ventrolaterală. Leziunile în acest nucleu abolesc comportamentele defensive pasive, cum ar fi înghețarea și postura „pe spate”.
.