Structura Kekulé pentru benzen
Se știa că benzenul are formula moleculară C6H6, dar formula sa structurală era necunoscută.
Dacă benzenul era o hidrocarbură nesaturată cu catenă dreaptă, ar trebui să sufere cu ușurință reacții de adiție (la fel ca alte alchene și alchine).
De exemplu, bromul, Br2, ar trebui să se adauge peste legătura dublă sau triplă, așa cum se arată mai jos:
| posibilă reacție de adiție a structurii cu catenă dreaptă: | |||
| CH3-C≡C-C≡C-CH3 | + Br2 | → | CH3-CBr=CBr-C≡C-CH3 |
Dar, atunci când bromul este adăugat la benzen la 25°C și 1 atm (101.3 kPa) presiune, nu pare să aibă loc nicio reacție.
Astfel, structurile posibile pentru benzen care implică legături duble și/sau triple dispuse în lanț păreau cele mai puțin probabile, deoarece acestea ar trebui să sufere reacții de adiție.
Dacă se adaugă brom la benzen în prezența FeBr3, acesta suferă o reacție de substituție în care unul dintre atomii de hidrogen este înlocuit cu un atom de brom pentru a produce un compus cu formula C6H5Br, așa cum se arată mai jos:
| reacție de substituție cunoscută: | ||||||||
| C6H6 | + Br2 | FeBr3 → |
C6H5Br | + HBr | ||||
În acest sens, benzenul se comporta mult mai mult ca o hidrocarbură saturată (doar legături simple între atomii de carbon).
Astfel, prima structură propusă de Kekulé pentru benzen în 1865 nu conținea nici o legătură dublă, dar dispunea cei 6 atomi de carbon într-un inel, așa cum se arată mai jos:
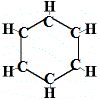
Kekulé și-a dat seama că această moleculă încalcă regula tetravalenței pentru carbon, adică fiecare atom de carbon formează doar 3 legături în loc de 4.
Așa că, în 1872, Kekulé a propus o structură a benzenului compusă din trei legături simple și duble alternative, așa cum se arată mai jos:
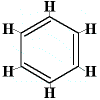
Rețineți că, deși atomii de carbon nu sunt scriși în cadrul structurii, se înțelege întotdeauna că există un atom de cabon acolo unde se unesc două linii ale hexagonului, astfel încât există 6 „îmbinări”, 6 unghiuri și, prin urmare, 6 atomi de carbon.
În această structură, fiecare atom de carbon este legat de un atom de hidrogen și, de alți doi atomi de carbon. Una dintre legăturile carbon-carbon este o legătură simplă, iar cealaltă legătură carbon-carbon este o legătură dublă. Fiecare atom de carbon a realizat 4 legături.
În timp ce această structură nu explică de ce benzenul nu suferă reacții de adiție, ea ar putea explica de ce benzenul formează doar un singur izomer structural atunci când benzenul reacționează cu bromul într-o reacție de substituție, așa cum se arată mai jos:
 structura propusă a benzenului |
+ Br2 | → | 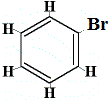 numai 1 izomer structural |
. | + HBr |
Celelalte structuri inelare propuse pentru benzen ar fi prezis mai mult de un izomer structural pentru produsul reacției de substituție, așa cum se arată mai jos:
| alte structuri propuse pentru structura inelară a reacției: | 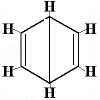 |
Br2 → |
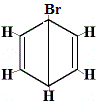 izomer structural 1 |
+ | . | 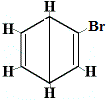 izomer structural 2 |
Ce s-ar întâmpla dacă un alt atom de hidrogen ar fi înlocuit (substituit) cu un atom de brom?
| C6H5Br | + Br2 | FeBr3 → |
C6H4Br2 | + HBr |
Câți izomeri structurali ai C6H4Br2 se vor produce?
 |
Br2 → FeBr3 |
. 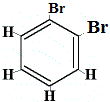 izomer structural 1 |
+ | 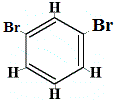 izomer structural 2 |
+ | . 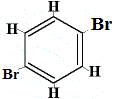 izomer structural 3 |
+ | 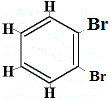 izomer structural 4 |
Izomerii structurali 1 și 4 sunt diferiți deoarece în izomerul 1 cei doi atomi de Br sunt legați de atomii de carbon pe un C-.C, în timp ce în izomerul 4 cei doi atomi de Br sunt legați de atomii de carbon pe o legătură C=C.
Cu toate acestea, când C6H5Br obținut din benzen reacționează cu bromul într-o reacție de substituție, se produc doar 3 izomeri structurali de C6H4Br2!
Pentru a rezolva această problemă, Kekulé a propus că inelul benzenic se află în echilibru rapid între structuri în care dublele legături se află în poziții alternative, așa cum se arată mai jos:
 |
⇋ | 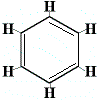 |
Așadar, atunci când bromul reacționează cu C6H5Br într-o reacție de substituție pentru a produce C6H4Br2, perechile de izomeri structurali ai C6H4Br2 se află în echilibru unul cu celălalt.
Aceasta înseamnă că izomerii structurali 1 și 4 prezentați mai sus, care diferă doar prin faptul că atomii de Br sunt legați printr-o legătură simplă sau printr-o legătură dublă, sunt acum în echilibru rapid unul cu celălalt, așa cum se arată mai jos:
| Atomi de Br pe atomi de C adiacenți, izomerul structural 1 are atomi de Br peste C-C izomerul structural 4 are atomi de Br peste C=C |
 izomerul structural 1 |
⇋ |  izomerul structural 4 |
Conform lui Kekulé, acești doi izomeri structurali ai C6H4Br2 se află într-un echilibru atât de rapid încât nu pot fi separați ca două molecule separate, astfel încât se pare că există doar 3 izomeri în loc de 4.
Deși această structură de echilibru rapid pentru benzen, cunoscută sub numele de structura Kekulé, s-a dovedit a fi utilă, ea nu explică stabilitatea unică (lipsa de reactivitate) a inelului benzenic, nu explică de ce benzenul nu suferă cu ușurință reacții de adiție, dar poate fi indus să sufere reacții de adiție.
Înțelegeți acest lucru?
Aderă la AUS-e-TUTE!
Fă testul acum!
.