Typer av asbest, egenskaper och användningsområden
Asbest delas in i två stora undergrupper: amfiboler och serpentiner, var och en med sina tydliga fysiska och kemiska egenskaper. Serpentinfibrer kännetecknas av sin böjda form vid elektronmikroskopi, och krysotil eller vit asbest är den enda medlemmen i denna undergrupp. De andra formerna är amfiboler, som består av raka styva fibrer av varierande längd, i allmänhet mindre än 5 μm.1
Asbest kännetecknas av sin beständighet mot höga temperaturer och kemikalier och sin höga draghållfasthet. Det används i mer än 3 000 olika tillämpningar inom många industrisektorer och även i andra allmänt spridda produkter som leksaker, brödrostar, torktumlare, rökvaror osv. Asbest finns i olika former: a) lös fyllning, b) ark eller plattor, c) inflätad i garn eller vävd i tyg, d) fibercement och e) som en komponent i murbruk. Dessa vitt skilda former gör det ofta svårt att identifiera asbest som ett material som använts av arbetstagare när man registrerar deras anställningshistorik. År 2002 trädde gemenskapsdirektiv 1999/77 i kraft som förbjöd användningen av alla typer av asbest i Europeiska unionen.2 I dag utgör yrkesmässig exponering för asbest fortfarande en risk för arbetstagare som arbetar med rivning, underhåll, reparation och transport av konstruktioner där asbest tidigare använts. I Spanien fastställs i det kungliga dekretet (RD) 396/20063 alla nödvändiga bestämmelser för vård av dessa arbetstagares hälsa.
Maligna och icke-maligna asbestrelaterade sjukdomar och deras patogenes (i dessa rekommendationer kommer vi att använda ordet godartad i stället för icke-malign) förtecknas i tilläggsmaterialet, som finns tillgängligt på nätet.
Diagnostiska tester för att utvärdera asbestrelaterade sjukdomarArbetsgivarhistoria
En fullständig arbetsgivarhistoria måste samlas in (konsekvent rekommendation, hög kvalitet på bevisen). Patienten måste tillfrågas om sin anställning, yrkeskategori, skyddsgrad, exponeringsgrad och företagsmedicinska kontroller under arbetslivet.
Om det finns någon känd exponering för asbest ska även följande uppgifter samlas in:
- –
år för första exponering, varaktighet och slut på exponeringen
- –
Typ av exponering: yrkesmässig, från arbete direkt med asbest; hushållsrelaterad, från byggnadsisolering eller andra föroreningar eller från tvätt av arbetskläder; miljörelaterad, från användning av asbest i offentliga lokaler, rivning av byggnader eller närhet till förorenande fabriker.
- –
Intensitet. Intensiv exponering anses vara direktkontakt under mer än 6 månader (8 timmar per dag, 40 timmar per vecka) eller en hög koncentration av asbestfibrer i inandningsluften (ministeriell förordning av den 31 oktober 1984. State Bulletin (BOE) 7 november 1984). Exponeringsrisken omfattar ett område inom en radie på 300-2200 meter från källan beroende på vindriktning, och yrkesmässig exponering är i allmänhet betydande efter 6 månaders arbete4 (konsekvent rekommendation, mycket låg beviskvalitet).
- –
Typ av asbest som används. Beroende på yrke.
- –
Index för samtidig rökning.
Bildgivande undersökningarStandardröntgenundersökning av bröstkorgen och datortomografi
Röntgenundersökning av bröstkorgen (Rx) är det grundläggande verktyget för att identifiera asbestrelaterade sjukdomar (samstämmig rekommendation, måttlig beviskvalitet).
Internationella arbetsbyråns (ILO) Rx-klassificering för bröstkorgen är användbar för att systematiskt beskriva och registrera radiografiska avvikelser i bröstkorgen som observeras inte bara vid asbestos, utan vid alla typer av pneumokonioser. I den senaste upplagan ses även kriterierna för klassificering av pleural förtjockning översiktligt över. 5 Dessa kriterier är alltså användbara för att beskriva radiologiska avvikelser, även om de inte är en förutsättning för att ställa diagnos.
Computertomografi (CT) är ett mer känsligt diagnostiskt verktyg (tabell 1).
Radiologiska kännetecken för pleuropulmonala asbestrelaterade sjukdomar.
| Asbestos | Irregulära retikulära opaciteter övervägande i baserna. Parenkymala band. Honeycombing Pattern |
|---|---|
| Pleurala plack | Långa täta eller linjära lesioner i den diafragmatiska pleuran, med respekt för phrenicocostala sinus och vertices. Oftast bilaterala. Kan vara förkalkade |
| Diffusa pleurala förtjockningar | Ansvälld pleurabredd som sträcker sig till minst en fjärdedel av bröstväggen. Vanligast unilateral och påverkar den bakre pleuran i baserna. Kan vara förkalkad. Kan vara associerad med parenkymala band och rundad atelektas |
| Benign pleurautgjutning | Unilateral, övervägande vänstersidig, liten till måttlig mängd. Kan inte särskiljas från andra orsaker till effusion ur radiologisk synvinkel |
| Rundad atelektas | Rundad oklarhet i pleurabasen med krökning av blodkärlen och intilliggande bronker (comet tail sign). Unilateral, |
| Pleuralt mesoteliom | Diffus nodulär pleuraförtjockning som påverkar den mediastinala pleuran i samband med pleurautgjutning och volymförlust i drabbade områden. hemithorax |
| Lungcancer | Indifferentierbart från andra fall |
Positronemissionstomografi (PET) och PET kombinerat med CT (PET-CT)
Bénard6 visade att denna teknik är användbar för att skilja godartade pleurala lesioner från pleurala mesoteliom, tack vare dess höga sensitivitet, specificitet och diagnostiska noggrannhet, förutom dess höga positiva prediktiva värde, och särskilt dess höga negativa prediktiva värde (92 %); 75%; 89%; 94.3 % respektive 92 %). Senare studier bekräftade dessa resultat.7 Dual PET är också till hjälp i den diagnostiska processen (SUV-indexet ökar i den sena fasen jämfört med den tidiga fasen vid mesoteliom och sjunker vid benigna lesioner). Liknande värden erhålls vid PET-CT. SUV-värdet varierar mellan de olika studierna. Om det finns en hög klinisk misstanke om mesoteliom, eller om PET eller PET-CT är positivt, måste diagnosen bekräftas med en patologistudie av en biopsi av pleuravävnad som erhållits företrädesvis genom kirurgi (samstämmig rekommendation, hög evidenskvalitet).
PET-CT är också en användbar bilddiagnostik vid stadiestudier av mesoteliom och vid undersökning av lesioner i lungparenkymet, eftersom det till skillnad från vid lungcancer inte sker något upptag av radiotracer vid rundad atelektas. Ett positivt resultat kräver histologisk bekräftelse.8
Magnetisk resonans och andra avbildningstekniker
Magnetisk resonanstomografi (MRT) har en mycket begränsad roll vid asbestrelaterade sjukdomar.
Det kan vara till hjälp när det gäller att skilja maligna pleurala tumörer från godartade lesioner, baserat på morfologiska förändringar och signalintensitet.9 Vid rundad atelektasi visar MRT den viscerala pleura som viker sig in i lesionen (konsekvent rekommendation, måttlig beviskvalitet).
Det definierar också extrapleuralt fett tydligare, och det är mer exakt när det gäller att fastställa invasion av bröstvägg och diafragma vid mesoteliomstagning, även om det inte är användbart för att detektera subdiafragmatisk invasion.10
Pleural ultraljud är användbart vid undersökning av pleurautgjutning och perifera massor som ett bildgivande verktyg för att vägleda förfaranden som t.ex. thorakocentes, pleurabiopsi osv. Det finns inga studier som stöder dess användning vid andra asbestrelaterade sjukdomar (konsekvent rekommendation, hög beviskvalitet).
Lungfunktionsundersökningar
Lungfunktionsundersökningar är obligatoriska vid diagnos och uppföljning av asbestrelaterade sjukdomar. När det används inom ramen för hälsoövervakning bidrar det till tidig diagnos av exponerade personer och är oumbärligt för att utvärdera en patients arbetsförmåga (samstämmig rekommendation, hög beviskvalitet).
Spirometri är det inledande förfarandet; forcerad expiratorisk volym i en sekund (FEV1), forcerad vitalkapacitet (FVC) och FEV1/FVC kan användas för att upptäcka och kvantifiera obstruktiva ventilationsdefekter och för att varna för ett restriktivt fel. Mätning av lungvolymer är obligatorisk för att diagnostisera en restriktiv ventilatorisk defekt. Mätning av diffusionskapacitet (DLCO) är ett känsligt test, men det saknar specificitet när det gäller att upptäcka interstitiell lungsjukdom och har en större variationskoefficient än spirometri.11 Vid asbestos är den karakteristiska funktionella förändringen ett restriktivt ventilationsmönster (minskad total lungkapacitet), och DLCO är vanligen nedsatt, båda till följd av fibros i lungparenkymet. En minskad diffusionskapacitet är ett av de känsligaste testerna för asbestos i ett tidigt stadium, även om specificiteten är låg. Diffus förtjockning av den viscerala pleuran utan interstitiellt engagemang kan också orsaka en restriktiv ventilationsdefekt.12 Efter mycket debatt ansågs pleuraplacken inte vara ansvariga för förändringar i lungfunktionen som, när de inträffar, beror på andra samtidiga orsaker, t.ex. begynnande interstitiellt engagemang eller rökning.13
Mineralogisk analys
Asbest kan påvisas i respiratoriska prover vid optisk mikroskopi i form av asbestkroppar (AB), även kallade ferruginösa kroppar, som bildas efter att fibrerna har belagts med proteinsubstanser i makrofagerna. Observation av AB i vanliga patologiska prover med hjälp av rutinmässig histologisk färgning (hematoxylin-eosin) är mycket specifik, men känsligheten är mycket låg. Därför krävs särskild behandling av proverna för att utvärdera asbestinnehållet i lungorna genom att räkna AB i lungvävnad eller bronkoalveolärt lavage14 (konsekvent rekommendation, hög kvalitet på bevisen). Prover av lungvävnad som väger minst 0,5 g krävs, och dessa smälts i natriumhypoklorit, filtreras och tvättas. AB-kvantifiering utförs med hjälp av ett 400× optiskt mikroskop. Storleken på de prover som krävs innebär att de vanligtvis erhålls från lobectomier, pneumonectomier eller obduktionsprover. Värden i lungbiopsi eller bronkoalveolärt lavage på mer än 1 000 AB/g torr lungvävnad eller 1 AB per milliliter bronkoalveolärt lavage tyder på exponering. Ett elektronmikroskop krävs för att upptäcka asbestfibrer. Om syftet är att identifiera fiberns kemiska sammansättning för att fastställa dess typ finns det olika metoder för provanalys, bland annat energidispersiv röntgenspektroskopi. Det krävs ett välutrustat laboratorium och utbildad personal för dessa förfaranden, och varje laboratorium måste fastställa referensvärden i enlighet med den lokala befolkningen. Det första steget som krävs för validering av laboratoriet i denna teknik är standardisering, eftersom anmärkningsvärda skillnader har konstaterats mellan grupper i olika länder. I Spanien har referensvärdena för lung-AB i den oexponerade befolkningen nyligen publicerats.15 Enligt de erhållna värdena bekräftades det att det internationella tröskelvärdet på 1 000 AB är lämpligt i vår miljö för att klassificera potentiellt sjukdomsframkallande värden.
Biomarkörer
Flera blod- och pleuravätskapselmarkörer för malignt pleuramesoteliom har undersökts, t.ex. hyaluronsyra, carcinoembryonalt antigen eller CA 125, men ingen av dem har visat sig vara användbar. Osteopontin produceras av malignt pleuramesoteliom, och nivåerna i serum är direkt kopplade till år av exponering och till lesionernas intensitet. Bristen på specificitet begränsar den diagnostiska användbarheten av denna markör.
Nackdelen med lösligt mesothelin är att det inte uttrycks i den sarkomatösa subtypen. Nivåerna i serum och i pleuravätska korrelerar mycket nära med varandra. I en nyligen genomförd metaanalys som studerade effekten av lösligt mesotelin vid diagnos av malignt pleuramesoteliom drogs slutsatsen att för en brytpunkt på 2ng/ml i plasma är arean under kurvan 0,77 (95 % KI: 0,73-0,81) med 95 % specificitet, men en mycket låg sensitivitet på 32 %.16 Med tanke på den höga specificiteten hos denna markör kräver positiva värden i riskpopulationer att patienten undersöks mer ingående. Dess låga specificitet innebär dock att ett negativt resultat inte utesluter diagnosen. Därför rekommenderas inte systematisk bestämning av lösligt mesothelin i den exponerade populationen som en metod för tidig diagnos (samstämmig rekommendation, hög beviskvalitet).
Fibulin-3, en ny biomarkör som beskrivits i gliomceller, är involverad i tumörinvasion och tumörtillväxt. Studier av malignt pleuramesoteliom har visat att fibulin-3-nivåer i plasma har 96 % sensitivitet och 95 % specificitet, och när den hittas i pleuravätska är sensitiviteten 84 % och specificiteten 93 %. Till skillnad från lösligt mesothelin finns det ingen korrelation mellan nivåerna i serum och nivåerna i pleuravätska. Nivåer av fibulin-3 i plasma kan bidra till att skilja personer som exponerats för asbest från patienter med malignt pleuramesoteliom, och i den sistnämnda gruppen är nivåerna associerade med prognosen. Lösligt mesotelin har dock visat sig vara överlägset fibulin-3 som diagnostisk markör.17 Trots sin låga känslighet, vilket gör den mindre användbar som metod för screening av den exponerade befolkningen, är lösligt mesotelin fortfarande den mest effektiva biomarkören för att diagnostisera mesoteliom (samstämmig rekommendation, låg kvalitet på bevisen).
Lagstiftning och specifikt protokoll för hälsoövervakning av asbest
Den nuvarande rättsliga ramen grundar sig på förordning (EG) nr 1299/2006 (tilläggsmaterial, tillgängligt online, bilaga I). Klassificeringen av yrkessjukdomar uppdaterades i denna RD, och en förteckning över verksamheter som kan orsaka yrkessjukdomar tillhandahölls. Asbestrelaterade sjukdomar förtecknas i bilaga II (kompletterande material, tillgängligt online), som nyligen utökats med larynxcancer.18 Sex grupper av yrkessjukdomar specificeras. Exponering för asbest förekommer i grupp 4 (icke-tumörsjukdomar) och i grupp 6 (tumörsjukdomar).
I övrigt gör lagen det obligatoriskt för varje läkare inom det nationella hälso- och sjukvårdssystemet att rapportera varje sjukdom som orsakas av yrkesmässig exponering för något av dessa ämnen som en misstänkt arbetssjukdom. Det finns ett standardformulär för deklaration för detta ändamål, som bedöms av det förvaltande organet, i allmänhet det spanska nationella institutet för social trygghet, och antingen godkänns eller avvisas. Denna deklaration är viktig för efterföljande rättstvister och bestämmer preskriptionstiden, i allmänhet ett år efter avslaget.
Lagen kräver också att företagen ska tillhandahålla information, vilket har lett till att varje autonom region har upprättat förteckningar över företag där asbest har använts.
Sedan denna förordning trädde i kraft har endast en förordning med anknytning till denna fråga publicerats: RD 843/2011, som reglerar riskförebyggande tjänster på arbetsplatsen.
I enlighet med detta ramverk har de autonoma regionerna inrättat program för riskförebyggande åtgärder på arbetsplatsen och stöd till exponerade personer.
Användning av det särskilda protokollet för hälsoövervakning: Första besöket och besöksintervall. Rekommendationer från EROM-gruppen
I artikel 16 i RD 396/2006 av den 31 mars 2006, som fastställer minimibestämmelser för hälsa och säkerhet som är tillämpliga på arbeten med risk för exponering för asbest, anges att ”med hänsyn till den långa latenstiden för de patologiska manifestationerna av exponering för asbest, ska varje arbetstagare som tidigare har exponerats för asbest och som slutar sitt anställningsförhållande med det företag där exponeringssituationen uppstod, oavsett om det beror på pensionering, byte av företag eller någon annan orsak, kommer att fortsätta att genomgå förebyggande hälsokontroller genom regelbundna undersökningar som utförs av det nationella hälsovårdssystemet på andningsmedicinska avdelningar som är utrustade med lämpliga resurser för undersökning av andningsfunktionen, eller på andra avdelningar som har anknytning till asbestrelaterade sjukdomar”.
I Spanien, liksom i andra länder, finns ett screening- och övervakningsprogram för arbetstagare som exponerats för asbest. Detta är medicinska program som är mycket viktiga för att identifiera och diagnostisera de olika sjukdomarna, men det finns få vetenskapliga bevis för att detta är en effektiv strategi för att förbättra sjukdomsförloppet.
Med tanke på detta rekommenderar SEPAR EROM-gruppen att de tester som utförs vid det första och de efterföljande besöken samt besöksintervallen bör vara följande:
1) Första besöket av en patient som konsulteras med en historia av möjlig exponering för asbest:
- –
Arbetshistoria: som anges ovan.
- –
Rökhistoria: om aktiv rökare, rådgivning eller behandling mot rökning (konsekvent rekommendation, hög beviskvalitet).
- –
Medicinsk anamnes och anamnes: patienten kommer att tillfrågas särskilt om respiratoriska symtom (dyspné, hosta och slemhinnor, bröstsmärta, hemoptys) samt asteni, anorexi och viktminskning.
- –
Fysisk undersökning: Bedöm om det finns knäppningar och spikklubbning.
- –
Tillkommande undersökningar:
- –
Kista Rx.
- –
Full lungfunktionstestning med forcerad spirometri, lungvolymer och DLCO i ett laboratorium som är utrustat för funktionstestning, enligt SEPAR:s rekommendationer.
Om sannolikheten för exponering är noll eller oklar utifrån patientens anställningshistoria (deras arbete finns inte med på listan över verksamheter med risk för exponering för asbest http://www.msssi.gob.es/ciudadanos/saludAmbLaboral/docs/ProtoVigiAmianto1.pdf) och om testresultaten är normala avslutas uppföljningen i detta läge.
En HRCT bör utföras om förändringar observeras på Rx i bröstet, om lungfunktionstesterna är onormala eller om en klinisk/funktionell diskrepans observeras (samstämmiga rekommendationer, låg beviskvalitet).
Vänligen är det sant att CT är känsligare än Rx i bröstkorgen för att diagnostisera okalkade pleurala plack, men användningen av CT för diagnostisering hos en patient med normal Rx i bröstkorgen, normala funktionstester och inga symtom kan ifrågasättas och stöds inte av vetenskaplig evidens (förhållandet mellan risk och nytta på grund av strålning måste också tas med i beräkningen).
En annan fråga är användningen av CT som screeningverktyg för lungcancer i tidiga sjukdomsstadier. I detta avseende fann man i en metaanalys som nyligen publicerades i Chest19 av sammanlagt över 5 000 arbetstagare en prevalens av lungcancer hos personer som exponerats för asbest på 1,1 %, vilket liknar den prevalens som rapporterades i studien om screening av lungcancer hos tunga rökare (1 %: 95 % KI: 0,09-1,1 %).20 Av denna anledning drar man i studien slutsatsen att CT-screening av arbetstagare som exponerats för asbest kan vara effektivt för att upptäcka asymtomatisk lungcancer i tidiga stadier, och att det alltså kan minska dödligheten i lungcancer i denna grupp arbetstagare.
Lungcancerscreening bland arbetstagare som exponerats för asbest är en brådskande fråga som kräver en stor, randomiserad studie för att fastställa konsekventa rekommendationer baserade på vetenskapliga bevis av hög kvalitet.
2) Regelbundna besök kommer att äga rum med de fastställda intervallen, beroende på de diagnostiska fynden, och under förutsättning att patienten är symtomfri och inte uppvisar några förändringar i symtomen (samstämmig rekommendation, låg evidenskvalitet):
- –
Ingen sjukdom: kontrollbesök med forcerad spirometri och Rx i bröstkorgen vart tredje år.
- –
Pleural sjukdom med pleurala plack: kontroll vart 1-3:e år med bröstkorgsröntgen och forcerad spirometri. Om patologiskt, komplettera undersökningen med fullständig lungfunktionsundersökning med volymer och DLCO.
- –
Pleurasjukdom med diffus pleuraförtjockning: årlig kontroll med lungröntgen och fullständig funktionsundersökning med volymer och DLCO.
- –
Pleurasjukdom på grund av asbest med rundad atelektasering: om typiska radiologiska tecken observeras, övervaka stabiliteten med tiden med bildgivande tekniker, företrädesvis CT var 6:e månad i 2 år. Efterföljande uppföljning liknande den för diffus pleuraförtjockning (samstämmig rekommendation, låg beviskvalitet). I avsaknad av typiska radiologiska tecken eller om symtom observeras, överväg andra tekniker (PET, PET-CT, CT-styrd FNAB) för att utesluta malignitet (samstämmig rekommendation, hög beviskvalitet).
- –
Asbestos: Årlig kontroll med Rx i bröstkorgen och fullständig funktionsundersökning. Vid försämrade lungfunktionstester eller radiologiska förändringar på Rx i bröstet bör man överväga att upprepa högupplöst CT.
- –
Antirökbehandling om patienten fortsätter att röka.
Förändringar i symtom, i lungfunktionstester eller i radiologiska studier kan föranleda en upprepad CT.
Varken bestämning av biomarkörer eller regelbunden CT är för närvarande indicerade för tidig upptäckt av mesoteliom (fig. 1).
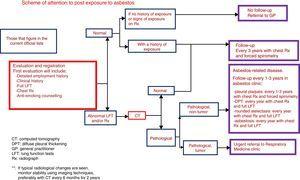
Besöksschema för patienter som tidigare exponerats för asbest.
Kriterier för att hänföra sjukdomar till asbest
Att hänföra en sjukdom till asbest har en diagnostisk betydelse som kommer att påverka den efterföljande övervakningen och kan också få rättsliga och ekonomiska konsekvenser, eftersom mesoteliom, asbestos, lungcancer och pleurafibros i samband med ventilationsbegränsning erkänns som arbetssjukdomar. Det faktum att asbest kan orsaka en hel rad luftvägssjukdomar gör inte tillskrivningen lättare i varje enskilt fall. Detta beror på att de tillgängliga epidemiologiska och experimentella uppgifterna visar att exponeringen måste uppfylla vissa kriterier i fråga om intensitet och varaktighet för att kunna betraktas som en orsak till en specifik sjukdom.
Som för andra sjukdomar som orsakas av inandning av ämnen krävs det för att diagnostisera processer som orsakas av asbest att man exponeras, att det finns en samstämmig klinisk och radiologisk bild och att man utesluter alla andra rimliga orsaker. Således innebär diagnosen mesoteliom vanligen att asbest tillskrivs, eftersom inget annat agens som tydligt orsakar sjukdomen har identifierats, och godartade pleurala sjukdomar uppvisar radiologiska tecken som kan göra dem lättare att känna igen.
Som en allmän regel måste exponeringens egenskaper utvärderas. Det är osannolikt att asbestos utvecklas med ackumulerade exponeringar som är lägre än 25 fibrer/ml/år,21 och ökningen av incidensen av lungcancer sker också efter intensiva exponeringar under längre tid än 20 år. Däremot kan godartade pleurasjukdomar uppträda efter 10 år från den första exponeringen, och exponeringen kan vara av lindrig intensitet.
I praktiken är patienten vanligtvis inte medveten om koncentrationen av fibrer som finns i arbetsmiljön, och det kan vara svårt för läkaren att utvärdera intensiteten i exponeringen utifrån den information som erhålls från anställningshistoriken. Faktum är att även vid användning av ett omfattande frågeformulär är känsligheten och specificiteten för att upptäcka exponering endast 50 % respektive 75 % när det gäller antalet AB som upptäcks i lungvävnad (personliga opublicerade uppgifter). När det gäller hushålls- eller miljöexponering är det svårare att fastställa orsakssambandet.
I patienter med en känd historia av exponering kan associerade sjukdomar tillskrivas denna exponering utan andra överväganden (konsekvent rekommendation, måttlig beviskvalitet).
Om det emellertid upptäcks diskrepanser mellan den kliniska bilden eller bildgivande undersökningar och uppfattningen om exponering är det användbart att ha objektiva bevis för exponering. Guldstandarden är påvisande av asbest i lungorna, fastställt genom testning för AB (avlagringar i lungsäcken är i allmänhet få). Värden som indikerar att det finns asbest i lungorna som kan orsaka sjukdom är 103AB/g i torr lunga eller mer än 106 fibrer/g, enligt uppgifter från det enda laboratorium i Spanien som har referensvärden15 . Denna teknik kan också utföras i bronkoalveolärt lavage, med tröskelvärden på 1AB/ml.
Uppkomsten av nya fibrer som har ersatt asbest och deras eventuella inverkan på hälsan granskas i tilläggsmaterialet, som finns tillgängligt online.
Interessentkonflikter
Författarna uppger att de inte har några intressekonflikter.