Uvolňování hormonůEdit
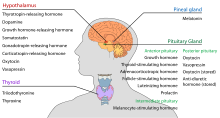
Hypotalamus má centrální neuroendokrinní funkci, především tím, že řídí přední část hypofýzy, která zase reguluje různé endokrinní žlázy a orgány. Uvolňující hormony (nazývané také uvolňující faktory) jsou produkovány v hypotalamických jádrech a poté transportovány po axonech buď do střední eminence, nebo do zadní hypofýzy, kde jsou ukládány a uvolňovány podle potřeby.
Přední hypofýza
V hypotalamo-adenohypofyzární ose se uvolňující hormony, známé také jako hypofyziotropní nebo hypotalamické hormony, uvolňují ze střední eminence, prodloužení hypotalamu, do hypofyzárního portálního systému, který je přenáší do přední hypofýzy, kde vykonávají regulační funkci na sekreci adenohypofyzárních hormonů. Tyto hypofyziotropní hormony jsou stimulovány parvocelulárními neurosekrečními buňkami umístěnými v periventrikulární oblasti hypotalamu. Po uvolnění do kapilár třetí komory putují hypofyziotropní hormony tzv. hypotalamo-hypofyzárním portálním oběhem. Jakmile tyto hormony dosáhnou svého cíle v přední hypofýze, vážou se na specifické receptory umístěné na povrchu buněk hypofýzy. V závislosti na tom, které buňky jsou touto vazbou aktivovány, hypofýza buď začne, nebo přestane vylučovat hormony do zbytku krevního oběhu.
| Sekreční hormon | Zkratka | Produkuje | Účinek |
|---|---|---|---|
| Hormon uvolňující tyrotropin (hormon uvolňující prolaktin) |
TRH, TRF, nebo PRH | Parvocelulární neurosekreční buňky paraventrikulárního jádra | Stimulují uvolňování hormonu stimulujícího štítnou žlázu (TSH) z přední hypofýzy (primárně) Stimulují uvolňování prolaktinu z přední hypofýzy |
| Kortikotropin-uvolňující hormon | CRH nebo CRF | Parvocelulární neurosekreční buňky paraventrikulárního jádra | Stimulují uvolňování adrenokortikotropního hormonu (ACTH) z přední hypofýzy |
| Dopamin (prolaktin-inhibující hormon) |
DA nebo PIH | Dopaminové neurony arcuate nucleus | Inhibují uvolňování prolaktinu z přední hypofýzy |
| Růstový-hormon uvolňující hormon | GHRH | Neuroendokrinní neurony arcuate nucleus | Stimulují růst-hormonu (GH) z přední hypofýzy |
| Hormon uvolňující gonadotropin | GnRH nebo LHRH | Neuroendokrinní buňky preoptické oblasti | Stimulují folikul-stimulující hormon (FSH) z přední hypofýzy Stimulují uvolňování luteinizačního hormonu (LH) z přední hypofýzy |
| Somatostatin (hormon inhibující růstový hormon) |
SS, GHIH, nebo SRIF | Neuroendokrinní buňky periventrikulárního jádra | Inhibují uvolňování růstového hormonu (GH) z přední hypofýzy Inhibují (mírně) uvolňování hormonu stimulujícího štítnou žlázu (TSH) z přední hypofýzy |
Mezi další hormony vylučované ze střední eminence patří vazopresin, oxytocin a neurotenzin.
Zadní hypofýza
V rámci hypotalamo-neurohypofyzární osy jsou neurohypofyzární hormony uvolňovány ze zadní hypofýzy, která je vlastně prodloužením hypotalamu, do oběhu.
| Vylučovaný hormon | Zkratka | Produkovaný | Účinek |
|---|---|---|---|
| Oxytocin | OXY nebo OXT | Magnocelulární neurosekreční buňky paraventrikulárního jádra a supraoptiku. jádra | Kontrakce dělohy Laktace (vypouštěcí reflex) |
| Vazopresin (antidiuretický hormon) |
ADH nebo AVP | Magnocelulární a parvocelulární neurosekreční buňky paraventrikulárního jádra, magnocelulární buňky supraoptického jádra | Zvýšení propustnosti pro vodu buněk distálního tubulu a sběrného kanálku v ledvinách a tím umožnění zpětného vstřebávání vody a vylučování koncentrované moči |
Je také známo, že hormony osy hypotalamus-hypofýza-nadledviny (HPA) mají vztah k některým kožním onemocněním a homeostáze kůže. Existují důkazy, které spojují hyperaktivitu hormonů HPA s kožními chorobami souvisejícími se stresem a kožními nádory.
StimulaceEdit
Hypotalamus koordinuje mnoho hormonálních a behaviorálních cirkadiánních rytmů, komplexní vzorce neuroendokrinních výstupů, složité homeostatické mechanismy a důležité způsoby chování. Hypotalamus proto musí reagovat na mnoho různých signálů, z nichž některé jsou generovány externě a některé interně. Signalizace delta vlnou vznikající buď v thalamu, nebo v kůře ovlivňuje sekreci uvolňujících hormonů; GHRH a prolaktin jsou stimulovány, zatímco TRH je inhibován.
Hypotalamus reaguje na:
- Světlo: délka dne a fotoperioda pro regulaci cirkadiánních a sezónních rytmů
- Čichové podněty, včetně feromonů
- Steroidy, včetně gonadálních steroidů a kortikosteroidů
- Nervově přenášené informace pocházející zejména ze srdce, enterického nervového systému (gastrointestinálního traktu) a reprodukčního traktu.
- Autonomní vstupy
- Podněty přenášené krví, včetně leptinu, ghrelinu, angiotenzinu, inzulinu, hormonů hypofýzy, cytokinů, plazmatických koncentrací glukózy a osmolarity atd.
- Stres
- Invaze mikroorganismů zvýšením tělesné teploty, resetování tělesného termostatu směrem nahoru.
Čichové podnětyEdit
Čichové podněty jsou důležité pro sexuální reprodukci a neuroendokrinní funkce u mnoha druhů. Například pokud je březí myš vystavena moči „cizího“ samce v kritickém období po souloži, pak těhotenství selže (Bruceův efekt). Samice myši si tak během soulože vytvoří přesnou „čichovou paměť“ svého partnera, která přetrvává několik dní. Feromonální signály napomáhají synchronizaci říje u mnoha druhů; u žen může synchronizovaná menstruace také vznikat na základě feromonálních signálů, ačkoli úloha feromonů u lidí je sporná.
Podněty přenášené krvíRedakce
Peptidové hormony mají důležitý vliv na hypotalamus, a aby tak mohly učinit, musí projít hematoencefalickou bariérou. Hypotalamus je částečně ohraničen specializovanými oblastmi mozku, které postrádají účinnou hematoencefalickou bariéru; endotel kapilár v těchto místech je fenestrovaný, aby umožnil volný průchod i velkých proteinů a dalších molekul. Některá z těchto míst jsou místy neurosekrece – neurohypofýza a střední eminence. Jiná místa jsou však místy, kde mozek odebírá vzorky složení krve. Dvě z těchto míst, SFO (subfornikální orgán) a OVLT (organum vasculosum lamina terminalis), jsou tzv. cirkumventrikulární orgány, kde jsou neurony v intimním kontaktu s krví i mozkomíšním mokem. Tyto struktury jsou hustě vaskularizované a obsahují osmoreceptivní a sodík-receptivní neurony, které řídí pití, uvolňování vazopresinu, vylučování sodíku a chuť na sodík. Obsahují také neurony s receptory pro angiotenzin, atriální natriuretický faktor, endotelin a relaxin, z nichž každý je důležitý pro regulaci rovnováhy tekutin a elektrolytů. Neurony v OVLT a SFO se promítají do supraoptického jádra a paraventrikulárního jádra a také do preoptických hypotalamických oblastí. Obvodové orgány mohou být také místem působení interleukinů, které vyvolávají horečku i sekreci ACTH prostřednictvím účinků na paraventrikulární neurony.
Není jasné, jak všechny peptidy, které ovlivňují hypotalamickou aktivitu, získávají potřebný přístup. V případě prolaktinu a leptinu existuje důkaz o aktivním vychytávání v choroidálním plexu z krve do mozkomíšního moku (CSF). Některé hypofyzární hormony mají negativní zpětnou vazbu na hypotalamickou sekreci; například růstový hormon se vrací zpět do hypotalamu, ale není jasné, jak se dostává do mozku. Existují také důkazy o centrálním působení prolaktinu.
Zjištění naznačují, že hormon štítné žlázy (T4) je vychytáván hypotalamickými gliovými buňkami v infundibulárním jádře/mediální eminenci a že je zde přeměňován na T3 pomocí dejodinázy typu 2 (D2). Následně je T3 transportován do neuronů produkujících hormon uvolňující tyreotropin (TRH) v paraventrikulárním jádře. V těchto neuronech byly nalezeny receptory pro hormony štítné žlázy, což naznačuje, že jsou skutečně citlivé na podněty T3. Kromě toho tyto neurony exprimovaly MCT8, transportér hormonů štítné žlázy, což podporuje teorii, že je do nich transportován T3. T3 by se pak mohl vázat na receptor pro hormony štítné žlázy v těchto neuronech a ovlivňovat produkci hormonu uvolňujícího tyreotropin, a tím regulovat produkci hormonů štítné žlázy.
Hypotalamus funguje jako určitý druh termostatu pro tělo. Nastavuje požadovanou tělesnou teplotu a stimuluje buď produkci a zadržování tepla za účelem zvýšení teploty krve na vyšší hodnotu, nebo pocení a rozšíření cév za účelem ochlazení krve na nižší teplotu. Všechny horečky jsou důsledkem zvýšeného nastavení hypotalamu; zvýšená tělesná teplota z jakékoli jiné příčiny se klasifikuje jako hypertermie. Vzácně způsobí horečku přímé poškození hypotalamu, například v důsledku cévní mozkové příhody; někdy se tomu říká hypotalamická horečka. Častěji však takové poškození způsobuje abnormálně nízkou tělesnou teplotu.
SteroidyEdit
Hypotalamus obsahuje neurony, které silně reagují na steroidy a glukokortikoidy – (steroidní hormony nadledvin, uvolňované v reakci na ACTH). Obsahuje také specializované neurony citlivé na glukózu (v arcuate nucleus a ventromediálním hypotalamu), které jsou důležité pro chuť k jídlu. Preoptická oblast obsahuje termosenzitivní neurony; ty jsou důležité pro sekreci TRH.
NeuralEdit
Sekrece oxytocinu v reakci na sání nebo vaginální stimulaci je zprostředkována některými z těchto drah; sekrece vazopresinu v reakci na kardiovaskulární podněty vycházející z chemoreceptorů v karotickém tělese a oblouku aorty a z nízkotlakých objemových receptorů síní je zprostředkována jinými. U potkana způsobuje stimulace pochvy také sekreci prolaktinu, což vede k pseudobřezosti po neplodném páření. U králíka vyvolává koitus reflexní ovulaci. U ovcí může stimulace děložního hrdla v přítomnosti vysokých hladin estrogenů vyvolat mateřské chování u panenské ovce. Všechny tyto účinky jsou zprostředkovány hypotalamem a informace jsou přenášeny především míšními drahami, které se přenášejí v mozkovém kmeni. Stimulace bradavek stimuluje uvolňování oxytocinu a prolaktinu a potlačuje uvolňování LH a FSH.
Kardiovaskulární podněty jsou přenášeny nervem vagus. Vagus také přenáší různé viscerální informace, včetně např. signálů vznikajících při roztahování nebo vyprazdňování žaludku, k potlačení nebo podpoře krmení, a to signalizací uvolňování leptinu, resp. gastrinu. Tyto informace se opět dostávají do hypotalamu prostřednictvím relé v mozkovém kmeni.
Kromě toho funkce hypotalamu reaguje na hladiny všech tří klasických monoaminových neurotransmiterů, noradrenalinu, dopaminu a serotoninu (5-hydroxytryptaminu), a je jimi regulována v těch drahách, z nichž dostává inervaci. Například noradrenergní vstupy vycházející z locus coeruleus mají důležité regulační účinky na hladiny hormonu uvolňujícího kortikotropin (CRH).
Řízení příjmu potravyEdit
| Peptidy, které zvyšují krmení. chování |
Peptidy, které snižují chování při krmení |
|---|---|
| Grelin | Leptin |
| Neuropeptid Y | (α,β,γ)-Melanocyty stimulující hormony |
| Agouti-related peptid | Kakainem a amfetaminem regulované transkripční peptidy |
| Orexiny (A,B) | Hormon uvolňující kortikotropin |
| Hormon koncentrující melanin | Cholecystokinin |
| Galanin | Insulin |
| Glukagon-podobný peptid 1 |
Krajní laterální část ventromediálního jádra hypotalamu je zodpovědná za kontrolu příjmu potravy. Stimulace této oblasti způsobuje zvýšený příjem potravy. Bilaterální léze této oblasti způsobuje úplné zastavení příjmu potravy. Mediální část jádra má řídící účinek na laterální část. Bilaterální léze mediální části ventromediálního jádra způsobuje hyperfagii a obezitu zvířete. Další léze laterální části ventromediálního jádra u téhož zvířete způsobí úplné zastavení příjmu potravy.
Existují různé hypotézy týkající se této regulace:
- Lipostatická hypotéza: Tato hypotéza tvrdí, že tuková tkáň produkuje humorální signál, který je úměrný množství tuku a působí na hypotalamus tak, že snižuje příjem potravy a zvyšuje výdej energie. Je zřejmé, že na hypotalamus působí hormon leptin, který snižuje příjem potravy a zvyšuje výdej energie.
- Gutpeptidová hypotéza: Gastrointestinální hormony jako Grp, glukagony, CCK a další údajně inhibují příjem potravy. Potrava vstupující do gastrointestinálního traktu vyvolává uvolňování těchto hormonů, které působí na mozek a vyvolávají pocit sytosti. Mozek obsahuje receptory CCK-A i CCK-B.
- Glukostatická hypotéza: Činnost centra sytosti ve ventromediálních jádrech se pravděpodobně řídí využitím glukózy v neuronech. Bylo postulováno, že když je jejich utilizace glukózy nízká, a tudíž když je rozdíl arteriovenózní glukózy v krvi přes ně nízký, aktivita přes neurony se snižuje. Za těchto podmínek je aktivita centra výživy nekontrolovaná a jedinec pociťuje hlad. Příjem potravy se rychle zvyšuje intraventrikulárním podáním 2-deoxyglukózy, a proto se snižuje utilizace glukózy v buňkách.
- Termostatická hypotéza: Podle této hypotézy snížení tělesné teploty pod danou požadovanou hodnotu stimuluje chuť k jídlu, zatímco zvýšení nad požadovanou hodnotu chuť k jídlu potlačuje.
Zpracování strachuEdit
Mediální zóna hypotalamu je součástí obvodu, který řídí motivované chování, například obranné chování. Analýzy značení Fos ukázaly, že řada jader v „sloupci kontroly chování“ je důležitá pro regulaci exprese vrozeného a podmíněného obranného chování.
Obranné chování proti predátorům
Vystavení predátorovi (např. kočce) vyvolává u laboratorních hlodavců obranné chování, i když zvíře nikdy nebylo kočce vystaveno. V hypotalamu tato expozice způsobuje zvýšení počtu buněk značených Fos v předním hypotalamickém jádru, v dorzomediální části ventromediálního jádra a ve ventrolaterální části premamilárního jádra (PMDvl). Preammillární jádro hraje důležitou roli v projevech obranného chování vůči predátorovi, protože léze v tomto jádře ruší obranné chování, jako je zamrznutí a útěk. PMD nemoduluje obranné chování v jiných situacích, protože léze tohoto jádra měly minimální vliv na skóre zmrazení po šoku. PMD má důležité spojení s dorzální periakveduktální šedou kůrou, která je důležitou strukturou pro vyjádření strachu. Kromě toho se u zvířat projevuje chování spojené s hodnocením rizika pro prostředí, které bylo dříve spojeno s kočkou. Analýza buněk značených Fos ukázala, že PMDvl je nejvíce aktivovanou strukturou v hypotalamu a inaktivace muscimolem před vystavením kontextu obranné chování ruší. Hypotalamus, hlavně PMDvl, má tedy důležitou roli v expresi vrozeného a podmíněného obranného chování vůči predátorovi.
Sociální porážka
Podobně má hypotalamus roli v sociální porážce: Jádra v mediální zóně jsou mobilizována i při setkání s agresivním konspecifikem. U poraženého zvířete dochází ke zvýšení hladiny Fos v sexuálně dimorfních strukturách, jako je mediální preoptické jádro, ventrolaterální část ventromediálního jádra a ventrální premamilární jádro. Tyto struktury jsou důležité pro další sociální chování, jako je sexuální a agresivní chování. Kromě toho se mobilizuje i premamilární jádro, a to jeho dorzomediální část, nikoli však ventrolaterální část. Léze v tomto jádře ruší pasivní obranné chování, jako je zamrznutí a postoj „na zádech“.