Hormonijärjestelmämme ymmärretään parhaiten, jos ajatellaan sitä kaskadina (kuva 1), jonka huipulla ovat aivot ja sen jälkeen aivolisäke, sitten kohde-elimet (esim. munasarjat, kilpirauhanen, kivekset) ja lopuksi fyysiset ja psyykkiset toiminnot (mm, ihon paksuus, kuukautiset, sukupuoliominaisuudet, aggressiivisuus, karvoituksen jakautuminen jne.).
Aivot
Hypotalamus on aivojen osa, josta hormonien vapautuminen lähtee liikkeelle, ja se käynnistää kaskadin erittämällä ”vapautushormoneja”, jotka käynnistävät aivolisäkkeen.
Aivolisäke
Aivolisäke tunnetaan nimellä ”isäntärauhasemme”. Se sijaitsee aivojemme tyvessä ja on suoraan yhteydessä hypotalamukseen erityisten hermojen ja verisuonten välityksellä. Vapautuvat hormonit kulkevat hypotalamuksesta aivolisäkkeeseen ja stimuloivat aivolisäkehormonien muodostumista ja vapautumista verenkiertojärjestelmäämme. Aivolisäkehormonit vaikuttavat moniin elimiin, kuten kilpirauhaseen, lisämunuaisiin, kiveksiin, munasarjoihin ja rintoihin.
Aivolisäkehormoneja, joista olemme kiinnostuneita, on viisi:
ihmisen kasvuhormoni (hGH)
Adrenokortikotrooppinen hormoni (ACTH)
Kilpirauhasen stimuloiva hormoni (TSH)
Follikkelia stimuloiva hormoni (FSH)
Luteinisoiva hormoni (LH)
Aivolisäkehormonit vapautuvat yleiseen verenkiertoon, ja niillä on vaikutuksia tiettyihin kohde-elimiin, jotka puolestaan vapauttavat omia hormonejaan. Aivolisäkehormonit toimivat siis kuin lennonjohtajat – ne kartoittavat paikan, määrittelevät, mitä tarvitaan, ja kertovat sitten elimistön elimille, milloin niiden on vapautettava hormoneja.
Kuvassa 1 on yleiskatsaus joihinkin tärkeimpiin hormoneihin.
Kuvio 1:
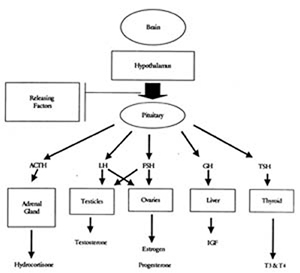
Ihmisen kasvuhormoni (hGH)
Ihmisen kasvuhormonilla on useita kohde-elimiä, mutta sen ensisijainen kohde on maksa, jossa se saa aikaan insuliinin kaltaisen kasvutekijän (IGF, a.k.a. Somatomedin C).
HGH:lla on monia aineenvaihdunnallisia vaikutuksia, joista hallitsevin on proteiinisynteesi. HGH vapautuu purskeina, joista suurin osa tapahtuu tiettyjen univaiheiden aikana. Kun kasvumme loppuu ja meistä tulee aikuisia, tuottamamme HGH:n määrä vähenee merkittävästi. IGF on hGH:n sivutuote, ja sen uskotaan olevan vastuussa suurimmasta osasta itse hormonin anabolisia (rakentavia) vaikutuksia. Onneksi IGF-pitoisuudet ovat veressä melko pysyviä ja niitä voidaan mitata helpommin kuin hGH:ta. Siksi me mittaamme veren IGF-tasot arvioidaksemme elimistössä kiertävän hGH:n määrää.
HGH on välttämätön luuston ja elinten kasvulle nuoruusiässä. Liian vähäinen määrä aiheuttaa kääpiöitymistä, liiallinen määrä aiheuttaa jättiläismäisyyttä. On hyvin selvää, että hGH:n ja IGF:n määrä alkaa laskea joskus 15-20 ikävuoden jälkeen, ja lasku jatkuu melko nopeasti. Vaikka hGH:ta ei enää sinänsä tarvita kasvuun aikuisiän saavuttamisen jälkeen, se on välttämätön monille muille elintärkeille toiminnoille, ja ikääntyessä havaittavan huomattavan alentuneen hGH:n määrän uskotaan olevan yhteydessä kaikkeen vähentyneestä energiasta painonnousuun (rasvaan) ja lihasmassan vähenemiseen.
Viime aikoina, jos aikuisen aivolisäke poistettiin tai tuhoutui kasvaimen vuoksi, hGH:ta ei korvattu, vaikka ”olennaisemmat” hormonit, kuten kilpirauhanen, hydrokortisoni ja testosteroni tai estrogeeni/progesteroni, korvattiin. Vasta tohtori B. Bengtssonin ja tohtori Daniel Rudmanin työ tunnusti kasvuhormonin arvon aikuisilla. Havaittiin, että GH-puutteisilla potilailla oli lähes 50 prosenttia odotettua korkeampi kuolleisuus sydänsairauksiin (kuva 4). Tohtori Bengtsson korvasi kasvuhormonin aivolisäkkeen vajaatoimintapotilailla ja saavutti erinomaisia tuloksia. Vuonna 1990 New England Journal of Medicine -lehdessä julkaistussa artikkelissa tohtori Rudman kertoi uraauurtavista kokeiluistaan hGH:n käytöstä iäkkäillä veteraaneilla. Hän havaitsi, että heidän ruumiinrasvansa väheni ja vähärasvainen lihasmassa, voima, ihon paksuus ja luuntiheys lisääntyivät. Toisin sanoen hän pystyi hidastamaan ikääntymisen tavanomaista etenemistä nostamalla potilaiden veren IGF-tasot nuorempaa ikäryhmää vastaaviksi. Vuonna 1999 National Institute on Aging sai valmiiksi toisen merkittävän tutkimuksen, jonka tarkoituksena oli joko kumota tai vahvistaa tohtori Rudmanin tulokset ja myös laajentaa hänen tutkimustaan mittaamalla muita parametreja. Kyseessä oli kaksoissokkoutettu, lumelääkekontrolloitu, monikeskustutkimus, johon osallistui sekä miehiä että naisia ja jossa oli suuri määrä potilaita. Tähän tutkimukseen osallistui hGH:n lisäksi myös sukurauhas- eli sukupuolisteroideja. Tämä tutkimus ei ainoastaan vahvistanut tohtori Rudmanin väittämiä hGH:n hyötyjä, vaan osoitti myös, että gonadoidien lisääminen paransi kasvuhormonin tehoa sekä miehillä että naisilla. Vaikka NIA:n tutkimus osoitti, että pelkkä hGH ei lisännyt lihasvoimaa, se lisäsi huomattavasti lihasmassaa ja aerobista kapasiteettia. Testosteronin lisääminen hGH:hen lisäsi kuitenkin lihasvoimaa huomattavasti. (Tämän tutkimuksen tulokset ovat saatavissa pyydettäessä.)
Ihmiskasvuhormonin (hGH)
Ihmiskasvuhormonin ottaminen nostaa IGF-1-tasoja veressä. Juuri korkeampi IGF-1 välittää kaikki hGH:lle liitetyt vaikutukset. Useimmat tutkimukset hGH:n käytöstä aikuisilla ja lapsilla eivät osoita kasvuhormonin käyttöön tai korkeampiin IGF-1-tasoihin liittyvää syöpäriskiä. Itse asiassa New England Journal of Medicine -lehdessä 14. lokakuuta 1999 julkaistussa katsausartikkelissa, jonka kirjoittajina olivat lääketieteen tohtori Mary Lee Vance ja lääketieteen tohtori Nellie Mauras, päädyttiin tyhjentävän kirjallisuushaun jälkeen siihen, että ”tällä hetkellä ei ole mitään näyttöä siitä, että kasvuhormonin modulaatio vaikuttaisi syöpäriskiin”. Kaikkien potilaiden tulisi kuitenkin olla tietoisia siitä, että on olemassa muita raportteja, jotka viittaavat siihen, että riski voi olla olemassa. Vuonna 1998 julkaistiin kaksi tutkimusta, joissa väitettiin eturauhassyövän esiintyvyyden olevan suurempi niillä miehillä, joiden IGF-1-tasot olivat korkeammat vuosia ennen syövän puhkeamista; useat asiantuntijat ovat kuitenkin samaa mieltä siitä, että nämä tutkimukset eivät ole yksiselitteisiä ja että ne voivat olla virheellisiä. Näihin tutkimuksiin liittyviä ongelmia ovat muun muassa tilastollinen analyysimenetelmä, verinäytteenoton ja syövän puhkeamisen välinen aika, joka oli useita vuosia, sekä IGF-mittausten puuttuminen syövän diagnoosin aikaan. Useat muut tutkimukset osoittavat, että IGF-1-tasoissa ei ole eroa normaalien terveiden miesten ja eturauhassyöpään sairastuneiden miesten välillä diagnoosin tekohetkellä ja sen jälkeen.
Toisessa hiljattain tehdyssä tutkimuksessa viitataan rintasyövän korkeampaan ilmaantuvuuteen ennen vaihdevuosi-iässä olevilla naisilla (mutta ei vaihdevuosi-iässä olevilla naisilla), joilla oli korkeammat IGF-1-pitoisuudet yhdestä viiteen vuotta ennen rintasyövän puhkeamista. Tässäkin tutkimuksessa veri otettiin ennen diagnoosia, eikä sitä analysoitu useiden vuosien ajan, mikä tekee tehdyistä johtopäätöksistä jokseenkin epäilyttäviä.
Vaikka suurin osa tutkimuksista viittaa ylivoimaisesti hGH:n turvallisuuteen, kuten lähes kaikilla lääketieteen aloilla, tutkimusten välillä on jonkin verran ristiriitaisia tietoja, jotka sekoittavat asiaa. Tämä johtuu ihmiskehon ja sen fysiologian monimutkaisesta luonteesta – ja siitä totuudesta, että lääketiede ei ole eksaktia tiedettä. Kuten kaikessa lääketieteellisessä terapiassa, jokaisen meistä on arvioitava saatavilla olevat tiedot sekä omat tarpeemme ja toiveemme ja suhteutettava ne mahdolliseen riskiin, jos sellainen on olemassa. Cenegenics®-lääkärisi voi auttaa sinua ymmärtämään ja arvioimaan kaikkea saatavilla olevaa tietoa mahdollisimman ennakkoluulottomasti. Ilmeisesti olemme sitä mieltä, että useimmille potilaille hGH-hoidosta saatava hyöty on paljon suurempi kuin riski – muuten emme harjoittaisi tämäntyyppistä lääketieteellistä käytäntöä. Vain sinä voit kuitenkin tehdä päätöksen itsellesi.
Kontekstiin liittyen voidaan todeta, että samankaltainen kiista on ympäröinyt estrogeenin käyttöä vaihdevuosien jälkeisissä naisissa viimeisten 30 vuoden ajan. Tiedämme nyt, että naisten estrogeenikorvaushoito saattaa lisätä rinta- ja endometriumsyövän riskiä joillakin naisilla, joilla on suvussa rintasyöpää ja muita riskitekijöitä. Koska estrogeenin on kuitenkin osoitettu suojaavan monilta muilta sairauksilta (Alzheimerin tauti, sydänsairaudet, osteoporoosi ja paksusuolen syöpä), kokonaiskuolleisuus on alhaisempi naisilla, jotka käyttävät estrogeenia, kuin naisilla, jotka eivät käytä. Kestää vielä vuosia, ennen kuin meillä on yhtä paljon tietoa hGH:sta kuin estrogeenista, mutta mielestämme useimmilla ihmisillä, joiden IGF-1-tasot ovat alhaiset, hGH:n käytön hyödyt ovat riskejä suuremmat.
Nämä tutkittuja ja julkaistuja hyötyjä ovat mm:
– Libidon lisääntyminen
– Kehon rasvan väheneminen
– Vähärasvaisen lihaksen lisääntyminen
– Luuntiheyden lisääntyminen
– Ihon paksuuden lisääntyminen
– Ihon ryppyjen väheneminen
– Kolesteroliprofiilin paraneminen
– Haavojen nopeampi paraneminen pienemmällä infektioiden määrällä
– Sairaalahoitojaksojen väheneminen 50 %:lla
. Sairauspoissaolopäivien väheneminen
– Liikuntakyvyn lisääntyminen
– Diastolisen verenpaineen väheneminen
– Vyötärön ja lantion suhteen väheneminen
– Munuaisverenvuodon lisääntyminen
– Hyvinvoinnin tunteen lisääntyminen/parantunut sosiaalinen kanssakäyminen
– Vahvistunut immuunijärjestelmä
Anecdotisesti väitettyihin hyötyihin kuuluu mm:
– Parantunut muisti
– Parantunut kognitiivinen toimintakyky
– Hiusten uusiutuminen
– Hämähäkkisuonten väheneminen
Mitä nämä hyödyt vähentävät kuolleisuutta ja pidentävätkö ne elinikää, ei selviä vielä moneen vuoteen. Se, mitä tiedämme, on se, että hGH:n käyttö parantaa merkittävästi elämämme laatua.
Kilpirauhashormoni
Kilpirauhashormoni vaikuttaa suuresti aineenvaihduntahäiriöihimme ja siten myös ruumiinlämpöömme. Ilman kilpirauhashormonia emme voi selviytyä. Alhainen kilpirauhashormonitaso aiheuttaa alentunutta ruumiinlämpöä, lisääntynyttä kolesterolia ja lisääntynyttä kehon rasvaa. Alhainen kilpirauhashormonitaso jää usein havaitsematta perinteisissä lääketieteellisissä hoitokäytännöissä, ja sen vuoksi laihduttaminen voi olla pirullisen vaikeaa. Ne voivat aiheuttaa subjektiivista velttoutta ja vähäistä energiaa sekä masennusta. Ikääntyessä kilpirauhasarvot laskevat toisinaan, jolloin kehon lämpötila ja aineenvaihdunta laskevat alle normaalin. Kilpirauhashormonin täydentäminen on helppoa ja edullista. Tavoitteena on palauttaa T3:n ja T4:n luonnolliset suhteet ja pitoisuudet veressä.
Kateenkorvan proteiini
Kateenkorvan rauhanen kutistuu iän myötä; 40-vuotiaana meillä saattaa olla vain pieni osa kateenkorvasta vielä ehjänä. Pidetään erittäin todennäköisenä, että tämä on osasyy ikään liittyvään heikentyneeseen immuniteettiin ja lisääntyneeseen syöpäriskiin.
Thymic Protein ATM (BioproTM) on hyödyllinen lisäämään immuniteettia ja vastustuskykyä syöpäsoluja ja infektioita vastaan. Tämä proteiini ohjelmoi T-4 ”auttajasoluja”, etsimään tunkeutujia, kuten viruksia, bakteereja ja syöpäsoluja. Tämän jälkeen auttajasolut lähettävät T-8-”tappajasoluja” etsimään tunkeutujia ja tuhoamaan ne. Tutkimukset ovat osoittaneet, että Thymic Protein ATM stimuloi immuniteettia ja tukahduttaa HIV:n. Tämä on sama proteiini, jota ihmisen kateenkorvan rauhanen tuottaa. Se luokitellaan ravintolisäksi ja otetaan suun kautta. Ylläpitoannos on yksi pakkaus päivässä kielen alle, ja se on erittäin tehokas.
Gonadaaliset steroidit
Nämä hormonit ovat välttämättömiä normaalille lisääntymistoiminnalle ja toissijaisille sukupuoliominaisuuksille. Niihin kuuluvat testosteroni, estrogeeni ja progesteroni.
Munuaiskuoren steroidit
Munuaisrauhaset vapauttavat hydrokortisonia (kortisolia) ja muita hormoneja, joita kutsutaan lisämunuaiskuoren steroideiksi. Ne ovat välttämättömiä elämälle, ja niillä on suuri merkitys vasteessamme fyysiseen ja emotionaaliseen stressiin. Yleensä ne eivät vähene iän myötä, kuten useimmat muut hormonimme.
Kaikki lisämunuais- ja sukurauhassteroidit ovat peräisin kolesterolin perusmolekyylistä. Useiden biosynteettisten reittien kautta kolesteroli muuntuu erilaisiksi steroidihormonimolekyyleiksi, ennen kuin siitä tulee estrogeenia, progesteronia tai testosteronia.
Pitäkää mielessä, että kun otamme pregnenolonia, DHEA:ta (dehydroepiandrosteronia) tai androstedionia, voimme vaikuttaa niiden lopputuotteiden: testosteronin, estrogeenin ja progesteronin tasoihin. Siksi on tärkeää seurata sekä annetun hormonin että sen lopputuotteiden tasoja.
Kuvassa 2 on esitetty eteneminen kolesterolimolekyylistä sukurauhas- ja lisämunuaiskuoren steroideihin.
Kuvio 2:
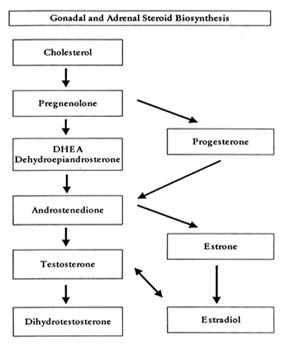
.