Mitä on koboltti
Koboltti (ääntäminen: KO-pultti) on kova, kiiltävä, hopeansininen alkuaine, joka kuuluu siirtymämetallien ryhmään, ja sitä edustaa kemiallinen symboli Co . Se on kemiallisesti aktiivinen ja voi muodostaa monia yhdisteitä . Se on ferromagneettinen metalli, joka voidaan magnetoida ja jota seostetaan nikkelin ja alumiinin kanssa voimakkaiden magneettien valmistamiseksi .

Koboltti Symboli
Isotoopit
Sillä on yksi vakaa, luonnossa esiintyvä isotooppi, 59Co ja 28 radioisotooppia, joista vakaimmat ovat 60Co, 57Co, 56Co ja 58Co, joiden puoliintumisajat ovat 5,2714 vuotta, 271,8 päivää, 77,27 päivää ja 70,86 päivää . Muiden radioisotooppien puoliintumisajat ovat alle 18 tuntia.
Missä kobolttia esiintyy
Kobolttia esiintyy luonnostaan yhdessä muiden alkuaineiden kanssa mineraalimalmeissa, kuten kobaliitissa (sulfidi, joka sisältää kobolttia, arseenia, rautaa ja nikkeliä), erytriitissä (hydratoitunut kobolttiarsenaatti) ja skutterudiitissa (kobolttiarsenaatti) . Sitä saadaan yleensä kupari- ja nikkelikaivostoiminnan sivutuotteena .
Merenpohjista löytyvät mangaanikiviesiintymät ovat valtavia siirtymämetallivarantoja, jotka sisältävät tonneittain kobolttia . Kolme suurinta kobolttivarantoja hallussaan pitävää maata ovat Kongon demokraattinen tasavalta, Australia ja Kuuba, kun taas kolme suurinta tuottajaa ovat Kongon demokraattinen tasavalta, Kiina ja Sambia .

Koboltti
Historia
Nimen alkuperä:
Kuka sen löysi: Alkuaineen löysi ruotsalainen kemisti ja mineralogi Georg Brandt .
Kun ja miten se löydettiin
Tutankhamonin, muinaisen Egyptin faaraon, joka hallitsi vuosina 1361-1352 eaa., haudassa oli syvänsininen lasiesine, joka oli valmistettu koboltista . Kiinassa koboltinsinistä käytettiin keramiikan lasitteiden valmistukseen .
Vanhan alkuperän lisäksi sen löytäminen viime aikoina juontaa juurensa 1730-luvulle, jolloin Georg Brandt oli kiinnostunut sinisestä malmista joistakin paikallisista kaivoksista . Lopulta hän onnistui osoittamaan, että sininen malmi sisälsi uutta metallia . Hän kuvasi sen ominaisuudet ja julkaisi tulokset vuonna 1739 .
Hänen löytönsä oli kiistanalainen, sillä muut kemistit kiistivät hänen havaintonsa monien vuosien ajan . Hänen ruotsalainen kemistitoverinsa Torbern Bergman teki kuitenkin lisätutkimuksia ja vahvisti Georg Brandtin löydön vuonna 1780 .
Koboltin tunnistaminen |
|||
| Atominumero | 27 | ||
| CAS-numero | 7440-48-4 | ||
| Sijoitus jaksollisessa järjestelmässä | Ryhmä | Jakso | Lohko |
| 9 | 4 | d | |
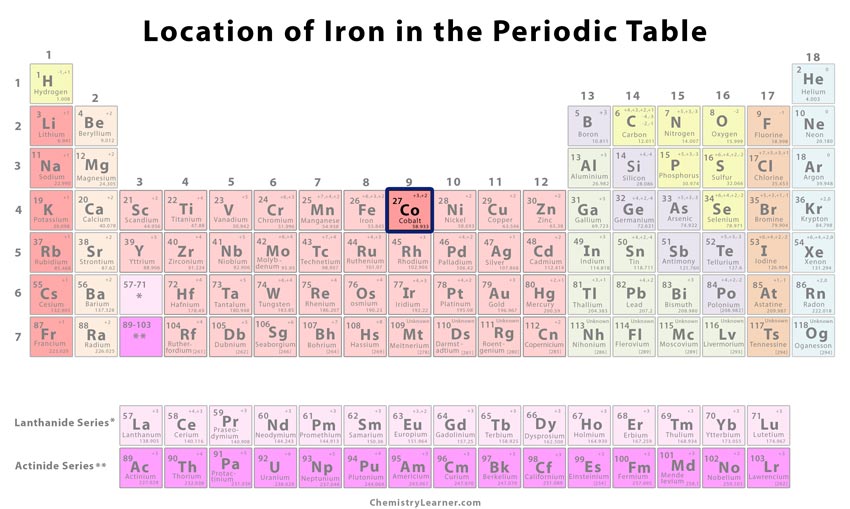
Missä sijaitsee koboltti jaksollisessa järjestelmässä
Koboltin ominaisuudet ja ominaisuudet
Yleiset ominaisuudet |
||||||||||||||||
| Relatiivinen atomimassa | 58.933 | |||||||||||||||
| Atomimassa | 58.933 amu | |||||||||||||||
| Molaarinen massa | 58.9331950 ± 0.0000050 g/mol | |||||||||||||||
| Molekyylipaino | 58.933 g/mol | |||||||||||||||
Fysikaaliset ominaisuudet |
||||||||||||||||
| Väri | Hopeansininen, sinertävän valkoinen | |||||||||||||||
| Sulamispiste/jäätymispiste | 1495 °C, 2723 °F | |||||||||||||||
| Kiehumispiste | 2927 °C, 5301 °F | |||||||||||||||
| Tiheys | 8.86 g cm-3 | |||||||||||||||
| Aineen olomuoto huoneenlämmössä (kiinteä/neste/kaasu) | Kiinteä | |||||||||||||||
| Kovuus | ||||||||||||||||
| – Brinell | 700 MPa | |||||||||||||||
| – Mohs | 5 | |||||||||||||||
| – Vickers | 1043 MPa | |||||||||||||||
| Sähkönjohtavuus | 1.7 X 107 S/m | |||||||||||||||
| Ionilataus | 3+ | |||||||||||||||
| Lämmönjohtavuus | 100 W/(m K) | |||||||||||||||
| Ominaislämpö | 421 J kg-1 K-1 | |||||||||||||||
| Massamoduuli | Tuntematon | |||||||||||||||
| Lujuusmoduuli | Tuntematon | |||||||||||||||
| Youngin moduuli | Tuntematon | |||||||||||||||
| Höyrynpaine | ||||||||||||||||
| – Lämpötila. (K) | 400 | 600 | 800 | 1000 | 1200 | 1400 | 1600 | 1800 | 2000 | 2200 | 2400 | |||||
| – Paine (Pa) | – | – | – | 2.09 X 10-10 | 1.00 X 10-6 | 4.19 X 10-4 | 0.0379 | 1.15 | 16 | – | – | |||||
Kemialliset ominaisuudet |
||||||||||||||||
| Hapetusasteet | 3, 2, 0, -1 | |||||||||||||||
| Isotoopit | Isotooppi | Massa | Liukumäärä (%) | Puoliintumisaika | Hajoamistapa | |||||||||||
| 59Co | 58.933 | 100 | – | – | ||||||||||||
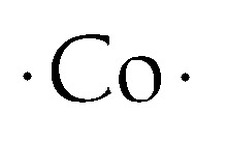
Koboltin Lewisin piste rakenne
Koboltin atomitiedot (alkuaine 27)
| Valenssielektronit | 9 | |||||||
| Kvanttiluvut | ||||||||
| – n | 3 | |||||||
| – ℓ | 2 | |||||||
| – mℓ | -1 | |||||||
| – ms | -1/2 | |||||||
| Elektronikonfiguraatio (jalokaasukonfiguraatio) | 3d74s2 | |||||||
| Atomin rakenne | ||||||||
| – Elektronien lukumäärä | 27 | |||||||
| – Neutronien lukumäärä | 32 | |||||||
| – Protonien lukumäärä | 27 | |||||||
| Atomin säde | ||||||||
| – Atomin säde | 2.00 Å | |||||||
| – Kovalenttinen säde | 1.18 Å | |||||||
| Elektronegatiivisuus (Pauling-asteikolla) | 1.88 | |||||||
| Elektronien affiniteetti | 63.873 kJ mol-1 | |||||||
| Ionisaatioenergia (kJ mol-1) | 1. | 2. | 3. | 4. | 5. | 6. | 7. | 8. |
| 760.402 | 1648.356 | 3232.3 | 4949.7 | 7670.6 | 9842 | 12437 | 15225.4 | |
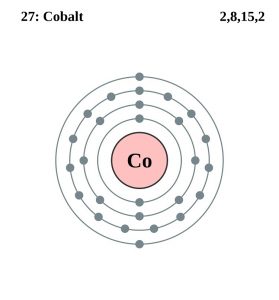
Koboltin elektronikonfiguraatio (Bohrin malli)
Mihin kobolttia käytetään
- Kobolttia seostetaan käytettäväksi kaasuturbiinigeneraattoreissa ja suihkuturbiineissa, koska se on lujuudeltaan ja korroosionkestävyydeltään korkea .
- Kobolttia käytetään toisinaan galvanoinnissa sen kovuuden ja houkuttelevan ulkonäön vuoksi .
- Kobolttia käytetään yleisesti katodimateriaalina litiumioniakuissa .
- Kobolttisuoloja käytetään antamaan voimakkaita sinisiä värejä lasille, posliinille, keramiikalle, emaleille ja maaleille .
- Radioaktiivista 60Co:ta käytetään syövän hoidossa ja elintarvikkeiden säteilyttämisessä taudinaiheuttajien hallitsemiseksi ja säilyvyysajan pidentämiseksi .
- Kromista, koboltista ja volframista koostuvia stelliittisuperseoksia käytetään korkeiden lämpötilojen ja suuren kulutuksen kestävien leikkuutyökalujen valmistukseen .
Koboltin myrkyllisyys ja terveysvaikutukset
Kobolttimyrkytys voi tapahtua, kun sitä vahingossa nautitaan, hengitetään tai se on kosketuksissa ihon kanssa suurina määrinä . Suurina määrinä koboltti voi olla karsinogeeninen ihmisillä ja joillakin eläimillä .
Kobolttia esiintyy ihmisessä pieniä määriä ja se on B12-vitamiinin välttämätön ainesosa . Pieniä annoksia kobolttia annetaan myös joillekin eläimille niiden kivennäisainepuutosten ehkäisemiseksi .

Kobolttimineraali (kobaliitti)
Interesting Facts
- Kobolttia kuvaa graafisesti ”koboldi” tai peikko (jota keskiaikaiset saksalaiset kaivostyöläiset pitivät kiusallisena), jonka taustalla on kiinalaista posliinia, mikä viittaa koboltin käyttöön muinaisessa Kiinassa keramiikkalasitteena .
- Koboltti voi säilyttää magneettiset ominaisuutensa aina 1121 °C:n lämpötilaan (Curie-piste) asti (2049.8 °F), joka on korkein kaikista ferromagneettisista alkuaineista .
- Saksalaiset tiedemiehet käyttivät kobolttiatomia vuonna 2010 kaapatakseen ensimmäiset kuvat spinin muuttumisesta .
Koboltin hinta
Puhtaan koboltin hinta on noin 0,21 dollaria grammalta, ja irtotavarana se maksaa noin 0 dollaria.044 per gramma .
- http://www.rsc.org/periodic-table/element/27/cobalt
- https://education.jlab.org/itselemental/ele027.html
- https://www.livescience.com/29275-cobalt.html
- https://www.chemicool.com/elements/cobalt.html
- https://education.jlab.org/itselemental/iso027.html
- https://www.webqc.org/molecular-weight-of-Co%28cobalt%29.html
- https://pubchem.ncbi.nlm.nih.gov/compound/cobalt#section=Top
- http://periodictable.com/Elements/027/data.html
- http://www.gpb.org/files/pdfs/gpbclassroom/chemistry/ionicChargesChart.pdf
- http://dwb4.unl.edu/Chem/CHEM869B/CHEM869BLinks/learn.chem.vt.edu/tutorials/bonding/valence.html
- http://chemistry-reference.com/q_elements.asp?Symbol=Co&language=en
- https://medlineplus.gov/ency/article/002495.htm