Abstract
Tavoitteet
Tunnistaa Barrettin ruokatorven (BE) esiintyvyys potilailla, joilla on nenä-nielun refluksitauti (NPR) ja jotka saapuvat tertiääriseen rinologian vastaanotolle vuonna 2017, ja arvioida, onko sillä yhteyttä oireisen gastroesofageaalisen refluksitaudin (GERD) esiintymiseen.
Menetelmät
Demografiset tiedot, itse raportoidut oireet ja merkityksellinen aikaisempi sairaushistoria koottiin standardoidusta vastaanottokyselylomakkeesta. Oireet ryhmiteltiin 3 luokkaan: NPR, laryngofaryngeaalinen refluksi (LPR) ja GERD. Kuvailevat ja ei-parametriset tilastolliset analyysit suoritettiin.
Tulokset
Vuonna 2017 vastaanotetuista 807 uudesta potilaasta 86 (10,7 %) ohjattiin gastroenterologian (GI) vastaanotolle NPR:ään liittyvien oireiden vuoksi, jotka perustuivat jo olemassa oleviin läheteindikaatioihin. Gastroenterologi arvioi 43 potilasta, ja 25 potilaalle tehtiin EGD, jonka patologinen raportti oli saatavilla tarkastelua varten. BE todettiin 6/25 potilaalla (24 %). Viisi näistä kuudesta potilaasta (83,3 %) ilmoitti joko lieviä tai ei lainkaan GERD-oireita. Mitkään potilastekijät tai oireet eivät olleet merkittävästi yhteydessä BE-diagnoosiin.
Johtopäätökset
Tämä peräkkäisiä uusia potilaita koskeva aineisto viittaa siihen, että NPR-potilaat noudattavat huonosti lähetteen antamista koskevia suosituksia ja että BE:n ilmaantuvuus tässä väestössä saattaa olla korkeampi kuin GERD-potilaiden keskuudessa yleensä raportoidaan. Tämä kokemus vahvistaa indikaatioita lähetteen antamiseksi EGD:hen BE:n poissulkemiseksi, ja se korostaa potilaskoulutuksen merkitystä vaatimusten noudattamisen parantamiseksi.
Avainsanat
Esofageaalinen syöpä, gastroesofageaalinen refluksi, seulonta, refluksiesofagiitti, kurkunpään refluksi, GERD
Esittely
Oireilevan gastroesofageaalisen refluksitaudin (GERD) tiedetään lisäävän potilaiden riskiä sairastua Barrettin ruokatorveen (BE). BE on laajalti tunnustettu syövän esiaste, jossa ruokatorven distaalisen limakalvon suojaava levyepiteeli korvautuu pylväsmäisellä suolen epiteelillä. BE:tä sairastavilla henkilöillä on paljon suurempi riski (arviolta 30-120 X>) sairastua ruokatorven adenokarsinoomaan (EAC) kuin väestöllä yleensä. Vaikka BE:n kehittymistä on aiemmin korostettu huolenaiheena niille, joilla on pitkäaikainen laryngofaryngeaalinen refluksi (LPR) , sitä ei ole kuvattu erityisenä huolenaiheena niille, joilla on pääasiassa nasofaryngeaalista refluksitautia (NPR), johon liittyy ekstrasofageaalisen refluksin (EER) nenäontelo- ja otologisia ilmenemismuotoja.
Mielenkiintoista on, että BE:tä havaitaan 1 – 2 %:lla kaikista potilaista, joille on tehty ruokatorven gastrofago- ja tuodensulkutähystysleikkaus (EGD) . Sen esiintyvyys on paljon suurempi niillä, joilla on oireinen GERD (5-15 %), ja se voidaan todeta useammin niillä, joilla on LPR-oireita (18 %). GERD-oireiden kesto korreloi BE:n suuremman todennäköisyyden kanssa, mutta GERD-oireiden vaikeusasteen ja BE:n kehittymisalttiuden välillä ei ole yhteyttä. Lisäriskitekijöinä BE:n kehittymiselle pidetään genetiikkaa, keskeistä lihavuutta, tupakointia, obstruktiivista uniapneaa (OSA) ja metabolista oireyhtymää .
Vuonna 2018 ilmeni kaksi huolenaihetta, jotka liittyivät Floridan Sinus & Nasal Institute of Floridan (SNI) -laitoksessa (Sinus & Nasal Institute of Florida, SNI) vastaanotettaviin EER-potilaisiin, ja jotka saivat aikaan sen johdosta tämän laadunarviointi- ja -parannushankkeen (Quality Assessment and Improvement (QAI) -hankkeen aloittamisen. Ensinnäkin kaksi hiljaista refluksipotilasta kielsi olevansa tietoisia biopsialla todistetusta BE-diagnoosistaan. Lisäksi nämä kaksi potilasta noudattivat huonosti suositeltuja ruokavaliotoimenpiteitä, elämäntapamuutoksia ja lääkkeitä. Lisäksi he eivät ymmärtäneet myöhemmän EGD:n merkitystä BE:n seurannassa. Toiseksi huomattava osa hiljaista refluksitautia sairastavista potilaista, joita kehotettiin käymään gastroenterologin vastaanotolla, ei noudattanut tätä suositusta.
Tämän tiedonannon tarkoituksena on jakaa laadunarviointi- ja laadunparannusohjelmamme (QAI-ohjelma) tulokset, jotka koskevat tertiäärisen rinologian kokemusta hiljaisesta refluksista ja BE:stä. Erityisesti tämän tiedonannon tarkoituksena on tutkia BE:n esiintyvyyttä NPR-potilailla ja tunnistaa niiden potilaiden prosenttiosuus, jotka jättivät huomiotta GI-lähetteen tärkeyden.
Menetelmät
Osana meneillään olevaa laadunarviointiohjelmaa kaikki uudet SNI-potilaat, jotka ohjattiin gastroenterologian (GI) vastaanotolle vuonna 2017, tunnistettiin sähköistä potilastietokantaa (EMR) hyödyntäen. Taulukossa 1 on lueteltu SNI:n vuoden 2017 lähetekriteerit GI:lle. Demografiset tiedot, itse ilmoitetut oireet, merkityksellinen aikaisempi sairaushistoria ja BMI, jotka liittyvät ruokatorven ulkopuolisen refluksin kliiniseen epäilyyn, koottiin standardoidusta vastaanottokyselylomakkeesta. Kerättyihin tietoihin sisältyivät itse raportoitu vakavuus: Nenän tukkoisuus, värjäytynyt nenäverenvuoto, nenäverenvuodon jälkeinen vuoto, nenäverenvuodon kesto, inhalaatioallergian oireet (sarveiskalvotulehdus), korvien täyteys, korvien naksuminen, äänen käheys, pahanhajuinen hengitys, kuolaaminen, tukehtuminen ruokaan, astman paheneminen, yskä, ruoansulatushäiriöt, närästys, nielemisvaikeudet ja nielemiskipu. Myös OSA:n ja tupakoinnin kannalta merkittävät aiemmat sairaushistoriat kirjattiin. Niiden osalta, joille tehtiin EGD, tarkasteltiin toimenpidelöydöksiä ja patologisia raportteja. Histopatologiset raportit vahvistivat BE:n esiintymisen tai puuttumisen.
Vertailun vuoksi itse raportoidut EER-oireet, jotka saatiin standardoidusta rinologian vastaanottokyselylomakkeesta, ryhmiteltiin kolmen anatomisen sijainnin perusteella: 1) Nenäontelo/nasofarynx NPR:n osalta; 2) kurkunpää/hypo-orofarynx LPR:n osalta; 3) ruokatorvi GERD:n osalta. NPR-oireet ovat: Nenän tukkoisuus, värjäytynyt nenävuoto, nenäontelon jälkeinen vuoto (PND), korvan täyteys ja korvan naksuminen. LPR koostui seuraavista oireista: äänen käheys, pahanhajuinen hengitys, kuolaaminen, tukehtuminen ruokaan, astman paheneminen ja yskä. GERD-oireet koostuivat ruoansulatushäiriöistä, närästyksestä, nielemisvaikeuksista ja nielemiskivusta.
Statistinen analyysi suoritettiin käyttäen Jamovi Version 0.9:ää (The jamovi project 2019 https://www.jamovi.org). Jatkuvien tietojen vertailuun kahden ryhmän välillä käytettiin Mann-Whitneyn U-testiä. Verrattaessa kategorisia tietoja kahden ryhmän välillä käytettiin Fisherin tarkkaa testiä.
Populaatio & oireet
Sähköisen potilastietojärjestelmämme EMR-ohjelmiston tietokonepohjainen rekisteriraportti tunnisti 807 uutta potilasta, jotka nähtiin SNI:ssä vuonna 2017. Näistä 86 (10,7 %) ohjattiin samana vuonna GI:hen yhden tai useamman taulukossa 1 luetellun indikaation vuoksi. Näistä 86 potilaasta 48 (55,8 %) oli naisia, ja keski-ikä oli 55 (15-83). Kuusikymmentäyksi potilasta (70,9 %) ohjattiin GI:hen ensikäynnin yhteydessä. Neljäkymmentäkolme potilasta (50 %) oli gastroenterologin vastaanotolla. GI:hen ohjatuista 86 potilaasta 79:llä oli täytetyt kyselylomakkeet ensimmäiseltä käynniltään käytettävissä tarkastelua varten. Taulukossa 2 on esitetty oireet, jotka oli luokiteltu lähetettyjen potilaiden, EGD:n läpikäyneiden potilaiden ja potilaiden, joilla oli biopsialla todistettu BE, mukaan.
Taulukko 1: GI:n lähetteen SNI-kriteerit. Näytä taulukko 1
Taulukko 2: Refluksiin liittyvät oireet ensikäynnillä. Näytä taulukko 2
Vähintään yksi NPR-oire esiintyi kaikilla 79 lähetetyllä potilaalla, joilla oli täytetty kyselylomake. Nenän vuotaminen oli yleisin oire, jota raportoitiin 73/79:llä (92,4 %) kaikista gastroenterologiaan lähetetyistä potilaista ja 100 %:lla potilaista, joille tehtiin EGD. Nenän vuotamista ja/tai korvien täyttymistä/napsautusta esiintyi 75/79 (94,9 %) potilaalla kaikista potilaista. Vähintään yksi LPR-oire esiintyi 69 potilaalla (87,3 %), mutta vain 44 potilaalla (55,7 %) oli yksi tai useampi GERD-oire. NPR-, LPR- tai GERD-oireissa ei ollut tilastollista eroa kolmen potilasryhmän välillä: 1) GI:hen ohjatut, 2) EGD:n läpikäyneet tai 3) BE:tä sairastavat.
BE:tä sairastavilla potilailla kaikilla oli NPR-oireita, 4:llä (66,7 %) esiintyi LPR-oireita ja 4:llä (66,7 %) esiintyi GERD-oireita. Kuitenkin vain yhdellä BE-potilaalla oli merkittäviä GERD-oireita ja loput olivat lieviä ilman merkittävää vaikutusta elämänlaatuun. Niistä potilaista, joilla ei ollut BE:tä, 7:llä (36,8 %) oli GERD-oireita ja 17:llä (89,5 %) LPR-oireita. Kun verrattiin potilaita, joilla oli ja ei ollut BE:tä, joilla oli ja ei ollut refluksiesofagiittia ja joilla oli ja ei ollut gastriittia, oireiden välillä ei ollut merkittävää eroa. Esiintyvien oireiden osalta ei ollut merkittävää eroa näiden 79 potilaan ja niiden 25 potilaan välillä, joille oli tehty EGD, tai niiden 6 potilaan välillä, joilla oli BE. Vaikka protonipumpun estäjän (PPI) käyttöaihetta ensimmäisellä rinologisella vastaanotolla ei voitu määrittää retrospektiivisesti, 50 % BE-potilaista ja 26,3 % potilaista, joilla ei ollut BE:tä, käytti jo PPI:tä.
EGD & Patologian tulokset
EGD tehtiin 25/86:lle (29,1 %). BE varmistui 6/25 (24 %) potilaalla (kuva 1 ja kuva 2), joista yhdellä oli matala-asteinen dysplasia. Yhdelläkään ei ollut korkea-asteista dysplasiaa tai pahanlaatuisuutta. Vain 2/6 potilaalla, joilla oli BE, ja 11/19 potilaalla, joilla ei ollut BE:tä, oli endoskooppinen todiste ruokatorvitulehduksesta, joka oli vahvistettu patologisesti. Toisin sanoen BE:hen ei aina liittynyt histopatologista näyttöä esofagiitista. Yksi BE-diagnoosin saanut potilas ei ollut riittävän tietoinen tästä diagnoosista, ennen kuin lähettävä rinologian erikoislääkäri hankki patologisen lausunnon. Gastriitti vahvistettiin histopatologisesti 21/25 (84 %) EGD-potilaalla. Kahdeksalla oli aktiivinen gastriitti ja 13:lla inaktiivinen gastriitti. Gastriitti todettiin kaikilla BE-potilailla ja 78,9 %:lla potilaista, joilla ei ollut BE:tä.
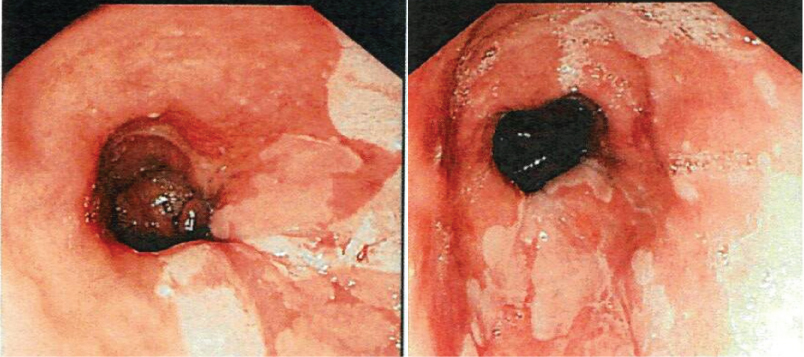 Kuva 1: EGD-kuvat, joissa näkyy ruokatorveen ruokatorven liittymästä ruokatorven sisään ulottuvia lohenpunaisia limakalvojen laikkuja, jotka sopivat suoliston metaplasiaan. Näytä kuva 1
Kuva 1: EGD-kuvat, joissa näkyy ruokatorveen ruokatorven liittymästä ruokatorven sisään ulottuvia lohenpunaisia limakalvojen laikkuja, jotka sopivat suoliston metaplasiaan. Näytä kuva 1
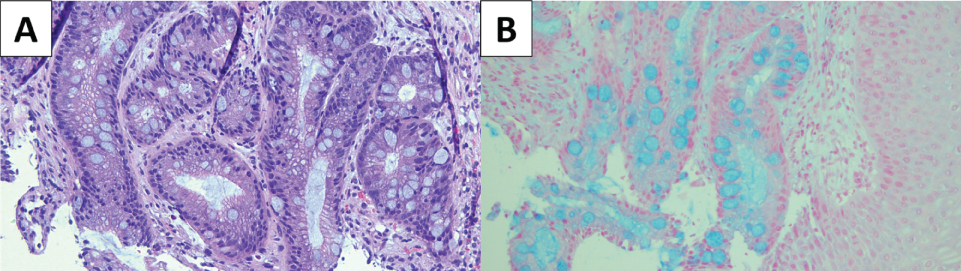 Kuva 2: (A) Hematoksyliini-&eosiini- (H&E) -värjätty preparaatti Barrettin ruokatorvesta; (B) Alcian-sinivärjäys korostaa pikarisolujen läsnäoloa, jotka liittyvät metaplastiseen suolen epiteeliin. Näytä kuva 2
Kuva 2: (A) Hematoksyliini-&eosiini- (H&E) -värjätty preparaatti Barrettin ruokatorvesta; (B) Alcian-sinivärjäys korostaa pikarisolujen läsnäoloa, jotka liittyvät metaplastiseen suolen epiteeliin. Näytä kuva 2
Kään potilaan ilmoittamista oireista ei eronnut merkittävästi niiden EGD-potilaiden välillä, joilla oli ja joilla ei ollut biopsialla todistettua BE:tä.
Keskustelu
Kun harvinainenkin, EAC:n ennuste on huono, ja sen arvioitu viiden vuoden eloonjäämisprosentti on 17 % . Kuten BE:n yleistyminen viime vuosikymmeninä, myös EAC:n määrä on lisääntynyt dramaattisesti (300-500 %) viimeisten 30-40 vuoden aikana. Jälleen kerran EAC:n kehittymisen riski kasvaa BE:n esiintyessä 30-125-kertaiseksi verrattuna väestöön yleensä . Kaiken kaikkiaan BE:n eteneminen EAC:ksi on arviolta 0,1-0,3 % vuosittain.
Kliinisissä BE:n diagnosointia ja hoitoa koskevissa ohjeissa suositellaan seulomaan potilaat, joilla on useita riskitekijöitä . EAC:n ja BE:n julkaistuja riskitekijöitä ovat yli 50 vuoden ikä, miespuolisuus, valkoihoinen rotu, lihavuus, tupakointi, BE:n tai EAC:n esiintyminen suvussa ja krooniset GERD-oireet . Pienessä QAI-populaatiossamme lihavuutta, ikää ja sukupuolta ei havaittu BE:n riskitekijöinä. Tupakointihistoria, OSA ja harvinainen tai lievä närästys osoittivat taipumusta olla riskitekijöitä.
Jos BE havaitaan, lisäseurantaa toteutetaan säännöllisesti dysplasian tai varhaisen pahanlaatuisuuden diagnosoimiseksi. BE:n endoskooppinen seuranta on yhdistetty parempiin tuloksiin EAC:n kuolleisuuden suhteen . On syytä huomata, että 50 prosenttia potilaista, joilla on BE tai EAC, ei ilmoita kroonisia refluksioireita. Yleisväestön EGD-seulontaa ei kuitenkaan suositella. Aiemmin on suositeltu, että LPR-oireet olisi sisällytettävä BE:n ja syövän seulonnan indikaatioihin.
EER eli hiljainen refluksi on kliininen diagnoosi, joka yleensä perustuu ENT-oireisiin, fyysisen tutkimuksen löydöksiin (mukaan lukien nenä-, kurkunpään- ja kurkunpään tähystys) ja testeihin, jotka on tilattu muiden ENT-sairauden selittävien tekijöiden poissulkemiseksi (esim. CT-selektiivinen sivuonteloiden tähystyskuvaus, allergiatutkimus). Hiljaisen refluksidiagnoosin varmistaminen on usein vaikeaa, kun potilaalla ei ole koskaan tai on harvoin GI-oireita. Valitettavasti mikään yksittäinen testi ei voi sulkea pois hiljaisen refluksin olemassaoloa. Tältä osin ehdotetaan, että ”vasteen puuttuminen aggressiiviseen happosuppressiiviseen hoitoon yhdistettynä normaaliin pH-testaukseen ilman hoitoa tai impedanssi-pH-testaukseen hoidon aikana vähentää merkittävästi todennäköisyyttä, että refluksi on myötävaikuttanut ruokatorven ulkopuolisten oireiden etiologiaan”. Näilläkään toimenpiteillä ei voida täysin sulkea pois EER:ää selittämättömien nenänielun oireiden, kuten nielun jälkeisen tiputtelun, selittäjänä. Tämä QAI-kokemus tukee käsityksiä, joiden mukaan BE:hen liittyy oireinen NPR, ei vain LPR ja GERD.
Koska hiljaiset refluksioireet ovat yleensä ärsyttäviä eivätkä hengenvaarallisia, monet potilaat turhautuvat helposti ja hylkäävät hoidon, kun he eivät näe nopeaa hoitovastetta. Hiljaisen refluksin diagnoosi haastaa usein potilaan luottamuksen lääkärin diagnostisiin kykyihin ja hoitosuunnitelmaan. Potilaat ovat tällöin haluttomia tekemään invasiivisia testejä refluksitautidiagnoosin vahvistamiseksi. Tämä saattaa osaltaan selittää QAI:n havainnon, jonka mukaan 50 % ei tehnyt gastroenterologista arviointia.
Postnasaalinen tyhjennys määritellään tässä yhteydessä nenän hengitysteistä lähtevän ja kurkkuun valuvan ärsyttävän tyhjennyksen tunteeksi. PND:n katsotaan tyypillisesti johtuvan poskionteloiden tulehdussairaudesta, mutta tiedot viittaavat siihen, että NPR voi esiintyä ei-allergisen nuhan muotona. Eräässä plasebokontrolloidussa tutkimuksessa osoitettiin, että kahdesti päivässä annettava protonipumppuhoito paransi PND:tä potilailla, joilla ei ollut näyttöä nenän sivuontelotulehduksesta tai allergiasta.
Tämä QAI-kokemus tuo esiin mahdollisen yhteyden refraktorisen NPR:n ja BE:n välillä närästyksen kanssa tai ilman sitä. Postnasaaliset ja otologiset oireet olivat yleisimpiä oireita EGD:hen ohjatuilla. Tämä QAI-hanke viittaa myös siihen, että tupakointihistoria ja obstruktiivinen uniapnea ovat riskejä ruokatorvitulehduksen ja/tai BE:n kehittymiselle, kuten aiemmin muualla on kuvattu. BE:n 25 prosentin esiintyvyyden perusteella tässä pienessä, itse valitussa väestössä uskomme, että ne potilaat, joilla epäillään NPR:ää, olisi sisällytettävä suositukseen EGD:n suorittamisesta. Tämä QAI-hanke viittaa siihen, että lisätutkimukset ovat tarpeen, ennen kuin voidaan tehdä varmoja johtopäätöksiä.
Tämän QAI-raportin haittapuolia ovat sen retrospektiivinen luonne ja pieni otoskoko sekä epäjohdonmukainen indikaatio PPI:iden käytölle sekä niillä potilailla, joilla oli että ei ollut BE:tä EGD:n yhteydessä. Potilaiden sisätautilääkäri tai lähettävä korva- ja nielulääkäri on saattanut määrätä PPI:n käytön EER-oireiden vuoksi tai vaihtoehtoisesti potilaat ovat saattaneet käyttää itsehoitoa oireisen GERD:n vuoksi. PPI:n käytössä ei kuitenkaan ollut eroa BE:tä sairastavien ja BE:tä sairastamattomien välillä.
Yhteenveto
Barrettin ruokatorvi tunnistettiin 24 %:lla itse valituista, peräkkäisistä uusista tertiäärisistä nuhapotilaista, joille tehtiin EGD. Tämä määrä on huomattavasti suurempi kuin GERD:tä ja LPR:ää koskevien julkaistujen tietojen perusteella odotettiin. Tämä QAI-kokemus vahvistaa indikaatioita ohjata potilaat gastroenterologiaan EGD:tä varten BE:n poissulkemiseksi. Ajoittaisen lievän närästyksen, tupakoinnin ja OSA:n pahentavat tekijät lähestyivät tilastollista merkitsevyyttä BE:n riskitekijänä, mutta eivät saavuttaneet sitä. Niissä potilaissa, joilla oli ruokatorvitulehdus, oli huomattavasti enemmän potilaita, joilla oli OSA.
Lähes puolet GI:hen ohjatuista uusista nuhapotilaista ei noudattanut lähetettä. BE:n merkityksen selittäminen EAC:n riskitekijänä voi auttaa motivoimaan potilaita noudattamaan GI-lähetteen suositusta. Jos BE:n löydös on olemassa, parempi potilasymmärrys todennäköisesti auttaa potilasta noudattamaan hoito- ja seurantasuosituksia.Tämänkaltaiset QAI-ohjelmat ovat potilaan hoidon parantamisen kulmakivi.
Kiitokset
Haluamme kiittää sekä Arthur Bermania, DO:ta endoskooppisten kuvien toimittamisesta että Kern Davisia, MD:tä patologisten kuvien toimittamisesta.
Rahoitus
Tämä hanke ei saanut erityistä avustusta miltään julkiselta, kaupalliselta tai voittoa tavoittelemattomalta rahoittajalta.
Declaration of Conflicting Interests
Tekijät ilmoittavat, ettei eturistiriitoja ole.
- Runge TM, Abrams JA, Shaheen NJ (2015) Epidemiology of Barrett’s esophagus and esophageal adenocarcinoma. Gastroenterol Clin North Am 44: 203-231.
- Reavis KM, Morris CD, Gopal DV, Hunter JG, Jobe BA (2004) Laryngofaryngeaaliset refluksioireet ennustavat ruokatorven adenokarsinooman esiintymistä paremmin kuin tyypilliset gastroesofageaaliset refluksioireet. Ann Surg 239: 849-856.
- Halum SL, Postma GN, Bates DD, Koufman JA (2006) Incongruence between histologic and endoscopic diagnoses of Barrett’s esophagus using transnasal esophagoscopy. Laryngoscope 116: 303-306.
- Shaheen NJ, Falk GW, Iyer PG, Gerson LB (2016) ACG Clinical Guideline: Diagnosis and Management of Barrett’s Esophagus. Am J Gastroenterol 111: 30-50.
- Hammad TA, Thrift AP, El-Serag HB, Husain NS (2019) Missed Opportunities for Screening and Surveillance of Barrett’s Esophagus in Veterans with Esophageal Adenocarcinoma. Dig Dis Sci 64: 367-372.
- Vaezi MF, Katzka D, Zerbib F (2018) GERD:hen liittyvät ekstraesofageaaliset oireet ja sairaudet: Missä heiluri heiluu nyt? Clin Gastroenterol Hepatol 16: 1018-1029.
- Vaezi MF, Hagaman DD, Slaughter JC, Tanner SB, Duncavage JA, ym. (2010) Protonipumpun estäjähoito parantaa oireita postnasaalisessa tyhjennyksessä. Gastroenterology 139: 1887-1893.
Sitaatti
Chislett SP, Kalathia J, Solyar AY, Limjuco AP, Lanza DC (2020) Nasopharyngeal Reflux: A New Indication for Esophagogastroduodenoscopy to Rule Out Barrett’s Esophagus?. J Otolaryngol Rhinol 6:093. doi.org/10.23937/2572-4193.1510093
.