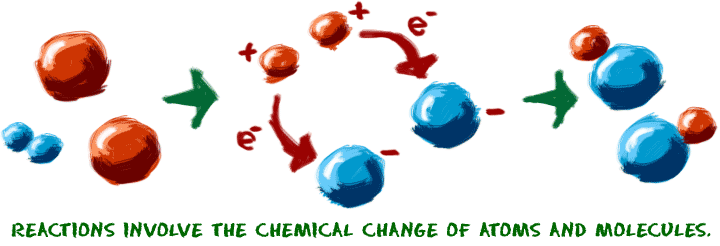
Débutons avec l’idée d’une réaction chimique. Les réactions se produisent lorsque deux ou plusieurs molécules interagissent et que les molécules changent. Les liaisons entre les atomes sont brisées et créées pour former de nouvelles molécules. C’est tout. Quelles sont ces molécules ? Comment interagissent-elles ? Que se passe-t-il ? Les possibilités sont infinies.
Lorsque vous essayez de comprendre les réactions chimiques, imaginez que vous travaillez avec les atomes. Imaginez que les blocs de construction sont juste en face de vous sur la table. Parfois, nous utilisons nos jouets de chimie pour nous aider à visualiser le mouvement des atomes. Nous branchons et débranchons les petits connecteurs qui représentent les liaisons chimiques. Il y a quelques points clés que vous devez savoir sur les réactions chimiques :
1. Un changement chimique doit se produire. On commence avec une molécule et on la transforme en une autre. Des liaisons chimiques sont établies ou rompues afin de créer une nouvelle molécule. Un exemple de réaction chimique est la rouille d’une poubelle en acier. Cette rouille se produit parce que le fer (Fe) du métal se combine avec l’oxygène (O2) de l’atmosphère. Des liaisons chimiques sont créées et détruites pour finalement donner de l’oxyde de fer (Fe2O3).  Lorsqu’un réfrigérateur ou un climatiseur refroidit l’air, il n’y a pas de réaction dans les molécules d’air. Le changement de température est un changement physique. Lorsque vous faites fondre un glaçon, c’est un changement physique. Lorsque vous mettez de l’eau de Javel dans la machine à laver pour nettoyer vos vêtements, un changement chimique brise les molécules de vos taches.
Lorsqu’un réfrigérateur ou un climatiseur refroidit l’air, il n’y a pas de réaction dans les molécules d’air. Le changement de température est un changement physique. Lorsque vous faites fondre un glaçon, c’est un changement physique. Lorsque vous mettez de l’eau de Javel dans la machine à laver pour nettoyer vos vêtements, un changement chimique brise les molécules de vos taches.
2. Une réaction peut inclure des atomes, des ions, des composés ou des molécules d’un seul élément. Tu dois te rappeler qu’une réaction chimique peut se produire avec n’importe quoi, du moment qu’un changement chimique se produit. Si vous mettez de l’hydrogène pur (H2) et de l’oxygène pur dans une pièce, ils pourraient être impliqués dans une réaction pour former de l’eau (H2O). Cependant, ce sera en très très petites quantités. Si vous ajoutez une étincelle, ces gaz seront impliqués dans une réaction chimique violente qui se traduira par une énorme explosion (exothermique). Une autre réaction chimique pourrait inclure des ions argent (Ag+). Si vous mélangez une solution avec des ions argent avec une solution qui a des ions chlorure (Cl-), le précipité de chlorure d’argent (AgCl) se formera et tombera de la solution.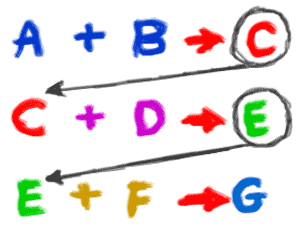 3. Les réactions uniques se produisent souvent dans le cadre d’une plus grande série de réactions. Lorsqu’une plante fabrique des sucres, il peut y avoir jusqu’à une douzaine de réactions chimiques pour passer par le cycle de Calvin et finalement créer (synthétiser) des molécules de glucose (C6H12O6). L’exemple de la rouille que nous avons utilisé précédemment ne vous a montré que les réactifs initiaux et les produits finaux de la réaction chimique. Il y avait plusieurs réactions intermédiaires où des liaisons chimiques étaient créées et détruites. L’exemple du chlorure d’argent ne portait que sur les ions. En réalité, les deux solutions ont été créées lorsque deux sels se sont dissociés (divisés en ions) dans l’eau.
3. Les réactions uniques se produisent souvent dans le cadre d’une plus grande série de réactions. Lorsqu’une plante fabrique des sucres, il peut y avoir jusqu’à une douzaine de réactions chimiques pour passer par le cycle de Calvin et finalement créer (synthétiser) des molécules de glucose (C6H12O6). L’exemple de la rouille que nous avons utilisé précédemment ne vous a montré que les réactifs initiaux et les produits finaux de la réaction chimique. Il y avait plusieurs réactions intermédiaires où des liaisons chimiques étaient créées et détruites. L’exemple du chlorure d’argent ne portait que sur les ions. En réalité, les deux solutions ont été créées lorsque deux sels se sont dissociés (divisés en ions) dans l’eau.
Wikipedia : Réactions chimiques
Encyclopédie.com : Réactions chimiques
Rhode Island College : Reactions