Iniziamo con l’idea di una reazione chimica. Le reazioni avvengono quando due o più molecole interagiscono e le molecole cambiano. I legami tra gli atomi vengono rotti e creati per formare nuove molecole. Questo è quanto. Che molecole sono? Come interagiscono? Cosa succede? Le possibilità sono infinite.
Quando cercate di capire le reazioni chimiche, immaginate di lavorare con gli atomi. Immagina che i mattoni siano proprio davanti a te sul tavolo. A volte usiamo i nostri giocattoli chimici per aiutarci a visualizzare il movimento degli atomi. Inseriamo e stacchiamo i piccoli connettori che rappresentano i legami chimici. Ci sono alcuni punti chiave che dovresti sapere sulle reazioni chimiche:
1. Deve avvenire un cambiamento chimico. Si inizia con una molecola e la si trasforma in un’altra. I legami chimici sono fatti o rotti per creare una nuova molecola. Un esempio di reazione chimica è l’arrugginimento di un bidone della spazzatura in acciaio. La ruggine avviene perché il ferro (Fe) nel metallo si combina con l’ossigeno (O2) nell’atmosfera. I legami chimici vengono creati e distrutti per creare infine l’ossido di ferro (Fe2O3).  Quando un frigorifero o un condizionatore raffredda l’aria, non c’è nessuna reazione nelle molecole dell’aria. Il cambiamento di temperatura è un cambiamento fisico. Quando si scioglie un cubetto di ghiaccio, è un cambiamento fisico. Quando metti la candeggina nella lavatrice per pulire i tuoi vestiti, un cambiamento chimico rompe le molecole delle tue macchie.
Quando un frigorifero o un condizionatore raffredda l’aria, non c’è nessuna reazione nelle molecole dell’aria. Il cambiamento di temperatura è un cambiamento fisico. Quando si scioglie un cubetto di ghiaccio, è un cambiamento fisico. Quando metti la candeggina nella lavatrice per pulire i tuoi vestiti, un cambiamento chimico rompe le molecole delle tue macchie.
2. Una reazione potrebbe includere atomi, ioni, composti o molecole di un singolo elemento. Devi ricordare che una reazione chimica può avvenire con qualsiasi cosa, basta che avvenga un cambiamento chimico. Se metti l’idrogeno puro (H2) e l’ossigeno puro in una stanza, potrebbero essere coinvolti in una reazione per formare acqua (H2O). Tuttavia, sarà in quantità molto molto piccole. Se si aggiungesse una scintilla, questi gas sarebbero coinvolti in una violenta reazione chimica che risulterebbe in un’enorme esplosione (esotermica). Un’altra reazione chimica potrebbe includere ioni d’argento (Ag+). Se si mescola una soluzione con ioni d’argento con una soluzione che ha ioni cloruro (Cl-), si formerà un precipitato di cloruro d’argento (AgCl) che cadrà fuori dalla soluzione.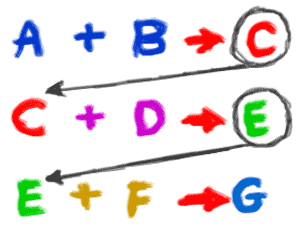 3. Le reazioni singole spesso avvengono come parte di una serie più grande di reazioni. Quando una pianta produce zuccheri, ci potrebbero essere fino a una dozzina di reazioni chimiche per passare attraverso il ciclo di Calvin e alla fine creare (sintetizzare) molecole di glucosio (C6H12O6). L’esempio della ruggine che abbiamo usato prima ti ha mostrato solo i reagenti originali e i prodotti finali della reazione chimica. C’erano diverse reazioni intermedie in cui i legami chimici venivano creati e distrutti. L’esempio del cloruro d’argento si è concentrato solo sugli ioni. In realtà, le due soluzioni sono state create quando due sali si sono dissociati (divisi in ioni) in acqua.
3. Le reazioni singole spesso avvengono come parte di una serie più grande di reazioni. Quando una pianta produce zuccheri, ci potrebbero essere fino a una dozzina di reazioni chimiche per passare attraverso il ciclo di Calvin e alla fine creare (sintetizzare) molecole di glucosio (C6H12O6). L’esempio della ruggine che abbiamo usato prima ti ha mostrato solo i reagenti originali e i prodotti finali della reazione chimica. C’erano diverse reazioni intermedie in cui i legami chimici venivano creati e distrutti. L’esempio del cloruro d’argento si è concentrato solo sugli ioni. In realtà, le due soluzioni sono state create quando due sali si sono dissociati (divisi in ioni) in acqua.
Wikipedia: Reazioni chimiche
Enciclopedia.com: Reazioni chimiche
Rhode Island College: Reactions