HormoonafgifteEdit
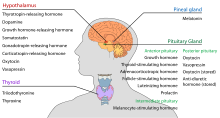
De hypothalamus heeft een centrale neuro-endocriene functie, met name door zijn controle van de voorste hypofyse, die op zijn beurt verschillende endocriene klieren en organen regelt. Afgiftehormonen (ook wel releasing factors genoemd) worden geproduceerd in hypothalamuskernen en vervolgens langs axonen getransporteerd naar de mediane eminentie of de achterste hypofyse, waar zij worden opgeslagen en naar behoefte afgegeven.
Hypofyse-voorste
In de hypothalamus-adenohypofyse-as komen releasing hormonen, ook bekend als hypofysiotrope of hypothalamushormonen, vrij uit de mediane eminentie, een verlengstuk van de hypothalamus, in het hypofyse portaalsysteem, dat ze naar de hypofyse-voorste transporteert, waar ze hun regulerende functies uitoefenen op de secretie van adenohypofyseale hormonen. Deze hypofysiotrope hormonen worden gestimuleerd door parvocellulaire neurosecretorische cellen die zich in de periventriculaire zone van de hypothalamus bevinden. Nadat zij in de haarvaten van de derde ventrikel zijn vrijgekomen, reizen de hypofysiotrope hormonen door wat de hypothalamo-hypofyse portale circulatie wordt genoemd. Zodra zij hun bestemming in de voorste hypofyse hebben bereikt, binden deze hormonen aan specifieke receptoren die zich op het oppervlak van hypofysecellen bevinden. Afhankelijk van welke cellen door deze binding worden geactiveerd, zal de hypofyse beginnen of stoppen met het afscheiden van hormonen in de rest van de bloedbaan.
| Gescheiden hormoon | Afkorting | Geproduceerd door | Effect | |
|---|---|---|---|---|
| Thyrotropin-releasing hormone (Prolactin-releasing hormone) |
TRH, TRF, of PRH | Parvocellulaire neurosecretorische cellen van de paraventriculaire kern | Stimuleren schildklier-stimulerend hormoon (TSH) afgifte uit voorste hypofyse (voornamelijk) Stimuleren prolactine afgifte uit voorste hypofyse |
|
| Corticotropine-releasing hormone | CRH of CRF | Parvocellulaire neurosecretorische cellen van de paraventriculaire kern | Stimuleren afgifte adrenocorticotroop hormoon (ACTH) uit voorste hypofyse | |
| Dopamine (Prolactine-remmend hormoon) |
DA of PIH | Dopamineneuronen van de arcuate kern | Remmt de afgifte van prolactine uit de voorste hypofyse | |
| Groei-hormoon-afgifte hormoon | GHRH | Neuro-endocriene neuronen van de Arcuate kern | Stimuleren groeihormoon (GH) uit de voorste hypofyse | |
| Gonadotropin-releasing hormone | GnRH of LHRH | Neuro-endocriene cellen van het Preopticum | Stimuleren van follikel-stimulerend hormoon (FSH) | .stimulerend hormoon (FSH) uit voorste hypofyse Stimuleren luteïniserend hormoon (LH) uit voorste hypofyse |
| Somatostatine (groeihormoon-remmend hormoon) |
SS, GHIH, of SRIF | Neuro-endocriene cellen van de periventriculaire kern | Remmt afgifte van groeihormoon (GH) door voorste hypofyse Remmt (matig) afgifte van schildklier-stimulerend hormoon (TSH) door voorste hypofyse |
Andere hormonen die worden afgescheiden door de mediane eminence zijn vasopressine, oxytocine, en neurotensine.
Hypofyse achteraan
In de hypothalamus-neurohypofyse-as komen neurohypofysaire hormonen vrij uit de hypofyse achteraan, die eigenlijk een verlengstuk van de hypothalamus is, en worden zij in de circulatie gebracht.
| Gescheiden hormoon | Afkorting | Geproduceerd door | Effect |
|---|---|---|---|
| Oxytocine | OXY of OXT | Magnocellulaire neurosecretorische cellen van de paraventriculaire kern en de supraopticus kern | Samentrekking van de baarmoeder Lactatie (afscheidsreflex) |
| Vasopressine (antidiuretisch hormoon) |
ADH of AVP | Magnocellulaire en parvocellulaire neurosecretorische cellen van de paraventriculaire kern, magnocellulaire cellen in de supraoptische kern | Verhoogde waterdoorlaatbaarheid van de cellen van de distale tubulus en de verzamelbuis in de nier, waardoor water kan worden gereabsorbeerd en geconcentreerde urine kan worden uitgescheiden |
Het is ook bekend dat hypothalamus-hypofyse-bijnieras (HPA)-hormonen verband houden met bepaalde huidziekten en de homeostase van de huid. Er zijn aanwijzingen dat er een verband bestaat tussen hyperactiviteit van HPA-hormonen en stressgerelateerde huidziekten en huidtumoren.
StimulatieEdit
De hypothalamus coördineert vele hormonale en gedragsmatige circadiane ritmen, complexe patronen van neuro-endocriene outputs, complexe homeostatische mechanismen, en belangrijke gedragingen. De hypothalamus moet daarom reageren op veel verschillende signalen, waarvan sommige van buitenaf en andere van binnenuit worden opgewekt. Delta-golfsignalen die hetzij in de thalamus, hetzij in de cortex ontstaan, beïnvloeden de secretie van hormonen; GHRH en prolactine worden gestimuleerd, terwijl TRH wordt geremd.
De hypothalamus is gevoelig voor:
- Licht: daglengte en fotoperiode voor het reguleren van circadiane en seizoensgebonden ritmen
- Olfactorische stimuli, waaronder feromonen
- Steroïden, waaronder gonadale steroïden en corticosteroïden
- Neurlijk doorgegeven informatie die met name afkomstig is van het hart, het enterische zenuwstelsel (van het maagdarmkanaal), en het voortplantingskanaal.
- Autonome inputs
- Bloedprikkels, waaronder leptine, ghreline, angiotensine, insuline, hypofysehormonen, cytokinen, plasmaconcentraties van glucose en osmolariteit enz.
- Stress
- Infectie van micro-organismen door verhoging van de lichaamstemperatuur, waardoor de lichaamsthermostaat naar boven wordt bijgesteld.
Olfactorische prikkelsEdit
Olfactorische prikkels zijn bij veel diersoorten belangrijk voor de geslachtelijke voortplanting en de neuro-endocriene functie. Als bijvoorbeeld een zwangere muis wordt blootgesteld aan de urine van een ‘vreemd’ mannetje tijdens een kritieke periode na de coïtus dan mislukt de zwangerschap (het Bruce-effect). Zo vormt een vrouwtjesmuis tijdens de coïtus een nauwkeurig “olfactorisch geheugen” van haar partner dat verscheidene dagen blijft bestaan. Feromonale signalen helpen bij veel diersoorten bij het synchroniseren van de bronst; bij vrouwen kan een gesynchroniseerde menstruatie ook het gevolg zijn van feromonale signalen, hoewel de rol van feromonen bij de mens wordt betwist.
Stimuli door het bloedEdit
Peptidehormonen hebben belangrijke invloeden op de hypothalamus, en om dat te doen moeten zij de bloed-hersenbarrière passeren. De hypothalamus wordt gedeeltelijk begrensd door gespecialiseerde hersengebieden die geen effectieve bloed-hersenbarrière hebben; het capillaire endotheel op deze plaatsen is gefenestreerd om vrije doorgang van zelfs grote proteïnen en andere moleculen mogelijk te maken. Sommige van deze plaatsen zijn de plaatsen van neurosecretie – de neurohypofyse en de mediane eminentie. Andere zijn echter plaatsen waar de hersenen de samenstelling van het bloed bemonsteren. Twee van deze plaatsen, het SFO (subfornicaal orgaan) en het OVLT (organum vasculosum van de lamina terminalis) zijn zogenaamde circumventriculaire organen, waar de neuronen in nauw contact staan met zowel het bloed als de liquor. Deze structuren zijn sterk gevasculariseerd en bevatten osmoreceptieve en natriumreceptieve neuronen die het drinken, de vasopressine-afgifte, de natriumuitscheiding en de natriumhonger regelen. Zij bevatten ook neuronen met receptoren voor angiotensine, atriale natriuretische factor, endotheline en relaxine, die elk belangrijk zijn voor de regulering van de vocht- en elektrolytenbalans. Neuronen in de OVLT en SFO projecteren naar de nucleus supraopticus en de nucleus paraventricularis, en ook naar preoptische hypothalamische gebieden. De circumventriculaire organen kunnen ook de plaats zijn waar interleukines werken om zowel koorts als ACTH-secretie uit te lokken, via effecten op paraventriculaire neuronen.
Het is niet duidelijk hoe alle peptiden die de hypothalamische activiteit beïnvloeden de nodige toegang krijgen. In het geval van prolactine en leptine zijn er aanwijzingen voor actieve opname bij de plexus choroideus vanuit het bloed in de cerebrospinale vloeistof (CSF). Sommige hypofysehormonen hebben een negatieve terugkoppelingswerking op de secretie door de hypothalamus; groeihormoon bijvoorbeeld werkt terug op de hypothalamus, maar hoe het in de hersenen terechtkomt is niet duidelijk. Er zijn ook aanwijzingen voor centrale acties van prolactine.
Er is gebleken dat schildklierhormoon (T4) wordt opgenomen door de hypothalamische gliacellen in de nucleus infundibularis/ mediane eminence, en dat het hier wordt omgezet in T3 door het type 2 deiodinase (D2). Vervolgens wordt T3 getransporteerd naar de thyrotropin-releasing hormone (TRH)-producerende neuronen in de paraventriculaire kern. In deze neuronen zijn schildklierhormoonreceptoren gevonden, wat erop wijst dat zij inderdaad gevoelig zijn voor T3-stimuli. Bovendien brachten deze neuronen MCT8, een schildklierhormoontransporter, tot expressie, wat de theorie ondersteunt dat T3 in deze neuronen wordt getransporteerd. T3 zou zich dan kunnen binden aan de schildklierhormoonreceptor in deze neuronen en de productie van thyrotropine-releasing hormoon beïnvloeden, waardoor de schildklierhormoonproductie wordt gereguleerd.
De hypothalamus functioneert als een soort thermostaat voor het lichaam. Hij stelt een gewenste lichaamstemperatuur in en stimuleert ofwel de warmteproductie en -retentie om de bloedtemperatuur op een hogere stand te brengen, ofwel zweten en vasodilatatie om het bloed tot een lagere temperatuur af te koelen. Alle koorts is het gevolg van een verhoogde instelling in de hypothalamus; een verhoogde lichaamstemperatuur door een andere oorzaak wordt geclassificeerd als hyperthermie. In zeldzame gevallen kan een directe beschadiging van de hypothalamus, bijvoorbeeld door een beroerte, koorts veroorzaken; dit wordt ook wel hypothalamuskoorts genoemd. Het komt echter vaker voor dat een dergelijke beschadiging een abnormaal lage lichaamstemperatuur veroorzaakt.
SteroïdenEdit
De hypothalamus bevat neuronen die sterk reageren op steroïden en glucocorticoïden – (de steroïdhormonen van de bijnier, die vrijkomen als reactie op ACTH). Het bevat ook gespecialiseerde glucose-gevoelige neuronen (in de arcuate kern en de ventromediale hypothalamus), die belangrijk zijn voor de eetlust. Het preoptische gebied bevat thermogevoelige neuronen; deze zijn belangrijk voor de TRH secretie.
NeuralEdit
Oxytocine secretie in reactie op zuigen of vagino-cervicale stimulatie wordt gemedieerd door sommige van deze paden; vasopressine secretie in reactie op cardiovasculaire stimuli afkomstig van chemoreceptoren in het carotislichaam en de aortaboog, en van lage-druk atriale volume-receptoren, wordt gemedieerd door anderen. Bij de rat veroorzaakt stimulatie van de vagina ook prolactine secretie, en dit resulteert in pseudo-zwangerschap na een onvruchtbare paring. Bij het konijn veroorzaakt coïtus een reflexmatige ovulatie. Bij het schaap kan stimulatie van de baarmoederhals in aanwezigheid van hoge oestrogeenniveaus moederlijk gedrag bij een maagdelijk ooi opwekken. Al deze effecten worden bemiddeld door de hypothalamus, en de informatie wordt hoofdzakelijk doorgegeven via spinale paden die zich in de hersenstam bevinden. Stimulatie van de tepels stimuleert de afgifte van oxytocine en prolactine en onderdrukt de afgifte van LH en FSH.
Cardiovasculaire stimuli worden overgebracht door de nervus vagus. De vagus geeft ook allerlei viscerale informatie door, waaronder bijvoorbeeld signalen van de maagspanning of -lediging, om de eetlust te onderdrukken of te bevorderen door het vrijkomen van respectievelijk leptine of gastrine aan te geven. Ook deze informatie bereikt de hypothalamus via relais in de hersenstam.
Daarnaast is de functie van de hypothalamus gevoelig voor – en gereguleerd door – het niveau van de drie klassieke monoamine neurotransmitters, noradrenaline, dopamine en serotonine (5-hydroxytryptamine), in de zenuwbanen van waaruit zij wordt geïnnerveerd. Zo hebben noradrenerge inputs afkomstig van de locus coeruleus belangrijke regulerende effecten op de corticotropin-releasing hormone (CRH) niveaus.
Controle van voedselinnameEdit
| Peptiden die het voedings gedrag |
Peptiden die voedingsgedrag |
|---|---|
| Ghreline | Leptine |
| Neuropeptide Y | (α,β,γ)-Melanocyte-stimulerende hormonen |
| Agouti-gerelateerd peptide | Cocaïne- en amfetaminegereguleerde transcriptpeptiden |
| Orexinen (A,B) | Corticotropin-releasing hormone |
| Melanine-concentrating hormone | Cholecystokinin |
| Galanine | Insulin |
| Glucagon-like peptide 1 |
Het uiterste laterale deel van de ventromediale kern van de hypothalamus is verantwoordelijk voor de controle van de voedselinname. Stimulatie van dit gebied veroorzaakt een verhoogde voedselinname. Bilaterale lesie van dit gebied veroorzaakt volledige stopzetting van de voedselinname. Mediale delen van de kern hebben een controlerend effect op het laterale deel. Bilaterale lesie van het mediale deel van de ventromediale nucleus veroorzaakt hyperfagie en zwaarlijvigheid bij het dier. Verdere laesie van het laterale deel van de ventromediale kern in hetzelfde dier veroorzaakt volledige stopzetting van de voedselopname.
Er zijn verschillende hypothesen met betrekking tot deze regulatie:
- Lipostatische hypothese: Deze hypothese stelt dat vetweefsel een humoraal signaal produceert dat evenredig is met de hoeveelheid vet en inwerkt op de hypothalamus om de voedselinname te verminderen en de energie-output te verhogen. Het is gebleken dat het hormoon leptine op de hypothalamus inwerkt om de voedselinname te verminderen en de energie-output te verhogen.
- Gutpeptide-hypothese: gastro-intestinale hormonen zoals Grp, glucagonen, CCK en andere zouden de voedselinname afremmen. Het voedsel dat het maagdarmkanaal binnenkomt, triggert het vrijkomen van deze hormonen, die inwerken op de hersenen om verzadiging te produceren. De hersenen bevatten zowel CCK-A als CCK-B receptoren.
- Glucostatische hypothese: De activiteit van het verzadigingscentrum in de ventromediale kernen wordt waarschijnlijk beheerst door de glucosebenutting in de neuronen. Er is verondersteld dat wanneer hun glucosegebruik laag is en bijgevolg wanneer het arterioveneuze bloedglucoseverschil over hen laag is, de activiteit over de neuronen afneemt. Onder deze omstandigheden is de activiteit van het voedingscentrum ongecontroleerd en voelt het individu zich hongerig. De voedselopname wordt snel verhoogd door intraventriculaire toediening van 2-deoxyglucose, waardoor het glucosegebruik in de cellen daalt.
- Thermostatische hypothese: Volgens deze hypothese stimuleert een daling van de lichaamstemperatuur onder een bepaald set-point de eetlust, terwijl een stijging boven het set-point de eetlust remt.
AngstverwerkingEdit
De mediale zone van de hypothalamus maakt deel uit van een circuit dat gemotiveerd gedrag controleert, zoals defensief gedrag. Analyses van Fos-labeling toonden aan dat een reeks kernen in de “gedragscontrolekolom” belangrijk is bij het reguleren van de expressie van aangeboren en geconditioneerd defensief gedrag.
Antipredatoir defensief gedrag
Blootstelling aan een roofdier (zoals een kat) lokt defensief gedrag uit bij laboratoriumknaagdieren, zelfs wanneer het dier nog nooit aan een kat is blootgesteld. In de hypothalamus veroorzaakt deze blootstelling een toename van Fos-gelabelde cellen in de voorste hypothalamische kern, het dorsomediale deel van de ventromediale kern, en in het ventrolaterale deel van de premammillaire kern (PMDvl). De premammillaire kern speelt een belangrijke rol in de expressie van defensief gedrag tegenover een roofdier, aangezien laesies in deze kern defensieve gedragingen, zoals bevriezen en vluchten, opheffen. De PMD moduleert geen defensief gedrag in andere situaties, aangezien laesies van deze nucleus minimale effecten hadden op post-shock freezing scores. De PMD heeft belangrijke verbindingen met het dorsale periaqueductale grijs, een belangrijke structuur in angst expressie. Bovendien vertonen de dieren risicobeoordelingsgedrag ten opzichte van de omgeving die eerder met de kat geassocieerd werd. Fos-gelabelde celanalyse toonde aan dat de PMDvl de meest geactiveerde structuur is in de hypothalamus, en inactivatie met muscimol voorafgaand aan blootstelling aan de context schaft het defensief gedrag af. De hypothalamus, voornamelijk de PMDvl, speelt dus een belangrijke rol in de expressie van aangeboren en geconditioneerd defensief gedrag tegen een roofdier.
Sociale nederlaag
Ook de hypothalamus speelt een rol in sociale nederlaag: Nuclei in mediale zone worden ook gemobiliseerd tijdens een ontmoeting met een agressieve soortgenoot. Het verslagen dier heeft een verhoging van Fos niveaus in sexueel dimorfe structuren, zoals de mediale pre-optische kern, het ventrolaterale deel van de ventromediale kern, en de ventrale premammilaire kern. Dergelijke structuren zijn belangrijk bij andere sociale gedragingen, zoals seksueel en agressief gedrag. Bovendien wordt ook de premammillaire nucleus gemobiliseerd, het dorsomediale deel maar niet het ventrolaterale deel. Lesies in deze kern heffen passief defensief gedrag op, zoals bevriezen en de “op-de-rug” houding.