Introdução
Patientes internados em unidades de terapia intensiva (UTI) freqüentemente requerem a administração IV de vários fármacos. Drogas vasoativas, analgésicos e sedativos estão entre os grupos terapêuticos mais utilizados e geralmente são administrados em infusão contínua.
De acordo com a revisão sistemática realizada por Moyen et al. há uma média de 1,7 erros/dia associados ao processo de administração de fármacos no ambiente da UTI.1 Por outro lado, os dados relatados por Merino et al. em um estudo realizado entre UTIs hospitalares espanholas são um pouco melhores (1,13 erros de medicação para cada 100 pacientes/dia).2 Mesmo assim, os erros de medicação são comuns nas UTIs e requerem cuidados dos profissionais de saúde para minimizá-los.
Os erros de medicação na administração de drogas nas UTIs são devidos a vários fatores: o uso de drogas de alto risco (drogas vasoativas, inotropos, sedativos, etc.) freqüentemente administradas em baixas doses devido à sua alta força medicamentosa, exigindo diluição e uma avaliação prévia à sua administração. Outro factor é a prescrição de doses em diferentes unidades de medida ou o elevado número de fármacos utilizados com cada paciente. Embora seja um avanço importante em relação à segurança, o uso de bombas inteligentes de infusão tem sido associado a um número importante ou erros de medicação devido a problemas de programação.3
A combinação destes fatores de risco aumenta as chances de cometer erros nos pacientes mais vulneráveis devido à sua gravidade. Pacientes gravemente enfermos têm frequentemente acessos venosos limitados. Isto significa que diferentes medicamentos são entregues usando a mesma via de administração, o que aumenta os riscos envolvidos ao misturar medicamentos incompatíveis. A mistura de drogas incompatíveis é um erro de medicação que pode ter consequências graves para o paciente, como falhas terapêuticas, microembolismo ou toxicidade.4
A infusão em Y de 2 drogas requer que ambas sejam fisicamente compatíveis.5 Esta coadministração ocorre quando se misturam drogas numa proporção de 1:1 e na ausência de sinais visíveis de incompatibilidade como precipitação ou mudança de cor. Por outro lado, para a coadministração segura de 2 drogas no mesmo diluente, a mistura precisa ser quimicamente estável. Isto significa que é necessária a confirmação prévia de que não ocorreu alteração significativa na concentração de nenhum dos medicamentos presentes na mistura.6
A padronização da concentração das soluções de infusão é uma das medidas mais úteis para evitar erros de medicação no ambiente da UTI, especialmente em medicamentos de alto risco devido ao seu potencial de causar danos graves e porque têm a maior incidência de erros de medicação.
Outra medida altamente recomendada para a administração segura de medicamentos é ter informações confiáveis disponíveis sobre compatibilidade de medicamentos quando se administra medicamentos comuns em pacientes críticos. Contudo, a informação sobre compatibilidade de medicamentos é escassa e, em muitas ocasiões, difícil de interpretar devido às diferentes concentrações utilizadas, à falta de informação sobre as técnicas de avaliação utilizadas ou à qualidade técnica suspeita das fontes. A falta de informações sobre a mistura segura de 2 drogas cria problemas no trabalho diário das equipes de enfermagem da UTI. Somado ao risco de complicações associadas à administração de 2 moléculas incompatíveis, esta falta de informação pode fazer com que a enfermeira tenha que procurar novos acessos venosos para administrar as drogas separadamente, o que aumenta o risco de complicações infecciosas ou tromboembólicas.
O objetivo desta revisão é reunir as informações publicadas sobre a compatibilidade física e química das drogas mais comumente utilizadas em uma UTI quando infundidas através da mesma linha através de um local em Y. Além disso, para avaliar a qualidade das informações publicadas e gerar um gráfico de compatibilidade com informações confiáveis e atualizadas para melhorar a segurança na administração de medicamentos a pacientes críticos.
MethodologySearch strategy
Foi realizada uma pesquisa sistemática nas bases de dados Medline, Stabilis, Handbook on Injectable Drugs e Micromedex para identificação de artigos originais, artigos de revisão e meta-análises sobre a compatibilidade física e química de medicamentos. Devido à sua abordagem clínica e falta de metodologia para determinar a estabilidade física e química, os estudos de caso foram descartados. As revisões publicadas por Kanji et al. e López-Cabezas et al.5,7 foram utilizadas como ponto de referência. A pesquisa concentrou-se em combinações de medicamentos sobre as quais esses autores não tinham informações ou não tinham procurado informações. Os anos de publicação dos estudos foram desde a década de 1990 até dezembro de 2017 e os idiomas incluídos foram inglês, espanhol e francês. A estratégia de pesquisa consistia em usar múltiplos termos descrevendo as informações de interesse para combiná-las com o operador booleano “OR” seguido de uma pesquisa refinada usando o operador “AND”. Os termos utilizados foram compatibilidade física, estabilidade da droga, y-site, y-injeção, droga intravenosa, mais os nomes e sinônimos das drogas de interesse.
As drogas usadas na revisão são rotineiramente utilizadas no ambiente da UTI são freqüentemente administradas por infusão contínua. As concentrações utilizadas como referência são as padronizadas em nosso centro7 para esses fármacos e são consistentes com as comumente utilizadas na maioria das UTIs (Tabela 1). Todas as informações sobre compatibilidade encontradas para uma determinada molécula sobre um intervalo de concentração diferente são mostradas na Tabela 2. O processo de busca de referência para cada droga foi realizado simultaneamente por 2 pesquisadores independentes.
Drogas de estudo e concentrações utilizadas como referência para a busca bibliográfica.
| Drug | Concentração padrão | Drug | Concentração padrão |
|---|---|---|---|
| Adrenalina | 40mcg/mL | Isoproterenol | 4mcg/mL |
| Amiodarona | 3.6mg/mL | Ketamina | 50mg/mL |
| Argatroban | 1mg/mL | Labetalol | 2mg/mL |
| Bicarbonato | 1mmol/L | Magnésio sulfato | 15mg/mL |
| Cloreto de cálcio | 10mg/mL | Meropenem | 30mg/mL |
| Gluconato de cálcio | 10mg/mL | Metadona | 0.2mg/mL |
| Ceftazidima | 24mg/mL | Midazolam | 4mg/mL |
| Cisatracurium | 2mg/mL | Milrinona | 0.2mg/mL |
| Clonidina | 7.5mcg/mL | N-acetilcisteína | 50mg/mL |
| Cloreto de morfina | 1mg/mL | Naloxona | 8mcg/mL |
| Dexmedetomidina | 4mcg/mL | Nitroglicerina | 0.2mg/mL |
| Diltiazem | 1mg/mL | Nitroprusside | 0,2mg/mL |
| Dobutamina | 8mg/mL | Noradrenalina | 0.32mg/mL |
| Dopamina | 8mg/mL | Pantoprazol | 0.32mg/mL |
| Esomeprazol | 0.32mg/mL | Piperacillin-tazobactam | 64mg/mL |
| Fenilefrina | 0.2mg/mL | Cloreto de potássio | 120mEq/L |
| Fentanil | 30mcg/mL | Propofol | 10mg/mL |
| Flumazenil | 40mcg/mL | Remifentanil | 20mcg/mL |
| Furosemida | 2mg/mL | Somatostatina | 24mcg/mL |
| Heparina de sódio | 50IU/mL | Vecurónio | 0.2mg/mL |
| Insulina | 1IU/mL | Verapamil | 0,1mg/mL |
Combinações de drogas física e quimicamente compatíveis com concentrações abaixo da marca de referência.
| Drug#1 | Concentração máxima compatível | Drug#2 | Concentração máxima compatível |
|---|---|---|---|
| Adrenalina | 32mcg/mL | Pantoprazol | 0.8mg/mL |
| 2mcg/mL | Verapamil | 0.08mg/mL | |
| Amiodarona | 4mg/mL | Fenilefrina | 0.04mg/mL |
| 6mg/mL | Furosemida | 1mg/mL | |
| 15mg/mL | Nitroprusside | 0.3mg/mL | |
| Cloreto de cálcio | 4mg/mL | Dobutamina | 4mg/mL |
| Gluconato de cálcio | 4mg/mL | Dobutamina | 4mg/mL |
| Ceftazidima | 120mg/mL | Dobutamina | 1mg/mL |
| 120mg/mL | Dopamina | Dopamina | 0.4mg/mL |
| 125mg/mL | Ketamina | 10mg/mL | |
| Dobutamina | 1mg/mL | Heparina | 50IU/mL |
| 4mg/mL | Sulfato de magnésio | 40mg/mL | |
| 4mg/mL | Cloreto de potássio | 60mEq/L | |
| Dopamina | 3.2mg/mL | Midazolam | 2mg/mL |
| Fentanil | 12.5mcg/mL | Remifentanil | 0,25mg/mL |
| Heparina | 20IU/mL | Verapamil | 0.08mg/mL |
| Isoproterenol | 4mcg/mL | Sulfato de magnésio | 1mg/mL |
| 200mcg/mL | Cloreto de potássio | 40mEq/L | |
| 4mcg/mL | Vecurónio | 0.1mg/mL | |
| 10mcg/mL | Verapamil | 0.08mg/mL | |
| Meropenem | 22mg/mL | Cloreto de potássio | 40mEq/L |
| Naloxona | 0.8mcg/mL | Verapamil | 0.08mg/mL |
| Nitroglicerina | 0.1mg/mL | Verapamil | 0.08mg/mL |
| Nitroprusside | 0.2mg/mL | Vecurónio | 0.1mg/mL |
| 0,1mg/mL | Verapamil | 0,08mg/mL | |
| Noradrenalina | 0,008mg/mL | Verapamil | >0.08mg/mL |
| Piperacilina…tazobactam | 40mg/mL | Dexmedetomidina | 4mcg/mL |
| 40mg/mL | Remifentanil | 250mcg/mL | |
| Potássio cloreto | 100mEq/L | Remifentanil | 250mcg/mL |
É consistente com as caixas cinzentas especificadas como I/C, como mostrado na Fig. 2.
Seleção do estudo
Após a pesquisa de referência, 2 revisores independentes avaliaram a qualidade dos estudos utilizando um processo de revisão por pares. Esta revisão foi realizada seguindo critérios de qualidade baseados na opinião de especialistas e seguindo diretrizes da prática clínica8-11:
-
Reprodutibilidade do estudo: descrição do princípio ativo e diluente, condições e metodologia do estudo.
-
Número de testes realizados (pelo menos em triplicata).
-
Tempo decorrido durante a coleta das amostras na análise de estabilidade: recomenda-se um período de 5 vezes o tempo da amostra incluindo um tempo de amostra de 0,
-
Estudos realizados para avaliar a estabilidade da mistura: (a) transparência: para partículas visíveis, observação com painel preto mate, contagem automática de partículas ou turbidimetria; para partículas subvisíveis, uso de microscopia óptica, espectrofotometria ou turbidimetria; (b) mudança de cor: inspeção visual ou espectrofotometria; (c) formação de gases: inspeção visual; (d) pH; e (e) estabilidade química: medida da variação da concentração dos 2 fármacos.
Criação do gráfico de resultados
Foi criado um gráfico com todas as combinações possíveis dos fármacos de interesse. As caixas foram nomeadas com um “C” se a mistura fosse compatível, com um “I” se fosse incompatível e com um “I/C” se a estabilidade dependesse de condições especiais. A combinação de drogas sem dados de compatibilidade foi deixada desmarcada.
ResultadosDesempenho da pesquisa de referência
Um total de 48 artigos foram identificados. A figura 1 mostra o processo de seleção. Dos 29 artigos incluídos na revisão, 4 foram escritos em espanhol, 3 em francês e 22 em inglês. Quanto às datas de publicação, 8 artigos foram publicados entre 1990 e 1999, 10 entre 2000 e 2009 e os 11 restantes foram publicados entre 2010 e 2017.
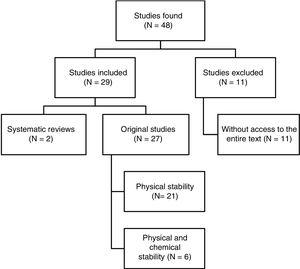
Resumo estruturado dos resultados da pesquisa de referência.
Qualidade dos estudos encontrados
Nenhum dos trabalhos estudados cumpriu todos os critérios de qualidade estabelecidos nesta revisão. Entretanto, 93% dos trabalhos descreveram as condições e metodologia do estudo com detalhes suficientes para garantir sua reprodutibilidade.
Testes foram realizados em triplicata apenas em 26% dos casos. Pelo contrário, 81% dos estudos seguiram a recomendação de colher amostras no tempo 0, embora apenas 10 tenham obtido uma amostra em 5 tempos diferentes.
No que diz respeito aos ensaios realizados para avaliar a estabilidade das amostras, todos os estudos avaliaram a transparência, enquanto 93% dos estudos relataram uma mudança na cor através de inspeção visual. Outros métodos foram utilizados em 16 estudos (59%) para ver partículas subvisíveis. 67% dos estudos avaliaram a formação de gases, e apenas 12 mediram mudanças de pH no tempo. Apenas 6 estudos avaliaram a estabilidade química das misturas sendo a cromatografia líquida de alta resolução o método utilizado em 5 estudos para medir a concentração dos ingredientes ativos da mistura.
Os resultados desta seção estão resumidos na Tabela 3.
Sumário dos critérios de qualidade dos trabalhos publicados.
| Indicador de qualidade | >Número de estudos (%) | |
|---|---|---|
| Avaliação da formação de precipitados | 27 (100) | 12,13,16-40 |
| Avaliação da mudança de cor | 25 (93) | 12,13,16-27,30-40 |
| Medição da alteração do pH | 12 (44) | 12,13,16,18,19,22,26,27,29,38,39 |
| Avaliação da formação de gases | 18 (67) | 12,13,17,19-21,24-26,31,33-40 |
| Análise realizada em triplicata | 7 (26) | 18,21,22,29,34,35,38 |
| Descrição da metodologia utilizada (inclui número e frequência de observações e condições de estudo) | 24 (89) | 12,13,17-24,26-33,35-40 |
| Descrição dos diluentes de todos os medicamentos em estudo | 21 (78) | 13,17-29,33,35-40 |
| Descrição do material dos receptores do estudo | 22 (81) | 12,13,17-31,33,36-39 |
| Estabilidade química | 6 (22) | 16,18,19,22,29,38 |
Resultados de compatibilidade física e química
Foram selecionadas 44 drogas usadas em perfusão contínua na UTI, incluindo uma solução para nutrição parenteral com e sem lipídios e 3 antibióticos beta-lactâmicos. A compatibilidade destes é mostrada na Fig. 2. Os dados obtidos pelas revisões realizadas por Kanji et al. e López-Cabezas et al. forneceram informações de compatibilidade em 393 das 945 combinações possíveis.5,7 Após completar a revisão sistemática, novos dados de estabilidade para 82 combinações de fármacos foram adicionados. As novas descobertas revelaram 29 combinações compatíveis, 27 combinações incompatíveis, e 26 combinações compatíveis em condições específicas. Portanto, a tabela final mostra os dados de compatibilidade de 475 das 945 combinações possíveis de 2 drogas (50,3%). Destes, 366 são compatíveis (77,1%), 80 são incompatíveis (16,8%) e 29 são compatíveis em condições específicas (6,1%) como mostra a Tabela 2.

Sumário de compatibilidades físicas e químicas. C, compatível; I, incompatível; I/C, compatível em condições especiais. As caixas pontilhadas mostram que a mistura é compatível apenas com soro glicosilado. Caixas com linhas diagonais mostram compatibilidade apenas com soro fisiológico.
Discussão
A certeza de que o uso de drogas é seguro é um dos principais compromissos assumidos pelos profissionais de saúde com seus pacientes. No ambiente da UTI e dada a enorme quantidade de drogas intravenosas administradas e o número limitado de vias de administração dos pacientes, esta segurança é às vezes comprometida devido aos riscos envolvidos ao co-administrar drogas incompatíveis em pacientes especialmente vulneráveis.
Bases de dados on-line como o Stabilis 4.0 são muito úteis para buscar informações sobre compatibilidade de medicamentos. No entanto, o pessoal que administra os medicamentos encontra tabelas muito mais úteis porque podem olhar rapidamente para as informações de que necessitam num determinado momento. Isto é especialmente interessante em situações urgentes quando qualquer atraso causado pelos profissionais de saúde pode ter conseqüências no paciente.
Esta revisão focou na análise da compatibilidade física e química dos fármacos intravenosos mais comumente usados através da infusão em “Y” na UTI e resumindo as informações obtidas em um gráfico de dupla entrada. Os estudos de compatibilidade física são os mais comuns porque são fáceis de realizar. Estudos de estabilidade química, entretanto, não são porque requerem técnicas analíticas mais sofisticadas para determinar a concentração inicial e final das drogas.
Embora isso, o número de combinações de drogas estudadas ainda é insuficiente. Como mostra a Fig. 2, não conseguimos encontrar nenhuma informação sobre a compatibilidade física e química de todas as combinações sugeridas; por exemplo, no caso do flumazenil e piperacilina-tazobactam só conseguimos determinar a estabilidade com 4 drogas e em ambos os casos as 39 combinações restantes permaneceram sem informação.
Even se levássemos em consideração todas as combinações possíveis sugeridas e acrescentássemos os novos dados encontrados, ainda teríamos zero informação sobre a compatibilidade física e química de 470 combinações. Isto significa que só temos dados disponíveis para 50,3% de todas as combinações possíveis sugeridas.
As combinações mais problemáticas em relação à incompatibilidade são drogas cuja estabilidade está intimamente ligada ao intervalo de pH; este é o caso do bicarbonato de sódio, furosemida ou pantoprazol. A furosemida, por exemplo, requer um pH básico para garantir a estabilidade da molécula em solução, razão pela qual a mistura com drogas ácidas (pH
4) causa turbidez e precipitação.12
A presença de adjuvantes na formulação farmacêutica, a concentração e a exposição a temperaturas extremas ou luminosidade são outros fatores associados à incompatibilidade de drogas.13 Há momentos em que uma determinada combinação de fármacos pode ser estável em um determinado diluente e incompatível em outro; por exemplo, a dopamina só é compatível com a amiodarona quando ambos são dissolvidos em soro glicosilado a 5%, porque este último é instável em soluções salinas a 0,9%. Assim, se esta mistura alegadamente compatível for realizada em soro fisiológico, pode ocorrer uma perda de concentração de amiodarona com o correspondente risco de falta de resposta terapêutica.
Por outro lado, em muitos casos, a qualidade dos estudos publicados até o momento pode ser melhor. Seria bom ter uma maior uniformidade nos padrões de qualidade deste tipo de estudos. Por exemplo, ainda que o pH seja um fator crítico na estabilidade dos medicamentos em solução, ele só foi verificado em 12 dos 27 trabalhos. Da mesma forma, a turbidimetria ou microscopia – técnicas mais precisas do que a observação visual para a detecção de partículas e mudanças de cor – são subutilizadas. Nos últimos anos, vários especialistas têm publicado diretrizes para o desenho de estudos de estabilidade de medicamentos.8-11 Só podemos esperar que isto melhore a qualidade geral deste tipo de estudos no futuro.
Os autores publicaram revisões destas características. Por exemplo, Flamein et al.14 estudaram este problema em UTIs neonatais; Knudsen et al.15 esclareceram a compatibilidade de analgésicos e sedativos. Nossa revisão é baseada no trabalho anterior realizado por Kanji et al.5 no Canadá e López-Cabezas.7 na Espanha. Ela foi completada com as novas informações disponíveis sobre drogas em nosso ambiente e dados sobre as concentrações de drogas mais utilizadas.
Overtudo, encontramos informações sobre 82 novas combinações de drogas de 27 referências diferentes, incluindo combinações de 3 antibióticos beta-lactâmicos (ceftazidima, meropenem e piperacilina-tazobactam) amplamente utilizadas no ambiente da UTI. Nos últimos anos as vantagens farmacocinéticas de uma via de perfusão prolongada da administração destes 3 antibióticos têm sido confirmadas.16-19
Perfusões em concentrações de fármacos que excedem as habituais são frequentemente utilizadas no paciente crítico. Neste sentido, não foi possível encontrar dados sobre todas as combinações de fármacos em relação às altas concentrações utilizadas na UTI (Tabela 1); entretanto, em alguns casos, obtivemos informações sobre concentrações menores do que as relatadas nesta revisão. Estes casos são mostrados na tabela de compatibilidade (Fig. 2) como compatibilidade condicionada (I/C), ou seja, que a combinação tinha sido estudada em uma concentração diferente da padrão.
Os dados de estabilidade relatados nesta revisão não podem ser generalizados para outras combinações ou concentrações de fármacos diferentes das descritas. Além disso, as informações fornecidas dizem respeito a 2 combinações de fármacos, podendo estar presentes incompatibilidades com>2 combinações de fármacos de cada vez, o que é altamente desaconselhável. Entretanto, os fármacos e concentrações selecionados são os mais utilizados nas UTIs adultas da maioria dos hospitais.
Até que tenhamos novos e melhores estudos de compatibilidade que esclareçam esta questão, esta revisão pode ser uma atualização de fácil leitura sobre as evidências disponíveis sobre a compatibilidade dos fármacos mais utilizados no ambiente da UTI. Seu objetivo é contribuir para a administração segura de medicamentos a pacientes que podem enfrentar as conseqüências de maior gravidade devido à sua fragilidade.
A contribuição dos autores
Genís Castells Lao: desenho e idéia do estudo, data mining, análise e interpretação dos dados; rascunho de documento ou revisão crítica do material intelectual; e aprovação final desta versão.
Montse Rodríguez Reyes: desenho e ideia do estudo, data mining, análise e interpretação dos dados; rascunho do artigo ou revisão crítica do material intelectual; e aprovação final desta versão.
Judit Roura Turet: data mining, análise e interpretação dos dados; rascunho do artigo ou revisão crítica do material intelectual; e aprovação final desta versão.
Marta Prat Dot: mineração de dados, análise e interpretação dos dados; rascunho de papel ou revisão crítica do material intelectual; e aprovação final desta versão.
Dolors Soy Muner: desenho e idéia do estudo; rascunho de papel ou revisão crítica do material intelectual; e aprovação final desta versão.
Carmen López Cabezas: desenho e idéia do estudo, mineração de dados, análise e interpretação dos dados; rascunho do artigo ou revisão crítica do material intelectual; e aprovação final desta versão.
Conflitos de interesse
Os autores não declararam nenhum conflito de interesse.