Na Exelead, abordamos a fabricação sob contrato com especialização focada em formulações lipossômicas e PEGylated para tratar doenças raras e populações pequenas ou mal atendidas. Somos especializados no desenvolvimento e fabricação de produtos à base de lipídios, medicamentos parenterais, e nossa equipe tem mais de 20 anos de experiência trabalhando com uma ampla gama de clientes pré-clínicos, clínicos e comerciais de fabricação sob contrato.
O que são lipossomas, e como eles são usados no fornecimento de medicamentos?
Lipossomas são veículos especializados de fornecimento que servem a múltiplos papéis no aprimoramento das capacidades dos ingredientes farmacêuticos ativos (APIs). Primeiro, eles podem proteger um medicamento da detecção pelo sistema imunológico do corpo, imitando as membranas biológicas e dando ao medicamento mais tempo para alcançar o destino pretendido. Segundo, eles servem para ajudar a solubilizar moléculas de drogas altamente lipofílicas ou modular a farmacocinética e a biodistribuição das IFAs – ajudando assim a minimizar os efeitos colaterais e melhorar o perfil de segurança do produto.
Lipossomos possuem uma estrutura vesicular única. Estas vesículas são compostas por uma camada lipídica que se forma em forma de esfera oca, englobando uma fase aquosa. Como tal, qualquer carga de interesse pode ser encapsulada dentro dos lipossomas tanto no compartimento aquoso (se for hidrossolúvel/hidrófilo) ou dentro da camada lipídica (se lipossolúvel/lipófilo).
alguns dos lípidos primários usados para fazer lipossomas são fosfolípidos e esfingolípidos. Estas duas categorias de lipídios são únicas em termos de um grupo de cabeça que adora água/hidrofílica e um grupo de cauda que odeia água/lipófilo. Devido à sua natureza anfifílica, estas moléculas auto-montagem espontânea para formar lipossomas e outras estruturas 3D únicas quando adicionadas a soluções aquosas. A forma ou morfologia das estruturas 3D depende de uma variedade de diferentes fatores – por exemplo, composição lipídica, temperatura, pH ou a presença de outros tampões, sais e açúcares na água.

Fonte de Imagem: Chem Libre Texts
Como uma droga interage com o corpo e se torna disponível para uso quando é formulada como um produto lipossômico?
Nos últimos anos, os lipossomas têm atraído atenção significativa como uma classe confiável de veículos de distribuição de drogas. Suas estruturas auto-fechadas podem encapsular múltiplas drogas de uma só vez, protegendo a carga fechada contra hidrólise e avarias. Além disso, o direcionamento de proteínas e ligandos funcionais de superfície no invólucro externo do bocal lipídico pode adicionar novas funcionalidades – possibilitando a entrada de lipossomos nas células, seja através de anticorpos ou de ligandos direcionados aos receptores. Estes ligandos fixam-se aos receptores celulares que são sobre-expressos em certas células doentes, permitindo a entrada do medicamento através da membrana celular.
“Os lipossomas protegem as moléculas carregadas do medicamento da degradação externa, e a sua semelhança com as membranas biológicas fornece oportunidades únicas para entregar moléculas do medicamento em células ou compartimentos subcelulares … Além disso, várias propriedades físico-químicas dos lipossomas – incluindo seu tamanho, carga e ligantes funcionais de superfície – podem ser alteradas, resultando em funcionalidades que favorecem tarefas específicas de administração de drogas. Estas vantagens fizeram dos lipossomas uma plataforma líder de administração de drogas com uma ampla gama de usos na clínica”
– Nanoestruturas semelhantes a lipossomas para administração de drogas | Gao W, Hu C-MJ, Fang RH, Zhang L 1
Tipicamente, os lipossomas são fabricados como injetáveis estéreis para administração à corrente sanguínea, e a liberação da droga ocorre quando os envelopes lipídicos se quebram – o que pode acontecer em ambientes extracelulares ou intracelulares.
Várias estratégias têm sido empregadas para projetar lipossomos convencionais com capacidades de liberação desencadeada, aumentando a eficácia terapêutica ao fazer com que os lipossomos liberem o API encapsulado ou “carga” com base em uma resposta de estímulo. Essa liberação é impulsionada pela quebra convencional dos lipossomas, ou é impulsionada por estímulos ativos e sugestões ambientais, incluindo energia térmica, gradiente de pH e estresse de cisalhamento.1
Formulações orientadas para liberação em ambientes intracelulares podem incluir lipídios sensíveis ao pH que alteram a estrutura lipossômica ou se degradam dentro de compartimentos ácidos, permitindo a liberação do medicamento encapsulado. Alternativamente, componentes termossensíveis ou fotossensíveis são às vezes incluídos para permitir a quebra e modulação da estrutura devido a mudanças na temperatura ou reação à luz de certos comprimentos de onda.
Os portadores de drogas do tipo lipossoma podem vir em muitas variedades diferentes, exibindo uma ampla gama de propriedades bioquímicas e biofísicas. Embora isso seja vantajoso e permita que essas partículas à base de lipídios assumam aplicações úteis em centenas de ambientes diferentes, o número de variações potenciais torna imperativo um rigoroso controle de fabricação.2
Exelead tem fabricado drogas à base de lipídios desde o início dos anos 90, começando com Abelcet. A anfotericina B, o princípio ativo do Abelcet, é mantido dentro de um complexo lipídico e seletivamente se funde com membranas fúngicas para alvejar células doentes.
Lipossomos vs. nanopartículas lipídicas
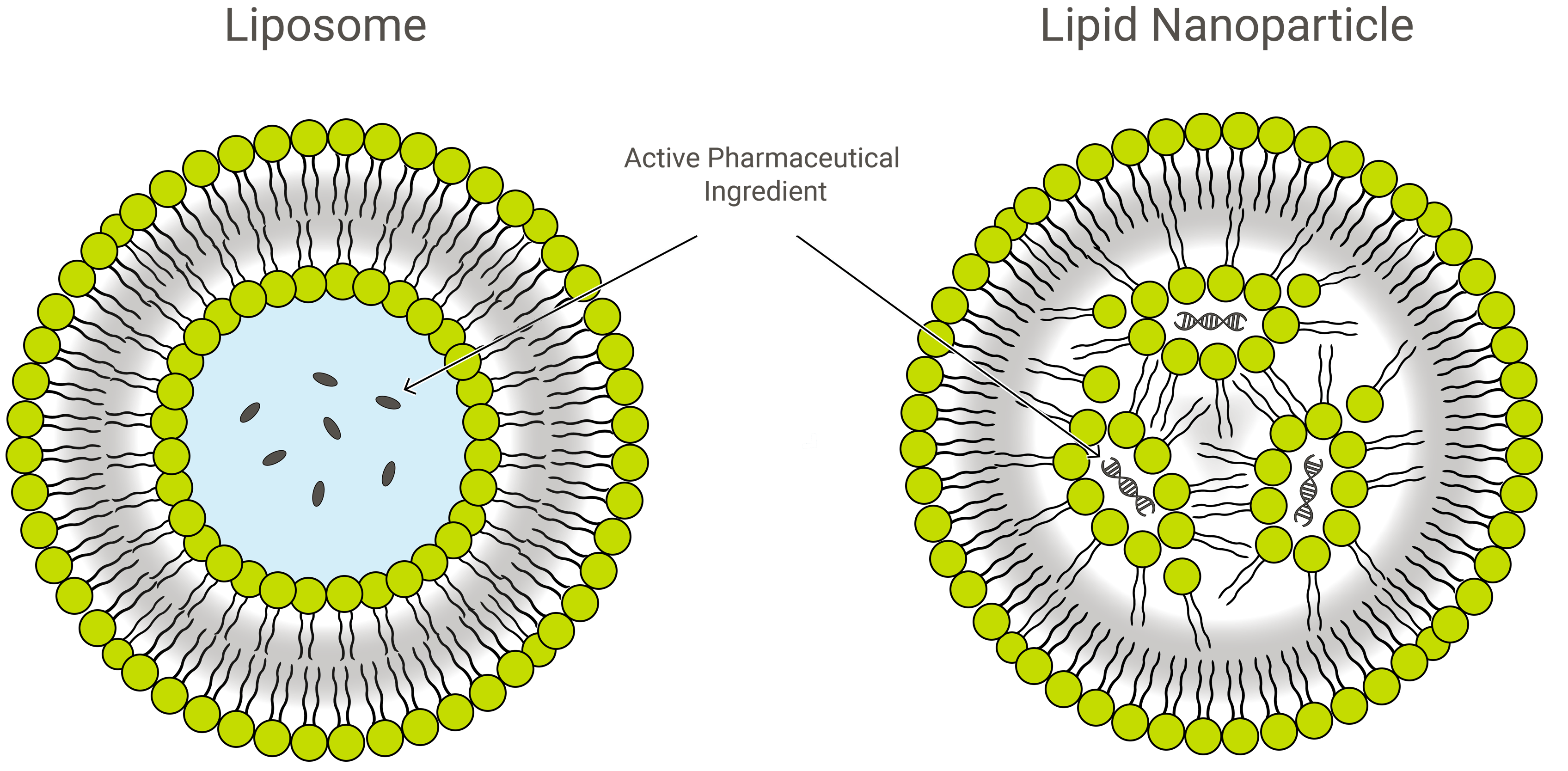
Lipossomos e nanopartículas lipídicas (LNPs) são similares por desenho, mas ligeiramente diferentes em composição e função. Ambos são nanoformulações lipídicas e excelentes veículos de distribuição de medicamentos, transportando cargas de interesse dentro de uma camada externa protetora de lipídios. Na aplicação, porém, os LNPs podem assumir uma variedade de formas.
LNPs são estruturas semelhantes a lipossomas especialmente orientadas para encapsular uma ampla variedade de ácidos nucleicos (RNA e DNA); e como tal, eles são o mais popular sistema de entrega de genes não-virais. Exelead desenvolve e fabrica LNPs para encapsular diferentes tipos de cargas úteis genéticas incluindo siRNA, mRNA e saRNA.
Lipossomos tradicionais incluem um ou mais anéis de camada lipídica ao redor de uma bolsa aquosa, mas nem todos os LNPs têm uma camada contígua que os qualificaria como vesículas lipídicas ou lipossomos. Alguns LNPs assumem uma estrutura semelhante a uma micela, encapsulando moléculas de drogas em um núcleo não aquoso.
PEGylation of LNPs and liposome-like drug delivery structures
LNPs são compostos principalmente de lipídios catiónicos (ver terapia genética abaixo) juntamente com outros ingredientes lipídicos. Estes incluem tipicamente moléculas neutras de fosfolípidos pertencentes à classe da fosfatidilcolina (PC) e esteróis, tais como o colesterol. Outro ingrediente lipídico comum é o chamado PEGylated phospholipid – um polímero de polietilenoglicol (PEG) ligado covalentemente ao grupo de cabeça de um fosfolipídeo.

PEGylated phospholipids são usados em muitos portadores de drogas à base de lipídios, principalmente porque oferecem o que é conhecido como um efeito furtivo ao produto da droga, uma vez que ele circula dentro do corpo. O sistema imunológico humano é orientado para proteger o corpo de qualquer objecto estranho, e as nanopartículas medicinais não são excepção. Para ajudar na eficiência da entrega e para permitir mais tempo de circulação para que as moléculas de carga alcancem os locais de doenças previstos, o PEG é adicionado para proteger essas nanopartículas, evitando que as proteínas do plasma sanguíneo sejam absorvidas pela superfície do lipossoma, aumentando a vida útil da circulação sanguínea.1
O segundo benefício do PEGylation é um aumento da estabilidade das nanoestruturas semelhantes às lipoestruturas. Os lipossomas convencionais, particularmente aqueles de tamanho inferior a 200 nm, podem ser instáveis por si só e tendem a fundir-se uns com os outros para reduzir a tensão superficial. Isto pode resultar na perda da droga encapsulada ou na mistura desfavorável de diferentes vesículas de carga. Uma forma dos fabricantes de medicamentos terem aprendido a superar este problema é cobrindo o exterior dos lipossomas com polímeros como PEG.
Estas nanopartículas furtivas resultaram em uma nova geração de formulações lipossômicas e múltiplos produtos clinicamente aprovados. Lipossomas PEGylated e LNPs são atualmente o novo paradigma para a maioria das terapias do câncer.
LNPs na terapia gênica
Por muito tempo, a maneira mais eficaz de entregar a terapêutica baseada em genes às células humanas foi usar um vírus que tinha sido modificado para transportar carga medicinal em vez de genes auto-replicáveis e prejudiciais. Este método ainda hoje é usado ocasionalmente, e é referido como entrega de genes virais. O fornecimento de genes não virais, no entanto, tornou-se popular nos últimos 20 anos devido a perfis de segurança melhorados, taxas mais baixas de reacções imunogénicas adversas e facilidade de fabrico. Um dos principais motores deste movimento tem sido o desenvolvimento de portadores de lipídios e polímeros, dos quais os LNPs são os mais populares.
LNPs usados para fornecer genes são primariamente sintetizados usando-se lípidos catiônicos, ou positivamente carregados, que se associam com ácidos nucleicos aniônicos, ou negativamente carregados. Outros componentes baseados em lipídios também podem ser adicionados para modular a eficiência da entrega e a liberação da localização da carga genética. Os LNPs também fornecem estabilidade mecânica, morfologia controlada e distribuição de tamanho estreito.1
Materiais inorgânicos, materiais orgânicos e hidrogéis foram explorados como núcleos para nanopartículas lipossômicas, encapsulados dentro de números variáveis de camadas lipídicas que formam a casca. Uma das variações mais bem sucedidas destas nanopartículas híbridas incorpora polímeros PLA ou PGLA dentro de uma monocamada lipídica. Esses dois biopolímeros centrais são particularmente úteis no fornecimento de drogas, pois facilitam a liberação controlada de drogas.1

A formulação de nanopartículas mostrada acima é um híbrido lipídico-polímero com um núcleo PGLA hidrofóbico e uma casca de lipídio-PEG hidrofílico.
Um campo em expansão
“Os lipossomas percorreram um longo caminho para se tornarem uma classe de portadores de drogas validadas … Uma variedade crescente de nanoestruturas semelhantes a lipossomas estão em desenvolvimento, cada uma com forças únicas adequadas para tarefas específicas de administração de drogas. Entretanto, a compreensão das interacções entre estas nanoestruturas e os sistemas biológicos está a progredir rapidamente. Uma quantidade substancial de informação sobre o seu tempo de circulação, acumulação de tecidos e toxicidade potencial foi obtida. É certo que os nanocarriers semelhantes a lipossomas desempenharão um papel maior para a administração de drogas num futuro próximo”
– Nanoestruturas semelhantes a lipossomas para a administração de drogas | Gao W, Hu C-MJ, Fang RH, Zhang L 1
– Enquanto há um trabalho significativo em curso no desenvolvimento de agentes medicinais de libertação controlada, nanocompartimentados, lipossomas e LNPs são opções especialmente promissoras. Estas estruturas proporcionam uma morfologia única, naturalmente estável, semelhante à das células para as nanomedicinas, e estão prontas para progredir no sentido de estratégias terapêuticas mais avançadas. A Exelead está assumindo tais desafios, incluindo o desenvolvimento de nanogéis que incorporam um conjunto de biólogos e pequenas moléculas.
Desde que os lipossomas foram propostos pela primeira vez como um sistema de administração de medicamentos no final dos anos 60, surgiram variações na estrutura e na funcionalidade, proporcionando valiosos avanços em termos de focalização da doença. Os medicamentos LNP surgiram em toda a indústria farmacêutica como terapias concebidas para fornecer agentes anti-cancerígenos, antibióticos, medicamentos genéticos, anestésicos e anti-inflamatórios.3
“Em aplicações clínicas, os medicamentos lipossómicos têm provado ser mais úteis pela sua capacidade de acumular “passivamente” em locais de maior permeabilidade à vasculatura, quando o seu diâmetro médio está na gama ultrafiltrável (<200 nm de diâmetro), e pela sua capacidade de reduzir os efeitos secundários dos medicamentos encapsulados em relação aos medicamentos livres. Isto resultou num aumento global do índice terapêutico, que mede a eficácia sobre a toxicidade.”
– Sistemas de administração de medicamentos lipossômicos: do conceito às aplicações clínicas | Allen TM, Cullis PR 3
Aplicações em medicamentos personalizados – uma nova era em estratégias terapêuticas
Em contraste com as abordagens tradicionais, de grandes carma para o tratamento de doenças, a medicina personalizada leva em conta diferenças individuais no estilo de vida, ambiente e biologia – incluindo a genética do paciente.
Isso é extremamente aplicável para doenças como o câncer. Mesmo dentro de um único tipo de câncer, os tipos de tumor diferem de um paciente para outro, e compreender a mutação genética particular que um paciente desenvolveu permite aos médicos empregar tratamentos mais específicos e precisos.4
Com o advento de terapias genéticas personalizadas, médicos e cientistas podem efetivamente adaptar um ingrediente farmacêutico ativo – geralmente RNA ou DNA – para combinar com o perfil específico da doença de um paciente em particular ou de um pequeno grupo de pacientes. Esta abordagem para a hiper-específica focalização da doença aumenta a eficácia e diminui os efeitos secundários indesejados para grupos de pacientes semelhantes.
LNPs como veículos de distribuição de oligonucleótidos
Porque grande parte do campo crescente da medicina personalizada está focada em terapias genéticas, os LNPs tornaram-se particularmente úteis como plataforma de distribuição de medicamentos. Qualquer oligonucleotídeo poderia teoricamente ser encapsulado dentro de um lipossoma ou LNP, mas o siRNA é atualmente a carga mais comum nestes tipos de medicamentos.
Em teoria, segmentos de siRNA podem ser projetados para silenciar qualquer gene, o que é um conceito excitante tanto para médicos quanto para pesquisadores. Infelizmente, o fornecimento de RNA livre e não encapsulado em células humanas é difícil, pois elas são grandes, instáveis no soro e propensas à degradação nuclease.5
Embora os pesquisadores tenham feito tentativas de estabilizar o siRNA no soro através da adição de ligações fosforotioato, doses altas são necessárias para silenciar efetivamente os genes em humanos. Os LNPs forneceram uma solução para este problema, fornecendo meios flexíveis e fáceis de encapsulamento, protegendo os segmentos de siRNA até atingirem o destino pretendido e facilitando a sua entrega às células alvo.5
“LNPs contendo lipídios catiônicos ionizáveis têm uma série de características necessárias para a entrega sistêmica de ácidos polinucleicos, incluindo pequenos tamanhos, estabilidade sérica, baixo potencial zeta superficial em pH fisiológico e carga catiônica em valores de pH ácido (por exemplo, em endossomos). Além disso, aproveitando os processos ‘endógenos’ de direcionamento devido à associação com ApoE após a administração, é possível obter uma absorção altamente eficiente em hepatócitos após a administração i.v., levando a uma excelente capacidade de silenciamento genético.”
– Sistemas de entrega de nanopartículas lipídicas para terapêutica baseada em siRNA | Wan C, Allen TM, Cullis PR 5
Tamanhos de lotes menores
Os medicamentos personalizados são frequentemente fabricados em tamanhos de lotes pequenos para pacientes individuais ou populações pequenas e podem frequentemente resultar em menos de um litro de produto. Em contraste, os lotes de fabricação tradicional para os medicamentos tradicionais geralmente produzem milhares de litros de produto farmacêutico em escala. A medicina personalizada requer uma abordagem única, e cada lote deve ser fabricado sob condições rigorosas de cGMP.
Como a medicina personalizada tornou-se um foco proeminente no desenvolvimento de medicamentos, muitas empresas da indústria farmacêutica adaptaram seus dutos para acomodar lotes menores programados para pequenos grupos de pacientes, além da produção tradicional de medicamentos em larga escala.
Na Exelead, esforços extensivos foram feitos para acomodar essas terapêuticas de pequenos lotes, que muitas vezes requerem IFAs caras e tempo de resposta rápido. Os medicamentos específicos para pacientes ou antígenos não deixam muito tempo desde o momento em que o oligonucleotídeo é sequenciado até o momento em que o produto precisa ser formulado em nosso site. Estas previsões a curto prazo, às vezes apenas seis semanas, apresentam desafios que temos sido capazes de superar refinando nossos sistemas existentes e incorporando técnicas inovadoras de formulação.
Aplicações generalizadas
Embora a medicina personalizada tenha o potencial de tratar quase qualquer doença, a pesquisa atual tem se concentrado principalmente em 1) imunoterapias, 2) terapias convencionais aumentadas via farmacogenômica e 3) tratamentos de câncer relacionados a biomarcadores. Lipossomas e LNPs têm aplicação como veículos de entrega para cada uma destas categorias de medicamentos, tornando-os um activo indispensável neste novo campo do desenvolvimento farmacêutico.
>

>
Artigos de referência
>
- Gao W, Hu C-MJ, Fang RH, Zhang L. Nanoestruturas tipo lipossoma para a entrega de medicamentos. Journal of materials chemistry B, Materiais para biologia e medicina. 2013;1(48):10.1039/C3TB21238F. doi:10.1039/C3TB21238F.
- Kraft JC, Freeling JP, Wang Z, Ho RJY. Tendências Emergentes de Pesquisa e Desenvolvimento Clínico dos Sistemas de Administração de Drogas Lipossoma e Nanopartículas Lipídicas. Journal of pharmaceutical sciences. 2014;103(1):29-52. doi:10.1002/jps.23773.
- Theresa M. Allen, Pieter R. Cullis. Sistemas de administração de drogas lipossomal: Do conceito às aplicações clínicas. Análises avançadas de administração de fármacos. 2013 Jan;65(1):36-48
- Esposito L. O que Realmente Significa Medicina Personalizada? Notícias dos EUA: Cuidados de Saúde. 2018 Jan;
- Wan C, Allen TM, Cullis PR. Sistemas de fornecimento de nanopartículas lipídicas para a terapêutica baseada em siRNA. Drug Deliv Transl Res. 2014 Fev;4(1):74-83. doi: 10.1007/s13346-013-0161-z.
- Vogenberg FR, Isaacson Barash C, Pursel M. Personalized Medicine: Parte 1: Evolução e Desenvolvimento em Teranóstico. Farmácia e Terapêutica. 2010;35(10):560-576.