Introdução
As micoses profundas são infecções incomuns causadas por fungos; elas são divididas em micoses subcutâneas e sistêmicas.1 Enquanto as manifestações cutâneas sempre ocorrem em micoses subcutâneas, ou micoses de implantação, como também são conhecidas, elas só ocasionalmente são vistas em micoses sistêmicas. Nesses casos, a pele é afetada diretamente, pela penetração do fungo na derme, ou indiretamente, por uma infecção que se alastrou a partir de um foco mais profundo. Segundo Rezusta et al.,2 a maioria das micoses subcutâneas e sistémicas em Espanha são importadas, com apenas algumas excepções (por exemplo, a mucormicose). Faltam dados epidemiológicos sobre a prevalência e incidência das micoses em Espanha.
Micoses subcutâneas
As micoses subcutâneas compreendem várias entidades clínicas causadas pela invasão da pele e tecido subcutâneo por fungos saprófitos que vivem no solo e na vegetação. Entretanto, embora cortes e feridas sejam muito comuns em pessoas que vivem em áreas rurais, em geral, há muito poucos casos de micoses subcutâneas.1
A rota típica de entrada do fungo é a inoculação traumática através de material contaminado, como lascas, espinhos ou outros objetos cortantes, explicando porque as micoses subcutâneas também são chamadas de micoses de implantação.3
Embora os fungos responsáveis pelas micoses subcutâneas sejam taxonomicamente heterogêneos, eles são unificados pelo fato de compartilharem a mesma via de entrada. Qualquer uma destas infecções pode afetar pessoas que viajaram para áreas endêmicas, mesmo anos após seu retorno.
As micoses subcutâneas mais comuns são esporotricose, cromoblastomicose e micetoma.1 Outras entidades menos comuns são a lacasiose, a feofomicose, a hialofomicose e a conidiobolomicose.
Sporotricose
A esporotricose é uma infecção subaguda ou crônica causada por fungos dimórficos, sendo a mais comum a Sporothrix schenckii.4,5 Estes fungos são universais, embora sejam mais comuns em áreas tropicais e subtropicais. A incidência estimada de esporotricose na América do Sul situa-se entre 48 e 60 casos por 100.000 habitantes por ano.6,7 Apenas alguns casos autóctones foram notificados na Espanha e em outras partes da Europa,8 e a maioria dos casos nestas áreas são importados.9
Após um período de incubação de 15 a 30 dias, a inoculação traumática por Sporothrix spp. resulta em uma infecção crônica caracterizada por lesões nodulares no tecido cutâneo e subcutâneo associadas a linfangite na área afetada.
Sporothrix spp. vivem em vegetação, plantas ou detritos vegetais no solo, e portanto as infecções são mais comuns em trabalhadores agrícolas e pessoas que trabalham em áreas abertas. A esporotricose é considerada uma doença ocupacional em guardas florestais, horticultores, jardineiros e trabalhadores agrícolas em geral.4,13 O alcoolismo e a diabetes também têm sido descritos como fatores de risco. A imunossupressão, independentemente da causa, também é um fator predisponente para doença disseminada ou sistêmica.1 A doença também pode ser adquirida através da manipulação do fungo em um ambiente de laboratório. Finalmente, houve uma epidemia interessante no sul do Brasil na qual a esporotricose foi transmitida para humanos através de arranhões de gatos, sugerindo que pode ser uma infecção zoonótica.14 A maioria das espécies isoladas nestes casos foram S brasiliensis.
Formulários Clínicos5
- 1)
Sporotricose linfocutânea. Também conhecida como esporotricose linfangitica, esta forma clínica representa mais de 75% de todos os casos de esporotricose.15 As lesões ocorrem em áreas expostas, como as mãos, face e pés. A doença começa como um nódulo roxo ou negro indolor que erode em uma pequena úlcera (châncreas esporotricóticas) com bordas inchadas, um centro granulomatoso doloroso e uma descarga mínima. Isto é seguido por linfangite com nódulos secundários ao longo da linha de drenagem linfática que pode progredir para úlceras; este padrão característico é conhecido como disseminação esporotricóidea (Fig. 1).6 A saúde geral do paciente não é afetada.15 O curso da doença varia de acordo com a resposta imunológica do hospedeiro, a virulência da estirpe, o tamanho do inóculo e a profundidade da lesão.
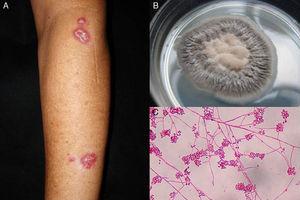 Figure 1.
Figure 1.A, esporotricose linfangitica. B, cultura Sporothrix schenckii. C, Exame microscópico de cultura em meio de ágar Sabouraud dextrose (eritrosina 2%, ampliação original ×40).
>
(0.21MB).>>
- 2)
Sporotricose fixa. Esta variante é caracterizada pela presença de uma lesão solitária. A infecção é limitada e geralmente se apresenta como uma placa verrucosa de crescimento lento e menos progressivo. A esporotricose fixa normalmente não afeta os vasos linfáticos e é mais comum em áreas endêmicas.16
- 3)
Outras formas clínicas:
Osteoarticular sporotricose. Esta é uma forma disseminada de esporotricose que afeta os ossos e articulações; é a forma mais comum de envolvimento sistêmico.17
Sporotricose pulmonar primária. Esta variante afeta preferencialmente os pacientes imunossuprimidos e é adquirida por inalação. Ela imita a tuberculose cavitária.16
Sporotricose pulmonar metastática. A forma metastática da esporotricose pulmonar é incomum e só tem sido descrita em casos isolados. Ocorre em pacientes imunocomprometidos, particularmente aqueles com infecção pelo vírus da imunodeficiência humana (HIV) na fase de AIDS.18
Invasão generalizada. A doença disseminada é rara na esporotricose, embora o envolvimento meníngeo e ocular tenha sido descrito em pacientes imunossuprimidos com diabetes descontrolada ou alcoolismo crônico.
No México, como em outros países da América Latina (lar da maior série de casos e da maior experiência com esporotricose), a esporotricose linfocutânea representa 60% a 80% de todos os casos de esporotricose, a esporotricose cutânea fixa 10% a 30%, e outras formas clínicas 1% a 2%.16
Sporotricose deve ser distinguida da tuberculose, leishmania, tularemia, nocardiose cutânea, infecções micobacterianas não tuberculosas, micetoma, cromoblastomicose, e lepra lepromatosa. A disseminação esporotricóide (linfangítica) pode ser vista em muitas dessas condições, que devem ser contempladas no diagnóstico diferencial.19
Diagnóstico
-
Pus (aspirado de nódulos). O exame microscópico direto não tem valor na esporotricose, pois as lesões contêm muito poucas formas de levedura. Sabouraud dextrose ágar (SDA) e SDA com antibióticos (cloranfenicol e ciclo-heximida) podem ser usados para cultura, o que produz colônias de leveduras que são inicialmente brancas e depois escurecidas (Fig. 1). O crescimento é caracteristicamente rápido (3-5 dias)20 mas são necessárias 2 semanas para identificar o fungo e confirmar o diagnóstico.16 A identificação molecular por reação em cadeia da polimerase (PCR) também é possível.10,21
-
Histologia. O exame histológico revela uma reação granulomatosa mista não específica com microabcessos neutrofílicos. O fungo apresenta-se como uma pequena forma de levedura em forma de charuto, por vezes rodeada por material eosinofílico radiante característico, conhecido como corpo de asteróide. Embora os corpos de asteróides possam ajudar no diagnóstico, não são patogênicos,16,20 pois também são encontrados intracelularmente em sarcoidose, silicose e lacasiose (lobomicose). Os corpos extracelulares de asteróides, entretanto, são mais característicos da esporotricose. Vários espécimes podem ser necessários para visualizar os microorganismos, embora sejam mais fáceis de encontrar no caso de doença disseminada ou visceral.
Tratamento
Sporotricose pode se resolver espontaneamente em alguns casos, como durante a gravidez, embora paradoxalmente a disseminação também tenha sido relatada em mulheres grávidas.
-
Solução saturada de iodeto de potássio. O tratamento com iodeto de potássio, como solução saturada, é iniciado com 5 gotas por refeição. Esta dose inicial é então gradualmente aumentada para 20 ou 30 gotas por refeição, de acordo com os níveis de tolerância. O tratamento deve ser mantido por 3 a 4 semanas após a resolução das manifestações clínicas. O mecanismo de acção é desconhecido, embora se pense que o iodeto de potássio actua como um imunoestimulante. Os efeitos adversos incluem um sabor metálico na boca, rinite, expectoração, urticária, petéquias, erupção bolhosa ou acneiforme, vasculite e indução de hipotireoidismo ou hipertireoidismo. O iodeto de potássio é contraindicado durante a gravidez.20,22
-
Itraconazol 200mg/d durante 3 a 6 meses.22 Este é o tratamento de primeira linha recomendado na maioria das diretrizes de tratamento. Ele tende a ser um pouco mais caro do que o iodeto de potássio, mas tem menos efeitos adversos.
-
Outras opções. Terbinafina 250-1000mg/d durante 3 a 6 meses23,24; fluconazol 400mg/d durante 3 a 6 meses22; anfotericina B (deoxicolato) 0.5-1mg/kg/d para doença sistêmica ou lipossomal ou formulações lipídicas de anfotericina B na dose de 3-5mg/kg/d22; calor local ou termoterapia por 2 ou 3 meses,22 ou uma combinação dos tratamentos acima (iodeto de potássio com itraconazol, itraconazol com terbinafina e terbinafina com iodeto de potássio).A adição de terapia fotodinâmica com metil aminolevulinato ou ainda melhor azul de metileno intralesional 1% (combinado ou não com itraconazol) tem produzido bons resultados in vitro e em 1 paciente.26
A cirurgia pode ter um papel importante na esporotricose osteoarticular.22 O desbridamento e a artrodese eram tradicionalmente considerados os tratamentos de escolha, mas a substituição protética da articulação seguida de tratamento antifúngico a longo prazo também tem sido descrita como uma opção viável
1,1Cromoblastomicose (cromomicose)
Cromoblastomicose, também conhecida como cromomicose, é uma infecção fúngica polimórfica crônica da pele e tecido subcutâneo. É causada por várias espécies de fungos melanizados ou demaáceos, que produzem um pigmento escuro. As formas parasitárias destes fungos são chamadas células fumagóides ou muriformes (corpos escleróticos).27-30
As espécies mais comuns que causam cromoblastomicose são Fonsecaea pedrosoi, Fonsecaea monophora, Cladophialophora carrionii, Phialophora verrucosa, e Rhinocladiella aquaspersa.5,27,28 A maioria dos pacientes tem um histórico de lesão traumática envolvendo madeira ou vegetação, e mais de 80% são trabalhadores rurais na África, Ásia e América do Sul que tendem a andar descalços. Os fungos responsáveis pela cromoblastomicose têm sido encontrados em todo o mundo, embora sejam mais comuns em países tropicais e subtropicais.27
Formas clínicas
O fungo geralmente penetra na pele através de uma lesão cutânea, tipicamente localizada nos membros inferiores.31 Cerca de 1 ou 2 meses depois, o indivíduo infectado desenvolve uma pápula que progride para um nódulo com verrugas de crescimento lento (Fig. 2). A infecção é limitada ao tecido subcutâneo e não se espalha para músculo ou osso, exceto em pacientes imunocomprometidos. As lesões individuais podem desenvolver um aspecto semelhante a uma couve-flor espessa e é comum a superinfecção bacteriana. Linfedema secundário, possivelmente progredindo para elefantíase, e carcinoma espinocelular pode ocorrer.27
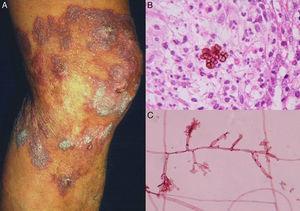 Figure 2.
Figure 2.A, Cromoblastomicose Nodular-verrucosa. B, Biópsia mostrando células fumagóides. C, Exame direto da cultura de Fonsecaea pedrosoi (biópsia; hematoxilina-eosina e eritrosina 2%, ampliação original em ambos os casos ×40).
(0,27MB).>Diagnóstico
-
Exame direto. O exame direto de crostas e fragmentos de pele pode revelar formas parasitárias que ocorrem isoladamente ou formar septos característicos (Fig. 2). As estruturas microscópicas observadas são comuns a todas as espécies.27,28
-
Cultura. Os fungos que causam a cromoblastomicose crescem lentamente quando cultivados em SDA com ou sem antibióticos (cloranfenicol e ciclo-heximida); produzem colônias oliváceas escuras ou negras com superfície plana aveludada e centro elevado. A distinção entre espécies é difícil e se baseia em estruturas reprodutivas e identificação molecular.30 Técnicas de biologia molecular (PCR), em particular visando regiões de DNA ribossômico (rDNA) transcrito internamente (ITS), também são úteis.32,33
-
Histologia. O exame histológico mostra uma hiperplasia pseudoepiteliomatosa característica na epiderme e um infiltrado inflamatório granulomatoso misto com células gigantes contendo estruturas fúngicas redondas características (Fig. 2) na derme.27
Tratamento
Cromoblastomicose é extremamente difícil de tratar e freqüentemente refratária a diversas opções, incluindo tratamentos não-farmacológicos como curetagem, eletrocoagulação e criocirurgia.5 Antifúngicos devem ser mantidos por pelo menos 6 meses e, embora possam produzir um resultado clínico favorável, recidivas durante ou após a terapia são comuns. O tratamento deve ser terminado quando todas as lesões desaparecerem.27
Outros tratamentos incluem ressecção cirúrgica de pequenas lesões; criocirurgia local (em associação com um antifúngico para prevenir a disseminação linfática); itraconazol 200-400mg/d sozinho ou combinado com 5-fluorocitosina 30mg/kg 4 vezes ao dia durante 6 meses; terbinafina 250-500mg/d durante 12 meses, e no caso de envolvimento sistêmico, anfotericina B intravenosa na dose de 1mg/kg ou lipossomal ou formulações lipídicas de anfotericina B na dose de 3-5mg/kg/d.27
Micetoma
Micetoma é uma infecção local crónica causada por várias espécies de fungos e bactérias. A infecção é chamada actinomicetoma quando é causada por bactérias filamentosas aeróbias e eumicetoma quando é causada por fungos.34 É caracterizada pela formação de agregados dos microrganismos causadores em abcessos. Estes agregados são conhecidos como grãos ou grânulos. Os grânulos podem drenar através da abertura dos seios nasais para a pele ou afectar os ossos adjacentes. A doença avança via propagação directa, com muito poucos casos de disseminação para locais distantes. Os agentes causadores são geralmente encontrados no solo e entram no corpo através da pele quebrada. A maioria dos casos envolve trabalhadores rurais.
Etiologia
-
Fungi. Os fungos que causam o eumycetoma produzem grânulos brancos ou escuros. Eles são particularmente comuns na África, Índia e México. Os grânulos escuros são formados por Madurella mycetomatis, Trematosphaeria grisea e Leptosphaeria senegalensis,35 enquanto os grânulos brancos são formados por Fusarium spp., Acremonium spp. e Aspergillus nidulans.
-
Bactérias filamentosas ou actinomycetes aeróbicos. Os grânulos formados por estas espécies são vermelhos (Actinomadura pelletieri), brancos-amarelos (Actinomadura madurae, Nocardia brasiliensis, e Nocardia spp.), ou amarelo-acastanhados (Streptomyces somaliensis). Actinomycetes são encontrados em todo o mundo, não apenas em países tropicais.36
Formas clínicas
As características clínicas do micetoma causado por fungos e actinomycetes são muito semelhantes. As lesões são mais comuns nos pés, nas canelas e nas mãos. A manifestação clínica mais precoce é um nódulo duro e indolor que se espalha lentamente para produzir pápulas e seios nasais que liberam fluido contendo grânulos na superfície da pele.35,36 O local original da infecção é distorcido pelo inchaço dos tecidos locais, formação de seios nasais crônicos e envolvimento ósseo tardio (Fig. 3). As lesões são raramente dolorosas, exceto em estágios tardios.
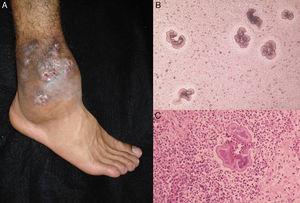 Figure 3.
Figure 3.A, Actinomicetoma do pé. B, Nocardia sp. granulado visto em exame directo (KOH, ampliação original ×10). C, Biopsia (hematoxilina-eosina ×40).
(0.27MB).Diagnóstico
Mycetoma granulado (Fig. 3) é um achado diagnóstico chave e é geralmente encontrado no exame de corrimento dos seios nasais ou na trituração de uma crosta retirada de uma lesão. O exame microscópico mostrará se estes grânulos são formados por pequenos actinomicetos ou por filamentos micoscóticos mais largos. A identificação definitiva requer cultura, que normalmente é realizada em SDA com ou sem antibióticos (cloranfenicol e ciclo-heximida); só cloranfenicol é preferível no caso de fungos hialinos. Os agentes também podem ser identificados através de testes de biologia molecular, particularmente análise por PCR usando diferentes marcadores37 dependendo dos agentes causadores (por exemplo, regiões ITS do rDNA, β-tubulin,38 e D1/D2). A análise parcial da sequência genética do RNA ribossómico, pelo contrário, pode ser usada para identificar espécies de Nocardia e Actinomadura.36 Os resultados histológicos são semelhantes em todas as formas de micetoma e incluem um centro inflamatório rico em células polimorfonucleares (verdadeiros abcessos), células epitelioides, células gigantes e fibrose. Os grânulos estão localizados no centro da inflamação.35,39 Estudos de imagem, embora complementares, podem auxiliar no diagnóstico mostrando edema de partes moles, lesões osteolíticas e espessamento cortical.
O diagnóstico diferencial deve incluir osteomielite bacteriana, osteomielite tuberculosa, hidradenite supurativa, sarcoma de Kaposi e tuberculose cutânea, entre outros.35,39
Tratamento
Actinomicetoma. O regime de tratamento com a base de evidência mais forte para o micetoma do miocárdio é o trimetoprim-sulfametoxazol mais diaminodifenil sulfona (dapsona) por 6 meses a 2 anos. O ácido amoxicilina-clavulânico, administrado durante 6 meses, pode ser usado para casos refratários.40-42 O tratamento de escolha para infecção extensa e/ou envolvimento visceral é amikacina combinada com trimetoprim-sulfametoxazol39 ou meropenem.43,44 Houve relatos isolados de resultados bem sucedidos com outros agentes em pacientes que não responderam a estes tratamentos.36,39,45
Eumicetoma. Ao contrário do actinomicetoma, onde o tratamento farmacológico está associado a bons resultados, o tratamento padrão no eumicetoma é uma combinação de tratamento médico e cirurgia. Resultados aceitáveis têm sido relatados para o uso de triazóis de última geração, tais como itraconazol e fluconazol usado sozinho ou em combinação com terbinafina. Estas drogas são administradas durante um longo período e somente após esgotar todas as opções cirúrgicas.35,45
Faeohyphomycosis
Faeohyphomycosis é um grupo heterogêneo de micoses causadas por fungos de parede escura (demáceos).46,47 Estes fungos são encontrados em todos os climas, embora sejam mais comuns em climas tropicais. Tem havido um aumento recente de casos entre pacientes imunossuprimidos com infecção pelo HIV ou AIDS, receptores de transplante e pacientes diabéticos, entre outros.46,48
Os agentes causadores mais comuns são Exophiala spp, Bipolaris spp., Curvularia spp., Pleurophomopsis spp., Phaeoacremonium spp. e Alternaria spp. Os fungos são encontrados principalmente em detritos orgânicos.
Formulários clínicos
-
Faeohomicose subcutânea. Após trauma local ou inoculação com material estranho, os pacientes desenvolvem uma lesão solitária de crescimento lento (geralmente um cisto ou um nódulo, ou possivelmente uma placa ou abscesso) normalmente localizada nas extremidades (Fig. 4).48,49 O diagnóstico diferencial deve incluir lipomas, cistos epidérmicos ou sinoviais, fibromas, cistos de corpo estranho e abscessos bacterianos.
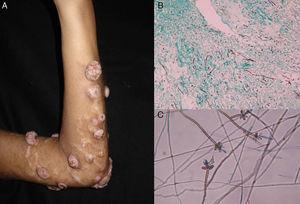 Figure 4.
Figure 4.A, Fa-hifomicose nodular. B, Filamentos e leveduras em amostra de biópsia (Grocott, ampliação original ×10). C, Exame microscópico da Veronaea botryosa (lactofenol azul de algodão, ampliação original ×40).
>
>
(0.22MB).>>
>
>
- >
Faeohomicose sistémica ou disseminada. Embora muito rara, a feofomicose sistêmica é muito grave em pacientes imunossuprimidos.50
>
Diagnóstico
Microscopia de montagem úmida mostra o diagnóstico de hifas de septo escuro formando ramos ou cadeias (Fig. 4). O crescimento é lento (3-4 semanas) em SDA e as colônias adquirem uma cor olivácea ou marrom escuro. A análise por PCR de marcadores como β-tubulin e regiões ITS pode ser usada para identificação molecular.51,52 A biópsia revela uma parede cística formada por macrófagos paliçadores com hifas micotrópicas.49
Tratamento
O tratamento de infecções causadas por Exophiala spp. é controverso, e uma opção que tem sido proposta é a ressecção cirúrgica.48 Também não há protocolos padrão para o tratamento de infecções por Alternaria.53 A melhor opção para a feofomicose parece ser uma combinação de terapia antifúngica (itraconazol, cetoconazol ou terbinafina) e cirurgia. As cepas de Exophiala spp. tendem a ser resistentes ao fluconazol. Infecções disseminadas são tratadas com anfotericina B.48,49
Hyalohyphomycosis
Hyalohyphomycosis é causada por fungos hialinos (Hyphomycetes) que formam hifas sépticas no tecido.47 Esta classificação, no entanto, é bastante arbitrária já que existem muitos tipos de Hyphomycetes terrestres e aquáticos. Apenas alguns organismos, no entanto, podem causar infecções, a maioria das quais são oportunistas, em humanos.54,55 A maioria dos gêneros envolvidos na hialofomicose são morfologicamente idênticos quando observados em seções teciduais e desencadeiam a mesma resposta patológica. Os agentes mais comuns envolvidos na hialofomicose são Aspergillus (fumigatus, niger, flavus), Scopulariopsis spp., Fusarium spp., Acremonium recifei, Paecilomyces spp., Purpureocillum spp., e Neoscytalidium spp.55 Todas elas estão amplamente distribuídas na natureza e podem ser encontradas em qualquer tipo de solo, madeira ou material vegetal em decomposição.56 Elas afetam indivíduos de qualquer sexo e em qualquer idade e a imunossupressão não é uma condição necessária para infecção.
Formas clínicas
Hyalohyphomycosis podem ser classificadas como superficiais, subcutâneas ou sistêmicas.
-
Halohyphomycosis superficial. As infecções superficiais incluem dermatomicose e onicomicose. São comuns em trabalhadores rurais, pescadores, pacientes com queimaduras graves e neonatos prematuros.57,58
-
Hialofomicose subcutânea. A inoculação traumática causa abscessos, cistos e lesões tumorais semelhantes às observadas no micetoma (Fig. 5).56
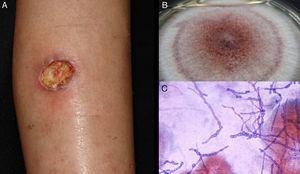 Figure 5.
Figure 5.Ulceração da hialofomicose por Acremonium sp. B, Cultura (meio de ágar Sabouraud dextrose). C, Exame directo do exsudado (Giemsa, ampliação original ×40).
(0.17MB).>
- Hialofomicose sistémica. As infecções sistémicas, embora pouco comuns, são muito graves. Elas afetam pacientes imunossuprimidos e podem ser fatais. A disseminação hematogênica e linfática leva ao envolvimento dos pulmões e do sistema nervoso central.55,57
- 2)
Diagnóstico
Identificação de hifas hialinas sépticas pelo exame microscópico de escamas de pele, fragmentos de unhas, secreções ou fragmentos fornece um diagnóstico presuntivo, que é então confirmado pela cultura (Fig. 5). A maioria dos fungos cresce em SDA sem antibióticos ou inibidores.47,59 Como nos casos descritos acima, a identificação molecular também é possível.60
O diagnóstico diferencial deve incluir outras dermatomicoses, cistos epidérmicos, actinomicetoma, eumicetoma, histoplasmose e criptococose.
Tratamento
Em indivíduos imunocompetentes, os tratamentos de escolha são triazóis, terbinafina ou cirurgia.61 Quando o sistema imunológico está comprometido, o tratamento de primeira linha é a anfotericina B combinada com um triazol (itraconazol 200mg/d durante 6 meses ou fluconazol 150mg duas vezes por semana durante 6 meses).
Lacaziose (Lobomicose)
Lacaziose, anteriormente conhecida como lobomicose, é uma infecção fúngica granulomatosa crônica da pele e tecidos subcutâneos descrita pela primeira vez sob o nome de blastomicose queloidal em 1930 por Jorge Lobo em Recife, Brasil.62 É uma infecção rara encontrada na América Central e do Sul; é causada pela Lacazia loboi,62,63 uma levedura que não pode ser cultivada em cultura. Pensa-se que a fonte da infecção esteja no solo e na vegetação. O fungo provavelmente entra pela pele após uma lesão penetrante, como uma picada de espinho ou picada de inseto.
Lacaziose é caracterizada por lesões queloidais com bordas lobuladas bem definidas em áreas expostas do corpo (freqüentemente a face, braços ou pernas). As lesões se espalham para locais contíguos, embora a transmissão para locais distantes também seja possível via autoinoculação.
Diagnóstico
Diagnóstico é facilitado pela identificação de estruturas fúngicas abundantes durante o exame direto e cadeias de células redondas difusas conectadas por pequenas estruturas tubulares em amostras de biópsia.62 Agentes causadores também podem ser identificados nos tecidos através da análise por PCR, em particular ensaios que visam o fragmento de rDNA 18S.64
O diagnóstico diferencial deve incluir quelóides, lepra lepromatosa e leishmania anergica.
Tratamento
Antifúngicos não são efetivos na lacasiose e o tratamento definitivo é a ressecção cirúrgica.62,63
Zigomicose
Zigomicose é um grupo heterogêneo de infecções fúngicas causadas por Zigomicetos oportunistas das ordens Mucorales (Rhizopus, Lichtheimia, Mucor, e Rhizomucor) e Entomophthorales (Basidiobolus e Conidiobolus).65 Nesta seção, discutiremos apenas os fungos Entomophthorales, pois os Mucorales são abordados na segunda parte desta revisão, que aborda as micoses sistêmicas.
Entomophthoromycosis é caracterizada pelo aparecimento de uma massa dura e progressiva que afeta os tecidos subcutâneos. Existem 2 variantes. A primeira é causada pelo Basidiobolus ranarum e é mais comum em crianças.66 As lesões geralmente aparecem no ombro e nas cintas pélvicas, e se apresentam como uma celulite lenhosa de lenta propagação. A segunda variante é causada pelo Conidiobolus coronatus e afeta adultos. A infecção primária começa nas turbinas inferiores do nariz e depois se espalha para o centro da face, causando inchaço endurecido e deformação severa do nariz, lábios e bochechas.65-68
Conclusão
Revisamos as principais características das micoses subcutâneas e os principais métodos de diagnóstico e tratamento disponíveis (Tabela 1).
Sumário das Características das Micoses Subcutâneas.
>
| Micose | Agente Causal Principal | Diagnóstico | Tratamento |
|---|---|---|---|
| Sporotricose | Sporothrix schenckii | Cultivo de pus aspirado a partir de nódulos; histologia; PCR | Solução saturada de iodeto de potássio para 3 wk; itraconazol 200mg/d para 3-6 mo; combinações |
| Cromoblastomicose | Fonsecaea pedrosoi | Exame microscópico; cultura; histologia | Muito difícil. Itraconazol 200mg/d para 6 mo; terbinafina para 12 mo; anfotericina B; combinações |
| Micetoma | Filamentosos actinomicetos e fungos filamentosos | Identificação de grânulos de micetoma; cultura; histologia; PCR | Antibióticos para actinomicetoma; antifúngicos+cirurgia para eumicetoma |
| Faeohifomicose | Exophiala jeanselmei Alternaria spp. |
Exame microscópico e cultura; histologia; PCR | Controversos. Cirurgia+combinação de antifúngicos |
| Hyalohyphomycosis | Opportunistic Aspergillus (fumigatus, niger, flavus), Fusarium spp., Paecilomyces, etc. | Exame microscópico e cultura; PCR | Doentes imunocompetentes: triazóis; terbinafina; ciclopirox olamina; cirurgia Doentes imunossuprimidos: anfotericina B combinada com um triazol para 6 mo |
| Lacaziose (lobomicose) | Lacazia loboi | Exame microscópico; histologia; PCR | Cirurgia |
| Entomophthoromycosis | Conidiobolus coronatus Basidiobolus ranarum |
Exame directo e cultura | Cirurgia e antifúngicos sistémicos |
A abreviatura: PCR, reação em cadeia da polimerase.
Conflitos de interesse
Os autores declaram que não têm conflitos de interesse.